- Способы получения кремния основаны в основном на восстановлении оксида кремния (IV) сильными восстановителями – активными металлами (Mg, Al) и углеродом. Сначала получают чистый кремний, достаточно смешать песок с углем и нагреть до 18000 .
Лабораторный способ: SiO2 + 2Mg = 2MgO + Si 1900oC Промышленный способ: SiCl4 + 2Zn = 2ZnCl2 + S SiO2 + 2C = 2CO + Si
6. Химические свойства (слайд 14) Химические свойства кремния мы рассмотрим по следующей схеме: 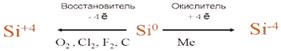
а ) кремний - восстановитель
Все реакции протекают при нагревании!
- В/д с кислородом
Si + O2 = SiO2 (оксид кремния (IV))
Si0 – 4e- = Si+4 восстановитель
O2 + 4e- = 2O-2 окислитель
- В/д с галогенами
Si + 2Cl2 = SiCl4 (хлорид кремния)
- В/д с неМе
Si + 2S = SiS2 (сульфид кремния)
20000C
Si + C = Si+4C-4
(карбид кремния или карборунд, по твёрдости близок к алмазу)
- В/д со сложными в-вами
Si + 2H2O(пар) = SiO2 + H2
Si + 2NaOH(конц.) + H2O = Na2SiO3 + 2H2
б) кремний – окислитель
1.В/д с Ме
Si + 2Ca = Ca2Si (силицид кальция)
2Mg + Si= Mg2Si (силицид магния)
Вывод: свойства кремния и углерода похожи. Оба неметалла взаимодействуют с кислородом, галогенами, серой, металлами. Но в отличие от углерода кремний напрямую не соединяется с водородом. Si+ H2 /=
Применение • Полупроводниковые материалы • Кислотоупорные сплавы • Затачивание резцов металлорежущих станков • Шлифовка драгоценных камней • Производство стекла и цемента • Силикатная промышленность (керамика, кирпич, фарфор, фаянс)
Соединения кремния
Свойства кремнезёма
Учитель подробно рассматривает свойства оксида кремния (IV) и проводит сравнительный анализ двух оксидов – SiO 2 и CO 2. результаты обсуждения в виде таблицы выводятся на экран.
Обратите внимание на одно важное свойство оксида кремния:
SiO2 + 4HF = 2H2O + SiF4
Оксид кремния входит в состав стекла, поэтому плавиковую кислоту нельзя хранить в стеклянной посуде.
Вывод: физические свойства оксидов резко отличаются, т.к. они образуют разные кристаллические решётки – молекулярную (CO2) и атомную (SiO2), но химические свойства схожи. Отличие состоит в различном отношении к воде.
I. SiO2 - оксид кремния (IV), песок, кварц, кремень – нерастворимое в воде твердое вещество, очень тугоплавкое, tпл. =17000 С. Атомная кристаллическая решетка.
Кварц – белый – горный хрусталь – поделочный камень;
Молочный, серый, дымчатый – опал, агат, яшма, халцедон
Кремень – имеет очень острые края; в древности изготавливали орудия труда и оружие.
Химические свойства: SiO2 - кислотный оксид
Это кислотный оксид, а для таких оксидов характерно взаимодействие с водой, основным оксидом и щелочью, но
1.)В/д с водой
SiO 2 + H 2 O не взаимодействует
При сплавлении взаимодействует с основными оксидами, щелочами, а также с карбонатами щелочных и щелочноземельных металлов с образованием солей — силикатов:
2. В/д с оксидами
SiO2 + CaO → CaSiO3
3.В/д с щелочами
SiO2 + 2NaOH → Na2SiO3 + H2O
4. В/д с карбонатами щелочных и щелочноземельных металлов с образованием солей — силикатов:
SiO2 + CaCO3 → CaSiO3 + CO2
SiO2 + K2CO3 → K2SiO3 + CO2
Окислительно — восстановительные реакции
Взаимодействие с металлами
При температуре выше 1000 °С реагирует с активными металлами,
при этом образуется кремний:
SiO2 + 2Mg → Si + 2MgO
II. H2SiO3 – кремниевая кислота.
Оксид кремния – песок, нерастворимый в воде. Следовательно, получить кремниевую кислоту растворением ее соответствующего оксида в воде невозможно. Ставится проблемный вопрос: «Как получить кремниевую кислоту?» H2SiO3 — очень слабая (слабее угольной), непрочная, в воде малорастворима (образует коллоидный раствор).
-кремниевая кислота H 2 SiO 3 -единственная нерастворимая неорганическая кислота, - двухосновная, - слабая H2SiO3 = H2O +SiO2
При высыхании образует силикагель, используемый в качестве адсорбента.
Получить кремниевую кислоту можно только из её солей.
Проведение лабораторного опыта и составление уравнения реакции получения кремниевой кислоты (самостоятельно, на доске)
Лабораторный опыт:
Качественные реакции на силикат-ион (Повторение ТБ).
Ход работы: Обнаружение силикат-иона. В пробирку налейте 1 мл силиката натрия прилейте по каплям раствор соляной кислоты. Что наблюдаете? Сделайте вывод о способе обнаружения силикат-ионов?
1. Na2SiO3 + 2HCl = 2NaCl + H2SiO3
SiO32- + 2Н+ = H2SiO3
2.При нагревании разлагается:
H2SiO3 –t°→ H2O + SiO2
Силан SiH 4 (слайд 17)
-Силан получают косвенно, действуя на силициды металлов водой или кислотами:
Mg2Si + 4H2O = 2Mg(OH)2 + SiH4
Силан – бесцветный газ, самовоспламеняющийся на воздухе и сгорающий с образованием оксида кремния и воды:
SiH4 + 2O2 = SiO2 + 2H2O