

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...
Топ:
Генеалогическое древо Султанов Османской империи: Османские правители, вначале, будучи еще бейлербеями Анатолии, женились на дочерях византийских императоров...
Когда производится ограждение поезда, остановившегося на перегоне: Во всех случаях немедленно должно быть ограждено место препятствия для движения поездов на смежном пути двухпутного...
Основы обеспечения единства измерений: Обеспечение единства измерений - деятельность метрологических служб, направленная на достижение...
Интересное:
Финансовый рынок и его значение в управлении денежными потоками на современном этапе: любому предприятию для расширения производства и увеличения прибыли нужны...
Распространение рака на другие отдаленные от желудка органы: Характерных симптомов рака желудка не существует. Выраженные симптомы появляются, когда опухоль...
Мероприятия для защиты от морозного пучения грунтов: Инженерная защита от морозного (криогенного) пучения грунтов необходима для легких малоэтажных зданий и других сооружений...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Тот факт, что при реакциях окисления и горения, при реакциях нейтрализации энергия всегда выделяется, говорит о том, что ещё до реакции вещества обладали запасом энергии Е.
Энергия Е, скрытая в веществе и выделившаяся при химических процессах, называется внутренней энергией (U, кДж/моль).
Внутренняя энергия зависит от температуры и объёма, различают энергию потенциальную и энергию кинетическую.
U = Uпот. + Uкин.
Uпот. – энергия взаимодействия всех частиц вещества, обусловленная силами притяжения и отталкивания.
Uкин. – энергия движения элементарных частиц ядра, колебаний ядер атомов, движения электронов, молекул вещества.
Определить или рассчитать абсолютное значение внутренней энергии U не представляется возможным, так как это нельзя экспериментально определить. Но можно определить разницу (изменение U)
 .
.
Пусть вещества (химические системы) переходят из состояния 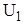 в состояние
в состояние 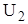 . Допустим, при этом системы поглощают тепло, процесс будет эндотермическим, тогда тепло, поглощенное системой будет затрачиваться на совершение работы расширения Qпогл.
. Допустим, при этом системы поглощают тепло, процесс будет эндотермическим, тогда тепло, поглощенное системой будет затрачиваться на совершение работы расширения Qпогл.
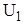 →
→ 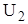 ;
;
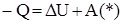 .
.
Уравнение указывает, что если к системе подводится теплота Q, то, в общем случае, она расходуется на изменение её внутренней энергии 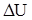 и на совершение работы A.
и на совершение работы A.
Под внутренней энергией системы подразумевается общий её запас, включая энергию поступательного и вращательного движения молекул, энергию движения электронов в атоме, внутриядерную энергию, то есть все виды энергии, кроме кинетической и потенциальной. Под величиной А понимают работу против всех сил, действующих на систему (внешнее давление, электрическое и магнитное поля).
|
|
В изохорном состоянии при V = const
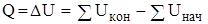 ;
;
Ap = 0.
Поэтому, в этом процессе 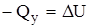 .
.
Для экзотермических процессов 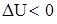 , для эндотермических процессов
, для эндотермических процессов 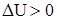 .
.
В изобарных условиях при р = const
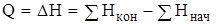 ;
;
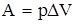 .
.
Подставим значения работы в (*) и получим первый закон сохранения энергии
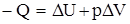 .
.
Тепло, поглощенное системой, затрачивается на приращение внутренней энергии 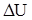 и на совершение работы внешних сил.
и на совершение работы внешних сил.
Закон сохранения энергии:
Энергия не может ни создаваться, ни исчезать. Она может только переходить из одной формы в другую. Она не исчезает бесследно.
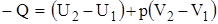 ;
;
 .
.
Сумма внутренней энергии и произведение давления на объем в термодинамике называется энтальпией.
 , [H] = кДж/моль;
, [H] = кДж/моль;
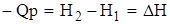 .
.
Тепловой эффект при р – const равен изменению энтальпии, но противоположен ей по знаку.
Энтальпию H невозможно определить и посчитать, но можно определить её изменение  при химических процессах.
при химических процессах.
Энтальпия H – это сложная термодинамическая функция состояния системы, характеризующая полный запас энергии системы.
|
| |
| Экзотермический | Эндотермический |
Теплота образования сложных веществ
Изменение энтальпии H при образовании одного моля сложного вещества из одного моля простых веществ при стандартных условиях (р = 101,3 кПа, Т = 298 К) называется теплотой образования вещества. Обозначается  °298°обр.
°298°обр.

 может принимать положительные и отрицательные значения.
может принимать положительные и отрицательные значения.  простых веществ равно нулю (
простых веществ равно нулю ( = 0). Чем отрицательнее значение принимает
= 0). Чем отрицательнее значение принимает  °298, тем больше выделяется тепла при образовании вещества, тем меньшим запасом обладает образовавшееся вещество и тем оно более устойчивое. Если
°298, тем больше выделяется тепла при образовании вещества, тем меньшим запасом обладает образовавшееся вещество и тем оно более устойчивое. Если  > 0, то такое вещество является термодинамически неустойчивым.
> 0, то такое вещество является термодинамически неустойчивым.
|
|
|
|
|

Археология об основании Рима: Новые раскопки проясняют и такой острый дискуссионный вопрос, как дата самого возникновения Рима...

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!