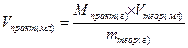Базовые растворы готовятся из химически чистых коммерческих субстанций с известной активностью.
Нельзя использовать соответствующие лечебные препараты!
При расчетах следует учитывать наличие в субстанции балластной части, которая в некоторых солях антибиотиков составляет значительную долю. Активность субстанции, как правило, указана на упаковке и выражается либо в процентном содержании действующего вещества, либо в милиграммах действующего вещества на 1 г субстанции.
Во втором случае для того чтобы вычислить процентное содержание активного вещества, необходимо значение активности, выраженное в мг/г, разделить на 10. Если активность субстанции не указана на упаковке, ее условно принимают за 100%.
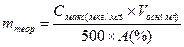 Например, необходимо приготовить серийные разведения ампициллина в диапазоне от 16 до 0,016 мг/л. Объем базового раствора – примерно 50 мл.
Например, необходимо приготовить серийные разведения ампициллина в диапазоне от 16 до 0,016 мг/л. Объем базового раствора – примерно 50 мл.
где
mтеор. – теоретическая масса навески с учетом активности субстанции,
Vосн. – объем базового раствора,
А – активность субстанции, выраженная в процентах.
mтеор. = 16 (мг/л) x 50(мл) / 500 x 100 = 0,016 (г).
Как правило, абсолютно точно взвесить необходимое количество антибиотика не удается. Чтобы получить в таком случае базовый раствор необходимой концентрации, следует варьировать объемом растворителя. Этот объем рассчитывают по формуле:
где
Vпракт. – практический объем растворителя,
Vтеор. – теоретический объем растворителя,
mпракт. – практическая масса навески,
mтеор. – теоретическая масса навески.
V практ. = 0,01654 (г) x 50 мл / 0,016 (г) x 51,7 (мл).
Рекомендуемые растворители и разбавители субстанций антибиотиков приведены в табл. 10.
Приготовленный базовый раствор разливается в стерильных условиях небольшими объемами (для тестирования 1, 2, 3.... N штаммов) и хранится при отрицательной температуре Ј–20оC в среднем в течение 6 нед.
Не следует хранить готовые базовые растворы в холодильниках с автоматической системой оттаивания, так как повторное размораживание и замораживание приводит к разрушению антибиотика. По этой же причине нельзя хранить размороженный базовый раствор.
Таблица 10. Растворители субстанций антибиотиков
| Субстанция
| Растворитель
| Разбавитель
|
| Ампициллин
| Фосфатный буфер, рН=8,0, 0,1 М
| Фосфатный буфер, рН=6,0, 0,1 М
|
| Амоксициллин
| Фосфатный буфер, рН=8,0, 0,1 М
| Фосфатный буфер, рН=6,0, 0,1 М
|
| Триметоприм
| 0,05 N молочная кислота или соляная кислота, 10% от необходимого объема (или 1,0 мл 0,1 М NaOH на каждые 10 мг субстанции)
| Вода (стабилен при температуре 4оС, может нуждаться в нагревании)
|
| Сульфаметоксазол
| 1/2 объма - горячая вода и минимальное количество 2,5 М NaOH для растворения (или 1,0 мл 0,1 М NaOH на каждые 10 мг субстанции)
| Вода
|
| Цефотаксим или
| Вода
| Вода
|
| Цефтриаксон, или
|
|
|
| Цефтазидим
|
|
|
| Меропенем
| Вода
| Вода
|
| Хлорамфеникол
| Этанол или метанол
| Вода
|
| Азитромицин или
| Этанол или метанол
| Вода
|
| Кларитромицин
| Этанол или метанол
| Вода
|
| Тетрациклин
| Вода
| Вода
|
Л и т е р а т у р а
1. Haemophilus. In: Koneman E.W., Allen S.D., Janda W.M., Schreckenberger P.C., Winn W.C., editors. Color Atlas and Textbook of Diagnostic Microbiology. 5th ed. Lippincott: Philadelphia;1997. p.363-94.
2. Pittman M. Variation and type specificity in the bacterial species Haemophilus influenzae. J Exp Med 1931; 53:471-92.
3. Kiehn T.E., Verhoef J. Haemophilus spp. In: Armstrong D., Cohen J., editors. Infectious diseases. Harcourt Publishers Ltd; 1999. p.8-20.7-20.11.
4. Spinola S.M., Peacock J., Denny F.W., et al. Epidemiology of colonization with nontypable Haemophilus influenzae in children: A longitudinal study. J infect Dis 1986; 154:100-9.
5. Harabuchi Y., Faden H., Yamanaka N., et al. Nasopharyngeal colonization with nontypeable Haemophilus influenzae and recurrent otitis media. J Infect Dis 1994; 170: 862-6.
6. Murphy T.F. Haemophilus. In: Gorbach S.L., Bartlett J.G., Blacklow N.R., editors. Infectious Diseases. 2nd ed. W.B. Saunders Company; 1998. p. 1845-58.
7. Orenstein W., Wharton M., Bart K.J., Hinman A.R. Immunization. In: Mandell G.L., Bennett J.E., Dolin R., editors. Principles and practice of infectious diseases. 5th ed. Churchill Livingstone; 2000. p. 3213-4.
8. Campos J.M. Haemophilus spp. In: Murrey P.R., Baron E.J., Pfaller M.A., Tenover F.C., Yolken R.M., editors. Manual of Clinical Microbiology. 7th ed. ASM Press; 1999. p.604-13.
9. Felmingham D., Washington J. Trends in antimicrobial susceptibility of bacterial respiratory tract pathogens – findings of the Alexander project 1992-1996. J Chemother 1999; 11:5-21.
10. Jacoby G.A. Prevalence and resistance mechanisms of common bacterial respiratory pathogens. Clin Infect Dis 1994;18:951-7.
11. Fuchs P.C., Barry A.L. Interpretative criteria for susceptibilities of Haemophilus influenzae to ampicillin, amoxicillin and amoxicillin/clavulanate. J Clin Microbiol 1994; 32:2846-50.
12. Crokaert F., Aoun M., Duchateau V. Are macrolides active against Haemophilus influenzae? Are the in vitro tests reliable? Proceedings of the 35th ICAAC, San Francisco, 1995.
13. Acar J. Resistance patterns of Haemophilus influenzae. J Chemother 1999; 11:44-50.
14. National Committee for Clinical Laboratory Standards. Performance standards for antimicrobial susceptibility testing; ninth informational supplement. NCCLS Document M100-S9 1999;19(1).
15. National Committee for Clinical Laboratory Standards. Methods for dilution antimicrobial susceptibility tests for bacteria that grow aerobically. Approved standard. 5th ed. NCCLS Document M7-A5 2000;20(2).
16. National Committee for Clinical Laboratory Standards. Performance standards for antimicrobial susceptibility testing; tenth informational supplement. NCCLS Document M100-S10(M7) 2000.
17. Leitch C., Boonlayangoor S. -Lactamase test. In: Isenberg H.D. Clinical microbiology procedures handbook. ASM; 1992. p.5.3.1.
[1] Рекомендованы Межрегиональной ассоциацией по клинической микробиологии и антимикробной химиотерапии (МАКМАХ), Научно-исследовательским институтом антимикробной химиотерапии Смоленской государственной медицинской академии



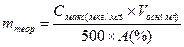 Например, необходимо приготовить серийные разведения ампициллина в диапазоне от 16 до 0,016 мг/л. Объем базового раствора – примерно 50 мл.
Например, необходимо приготовить серийные разведения ампициллина в диапазоне от 16 до 0,016 мг/л. Объем базового раствора – примерно 50 мл.