Мы уже говорили о том, что процессы плавления и кристаллизации — это довольно-таки сложные процессы. Поэтому полезно уметь графически изображать данные процессы на графике. На нём отображают все этапы перехода вещества из одного агрегатного состояния в другое. Для понимания того, как строятся подобные графики, рассмотрим некоторые примеры.
Итак, вы видите график зависимости температуры кристаллического вещества от времени его нагревания. На нём по оси абсцисс отложено время, а по оси ось ординат — температура вещества, в качестве которого у нас выступает лёд, находящийся в момент начала наблюдения при отрицательной температуре.
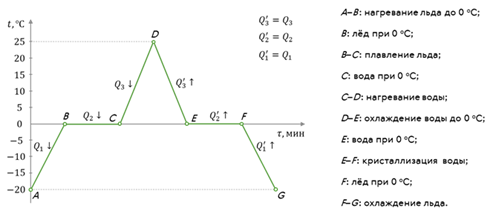
Обратите внимание на то, что начало оси времени совпадает с температурой плавления льда. Это очень важный момент, так как в дальнейшем, для удобства построения подобных графиков, мы будем стараться располагать начало оси абсцисс в точке, соответствующей температуре плавления вещества.
Из графика видно, что в момент начала наблюдения за процессом температура льда равнялась –20 оС.
Затем в течение некоторого промежутка времени лёд получает энергию, и его температура увеличивается до тех пор, пока не станет равной температуре плавления.
При этом обратите внимание на то, что в точке B, указанной на графике, — это ещё лёд — лёд, при температуре 0 oC. Т. е. молекулы ещё полностью сохраняют порядок, характерный для твёрдого тела.
Дальше мы с вами видим, что некоторое время температура остаётся постоянной, о чём свидетельствует горизонтальный участок графика BC. Это участок плавления. На нём происходит агрегатное превращение льда в воду. И вся энергия, которую получает вещество при плавлении, расходуется на разрушение порядка в расположении молекул тела.
В точке С лёд полностью превратится в воду, которая также имеет температуру 0 оС.
После того, как лёд полностью растаял, температура снова начала увеличиваться, что соответствует участку графика «CD». При этом жидкость всё ещё продолжает получать энергию.
Достигнув отметки в 25 oC (точка D на графике), воду перестали нагревать.
Следующий участок графика — участок DE. На нём мы видим, что вода начала остывать до 0 oC. Следовательно, её внутренняя энергия уменьшается и выделяется теплота. При этом выделится столько же теплоты, сколько жидкость получила на участке CD. Вспомните — тело, при нагревании или охлаждении на одно и тоже число градусов, получает или отдаёт одно и тоже количество теплоты.
Итак, в точке E у нас вода, находящаяся при 0 oC.
Далее, достигнув температуры кристаллизации, вода начала превращаться в лёд — участок графика EF. Это заняло какое-то время, в течение которого её температура вновь не менялась.
При этом происходило выделение такого же количества энергии, какое вещество поглотило на участке ВС. Выделение энергии связано с восстановлением порядка в расположении молекул тела.
Обратите внимание на то, что только в точке F вода полностью превратилась в лёд.
И последний участок графика соответствует охлаждению уже твёрдого тела до первоначальной температуры.
Запомните, что при построении графиков очень важно соблюдать масштаб, то есть равные интервалы, относящиеся к одной и той же величине, необходимо обозначать равным количеством клеток.
Таким образом, процесс перехода вещества из твёрдого состояния в жидкое, называется плавлением, а обратный процесс, т. е. переход вещества из жидкого состояния в твёрдое, кристаллизацией или отвердеванием, причем в течение всего процесса плавления температура тела не изменяется. И только когда тело полностью расплавиться, его температура начнёт повышаться.
Однако во время всего процесса плавления вещество получает энергию от какого-либо нагревателя. А из закона сохранения энергии следует, что она не может просто так исчезнуть. Тогда возникает закономерный вопрос: «На что расходуется энергия топлива во время плавления вещества?»
 Мы уже с вами знаем, что в кристаллических телах молекулы расположены в определённом строгом порядке. Однако даже в кристаллах молекулы совершают тепловое движение — колеблются около своих положений равновесия. Естественно, что при увеличении температуры тела, интенсивность этого колебания увеличивается, то есть происходит изменение характера и амплитуды колебаний частиц.
Мы уже с вами знаем, что в кристаллических телах молекулы расположены в определённом строгом порядке. Однако даже в кристаллах молекулы совершают тепловое движение — колеблются около своих положений равновесия. Естественно, что при увеличении температуры тела, интенсивность этого колебания увеличивается, то есть происходит изменение характера и амплитуды колебаний частиц.
Как следствие, увеличивается и их средняя кинетическая энергия. А когда тело нагреется до температуры плавления, то начнёт нарушаться порядок в расположении молекул в кристаллической решётке. Кристаллы начинают разрушаться — вещество плавится. Значит, подводимая в этот момент теплота идёт на разрушение кристаллической упорядоченной структуры вещества.
Вы знаете, что различные кристаллические вещества имеют разное строение — разные кристаллические решётки.

Следовательно, чтобы её разрушить при температуре плавления, необходимо затратить разную энергию, то есть сообщить веществу разное количество теплоты.
Физическая величина, численно равная количеству теплоты, которое необходимо передать твёрдому телу массой 1 кг при температуре плавления для перехода в жидкость, называется удельной теплотой плавления.
Обозначается удельная теплота плавления греческой буквой λ (лямбда).
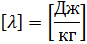
Разные вещества имеют разную удельную теплоту плавления, значение которой определяют экспериментально:

Также различные эксперименты показали, что удельная теплота плавления равна удельной теплоте кристаллизации.
Из таблицы видно, что, например, удельная теплота плавления ртути равна 12 000 Дж/кг. Это значит, что для перехода 1 кг ртути, имеющей температуру –39 оС, из твёрдого состояния в жидкое она должна поглотить 12 000 Дж теплоты. При обратном переходе столько же теплоты выделяет каждый килограмм ртути.
Также из таблицы видно, что лёд имеет сравнительно большую удельную теплоту плавления и кристаллизации. Это и объясняет затяжное таяние снега и льда озёр, рек и других водоёмов, что позволяет избежать больших паводков. А так как теплоту лёд поглощает из окружающей среды, то погода в это время, как правило, прохладная. И наоборот, при замерзании озёр, рек и других водоёмов выделяется большое количество энергии, что делает более тёплой позднюю осеннюю погоду.
Очевидно, что если известно количество теплоты, необходимое для плавления 1 кг ртути при температуре плавления, то для плавления 5 кг ртути нужно затратить количество теплоты в 5 раз больше, то есть 60 000 Дж.
Таким образом, чтобы вычислить количество теплоты необходимое для плавления вещества массой m взятого при температуре плавления, следует удельную теплоту плавления этого вещества умножить на его массу:
Q = λm
Эта же формула используется при вычислении количества теплоты, выделяющегося при кристаллизации жидкости.
Пример решения задачи.
Определите, какое количество теплоты поглощает лёд при 0 оС, если образовалось 5 кг воды?

8.11 Испарение. Насыщенный и ненасыщенный пар. Конденсация. Поглощение энергии при испарении жидкости и выделение ее при конденсации пара
На прошлых уроках мы с вами говорили о том, что существует три агрегатных состояния вещества — твёрдое, жидкое и газообразное.
И выяснили, что при агрегатных превращениях возможны переходы вещества из одного агрегатного состояния в другое.
На этом уроке мы рассмотрим процесс превращения жидкости в газ, и обратное превращение вещества из газообразного состояния в жидкое.
Задумывался ли кто-нибудь из вас над вопросом: почему сохнет мокрая одежда? И почему в ветреную погоду она высыхает значительно быстрее, чем в тихую и прохладную? А если оставить открытым флакон духов, то очень скоро он может оказаться пустым. Почему? Попытаемся ответить на эти и некоторые другие вопросы.
Для начала давайте вспомним, что молекулы вещества в любом его агрегатном состоянии находятся в непрерывном движении. Их скорости меняются самым случайным образом.
 Так, например, молекула жидкости, имеющая большую скорость, несомненно обладает и большой кинетической энергией. Такая молекула может преодолеть силы притяжения к другим молекулам и покинуть жидкость. А так как молекулы с большой энергией есть всегда, то со временем количество жидкости будет уменьшаться, а над жидкостью будет образовываться пар.
Так, например, молекула жидкости, имеющая большую скорость, несомненно обладает и большой кинетической энергией. Такая молекула может преодолеть силы притяжения к другим молекулам и покинуть жидкость. А так как молекулы с большой энергией есть всегда, то со временем количество жидкости будет уменьшаться, а над жидкостью будет образовываться пар.
Явление превращения жидкости в пар называется парообразованием.
Водяной пар невидим. А то, что мы свами часто ошибочно называем паром — например, белёсую струю, выходящую из кипящего чайника, — это не пар, а туман. Он состоит из крошечных капелек воды, образовавшихся при конденсации пара. Но об этом явлении мы поговорим позже.
Отличают два вида парообразования — это испарение и кипение. Они осуществляются при разных условиях.
Испарение — это парообразование, идущее со свободной поверхности жидкости.
А от чего зависит скорость испарения жидкости? Чтобы ответить на этот вопрос, давайте с вами проведём следующий опыт. На стекло нанесём тампоном влажные пятна одинаковых размеров в такой последовательности: подсолнечное масло, вода, ацетон. И проследим, какая жидкость испарится первой.

Через некоторое время мы заметим, что первым исчезнет пятно ацетона, затем воды, и позже всех — подсолнечного масла. Следовательно, скорость испарения зависит от рода жидкости. Это и понятно, ведь у разных жидкостей силы взаимодействия молекул неодинаковые.
Продолжим опыт. Одну стеклянную пластинку возьмём холодную, а другую нагреем. И нанесём на них две одинаковые капли воды.

С нагретого стекла капля исчезнет быстрее, чем с холодного.
И это неудивительно, поскольку чем выше температура жидкости, тем больше скорость движения её молекул, и, соответственно, их кинетическая энергия. Следовательно, большее число молекул способно преодолеть силы притяжения и выйти за пределы поверхности жидкости.




 Мы уже с вами знаем, что в кристаллических телах молекулы расположены в определённом строгом порядке. Однако даже в кристаллах молекулы совершают тепловое движение — колеблются около своих положений равновесия. Естественно, что при увеличении температуры тела, интенсивность этого колебания увеличивается, то есть происходит изменение характера и амплитуды колебаний частиц.
Мы уже с вами знаем, что в кристаллических телах молекулы расположены в определённом строгом порядке. Однако даже в кристаллах молекулы совершают тепловое движение — колеблются около своих положений равновесия. Естественно, что при увеличении температуры тела, интенсивность этого колебания увеличивается, то есть происходит изменение характера и амплитуды колебаний частиц.
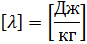


 Так, например, молекула жидкости, имеющая большую скорость, несомненно обладает и большой кинетической энергией. Такая молекула может преодолеть силы притяжения к другим молекулам и покинуть жидкость. А так как молекулы с большой энергией есть всегда, то со временем количество жидкости будет уменьшаться, а над жидкостью будет образовываться пар.
Так, например, молекула жидкости, имеющая большую скорость, несомненно обладает и большой кинетической энергией. Такая молекула может преодолеть силы притяжения к другим молекулам и покинуть жидкость. А так как молекулы с большой энергией есть всегда, то со временем количество жидкости будет уменьшаться, а над жидкостью будет образовываться пар.




