

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...
Топ:
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов...
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного...
Установка замедленного коксования: Чем выше температура и ниже давление, тем место разрыва углеродной цепи всё больше смещается к её концу и значительно возрастает...
Интересное:
Инженерная защита территорий, зданий и сооружений от опасных геологических процессов: Изучение оползневых явлений, оценка устойчивости склонов и проектирование противооползневых сооружений — актуальнейшие задачи, стоящие перед отечественными...
Как мы говорим и как мы слушаем: общение можно сравнить с огромным зонтиком, под которым скрыто все...
Влияние предпринимательской среды на эффективное функционирование предприятия: Предпринимательская среда – это совокупность внешних и внутренних факторов, оказывающих влияние на функционирование фирмы...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Поверхностные воды обезжелезивают при одновременном осветлении и обесцвечивании.
Железо, находящееся в воде в виде коллоидов, тонкодисперсных взвесей и комплексных органических соединений, удаляется обработкой воды коагулянтами (сульфатом алюминия, хлоридом железа(III), либо смешанным коагулянтом).
Для разрушения комплексных соединений железа воду обрабатывают хлором, озоном или KMnO4.
Оптимальным рН для коагуляции является 5,7-7,5.
В институте общей и неорганической химии АН УССР разработан метод обезжелезивания воды, состоящий в применении алюмината натрия и хлорида железа(III).
Оптимальное соотношение FeCl3 и NaAlO2 - 1:1. Кроме того, разработан метод удаления железа из воды пропусканием ее через взвешенный слой тонкодисперсного мела и гидроксида аммония.
Соли железа переводятся мелом в карбонат железа(II), который гидролизуется в гидроксид железа(II) и окисляется до гидроксида(III).
4CaCO3 + 4FeSO4 + O2 + 6H2O → 4Fe(OH)3 + 4CaSO4 + 4CO2
Обезжелезивание подземных вод
Для предварительного выбора метода обезжелезивания подземных вод необходимо руководствоваться следующим:
- обезжелезивания воды упрощенной аэрацией применяется для вод, содержащих до 10 мг/л общего железа (в т.ч. Fe(II) не менее 70%).
- рН не менее 6,8
- щелочность – более (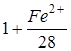 ) млэкв/л
) млэкв/л
- содержание сероводорода – не более 0,5 мг/л
Аэрированием из воды удаляется гидрокарбонат железа, который является не прочным, легко гидролизующимся в воде соединением:
Fe(HCO3)2 + 2H2O ↔ Fe(OH)2 + 2H2CO3
H2CO3 → H2O + CO2
Образующийся гидроксид (II) кислородом воздуха окисляется в III.
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
Удаление из воды марганца
Удалить из воды марганец можно следующими методами:
- обработкой воды перманганатом калия;
|
|
- аэрацией с подщелачиванием;
- фильтрованием через грубозернистый песок или катионит;
- окислением озоном, хлором или оксидом хлора.
Перманганат калия окисляет марганец (II) до оксида марганца (IV).
3Mn2+ + 2MnO4- + 2H2O → 5MnO2↓ + 4H+
Удаление марганца перманганатом калия из поверхностных вод осуществляют на фильтровальных станциях совместно с коагуляцией, фильтрованием или хлорированием.
Раствор KMnO4 вводят в воду в трубопровод насосной станции первого подъема до коогуляции.
Для удаления марганца из подземных вод применяют открытые напорные фильтры, загруженные песком на высоту 1,2 м. В этом случае KMnO4 подают насосами – дозаторами в трубопровод перед фильтрами.
Ионы Mn2+ могут быть удалены на Na – катионитовых фильтрах.
Фторирование и дефторирование воды
Интерес к фтору начал проявляться с 1931 г., когда ряд ученых доказали, что причиной заболевания флюорозом является повышенное содержание фтор – иона в питьевой воде.
Одновременно было установлено также, что и недостаток фторид-иона, т.е. его содержание ниже 0,1-0,2 мг/л приводит к заболеванию кариесом.
Эти данные позволили поставить вопрос о целесообразности искусственного обогащения хозяйственно – питьевой воды фтором при его недостатке и дефторировании воды при его избытке.
Впервые фторирование воды применили в США в 1945 г.
Многолетний опыт фторидирования воды в СССР дал положительные результаты, что позволило министерству здравоохранения рекомендовать повсеместно применять этот способ.
Согласно ГОСТ 2874-73 допустимая концентрация в воде фторид-иона для климатических районов не должна превышать, мг/л I, II – 1,5; III-1,2; IV-0,7.
Исходя из данных экспериментальных исследований профессора Габович в 1952 г. предложил воду по содержанию фторид-иона классифицировать так:
1. до 0,3 мг/л – очень низкая концентрация, поражаемость населения кариесом в 3-4 раза выше, чем при нормальной концентрации.
2. 0,3–0,7 мг/л – низкая концентрация фторид-иона, поражаемость населения кариесом в 1-3 раза больше.
|
|
3. 0,7–1,1 мг/л – оптимальная концентрация, поражаемость кариесом минимальная, флюороз в слабой форме наблюдается у 3-х % жителей.
4. 1,1-1,5 мг/л – повышенная, но допустимая. Процент населения с флюорозом достигает 15-20%
5. 1,5-2 мг/л – концентрация выше допустимой. Флюороз зубов у населения 30-40%
6. 2-4 мг/л – высокая концентрация. Флюороз 40-100%. Воду нужно дефторировать.
Устранение запахов, привкусов и токсических микрозагрязнений воды
Общие сведения
● Вода, используемая для хозяйственно-питьевых нужд, должна иметь высокие органолептические показатели (отсутствие окраски, мутности, привкусов и запахов). Для получения воды с такими свойствами применяют разные способы очистки. Проблема улучшения вкусовых показателей воды приобретает особое значение в связи с необходимостью использования поверхностных источников водоснабжения, поскольку запасов подземных вод не хватает.
● Дезодорация такой воды чрезвычайно осложняется из-за непрерывного загрязнения рек, озер и других водоемов стоками промышленных предприятий, часто содержащими значительные количества гомофазных примесей.
● Различают запахи и привкусы, вызываемые неорганическими соединениями (минеральные соли, сероводород) и органическими веществами. Запахи органического происхождения могут вызываться органическими веществами биологического происхождения, так и вносимые со стоками промышленных предприятий.
Появление в воде растворимых органических веществ биологического происхождения является следствием распада водных растений, планктоновых и бентосных организмов.
Наиболее интенсивно обогащается природная вода органическими веществами в период «цветения» водоёмов.
Сброс промышленных сточных вод в природные водоёмы приводят к загрязнению воды различными по составу и свойствам органическими свойствами. Среди них наиболее распространены углеводороды нефти и нефтепродуктов, фенолы и полифенолы, синтетические алифатические спирты и кислоты, поверхностно-активные вещества, пестициды и т.д.
Единых методов для устранения всех видов запахов и привкусов не существует, однако некоторые из них сами по себе или в сочетании с друг с другом обеспечивают требуемую степень дезодорации.
|
|
Когда вещества, продуцирующие неприятные запахи и привкусы находятся в состоянии взвесей и коллоидов, их удаляют из воды коагулированием.
● Запахи и привкусы, обусловленные повышенным содержанием неорганических веществ, находящиеся в молекулярном и ионном состояниях, можно удалять методами корректирования минерального состава воды (обессоливание, обезжелезивание, дегазация и др.).
● Запахи и привкусы, вызываемые органическими веществами биологического происхождения или органическими веществами сточных промышленных вод, являются наиболее стойкими. Удаляют их в большинстве случаев окислением, адсорбированием и аэрированием.
Окислительными методами хорошо удалятся из воды вещества, обладающие сильными восстановительными свойствами. К ним относятся: поли- и одноатомные фенолы, дубильные вещества и гумусовые кислоты, соли железа (ІІ), сероводород, нитриты.
2) Аэрирование воды.
● Запахи и привкусы, вызываемые органическими веществами биологического происхождения или органическими веществами сточных промышленных вод, являются наиболее стойкими.
Для удаления их в большинстве случаев необходимы специальные мероприятия.
● На протяжении десятилетий единственным методом устранения из природных вод привкусов и запахов, вызываемых органическими веществами, было аэрирование воды, основанное на летучести этих соединений.
● На практике аэрирование проводят в специальных установках – аэраторах барботажного, разбрызгивающего и каскадного типов.
● В аэраторах борботажного типа воздух, подаваемый воздуходувками, распределяется в воде дырчатыми трубами, подвещаными в резервуаре, рис. 14.1 (слайд 57).
Степень аэрирования регулируют изменением количества подаваемого кислорода.
3) Обработка воды окислителями.
● Интенсивный рост химической промышленности привёл к значительному ухудшению вкусовых качеств вод, забираемых из поверхностных источников водоснабжения, в связи с этим вопросы дезодорации воды стали первостепенными.
● В результате исследований были предложены реагенты, обладающие окислительными свойствами и эффективно устраняющие привкусы и запахи.
|
|
Так, ещё в 1913 году в Англии для дезодорации был применён перманганат калия, который удалял из воды привкус касторового масла.
● В настоящее время как профилактика для борьбы с хлорфенольным запахом и привкусом используют хлорирование с аммонизацией, которое не устраняет хлорфенольный запах, а предупреждает его возникновение. При введении в воду сначала аммиака, а потом хлора – хлорфенольные соединения не образуются. Метод хлорирования с аммонизацией применяется при содержании фенола в воде до 1 мг/л воды.
● В последние годы в практике водоочистки для дезадорации начали применять озонирование, что оказалось весьма перспективным.
Благодаря высокому окислительному потенциалу озон окисляет вещества, обуславливающие привкусы и запахи, которые обычно не окислятся другими реагентами. Время контакта 10-15 минут, дополнительных соединений не образуется. В результате озонирования вода приобретает освежающий запах и привкус, характерный для ключевых вод.
● Однако в случае высокого загрязнения воды органическими веществами озон из-за плохой его растворимости в воде не дает хорошего дезодорирующего эффекта. Например, углеводороды нефти окисляются озоном в карбоновые кислоты ступенчато, образуя в качестве промежуточных продуктов альдегиды и кетоны, обладающие неприятным запахом. Предельно допустимые концентрации альдегидов и кетонов в воде составляет 0,1-2,0 мг/л, в то время как ПДК для кислот 5-250 мг/л.
● И все же в практике наиболее распространенным способом дезодорации воды является ее хлорирование. Дезодорация активным хлором может быть использована при любой загрязненности, так как высокая растворимость хлора обеспечивает его дезодорирование в необходимом количестве.
Для различных загрязнений воды существуют оптимальные концентрации хлора.
При воздействии относительно малых концентраций хлора на фенол образуются хлорфенолы. Атомы хлора в этих соединениях не реакционноспособны. В то же время при взаимодействии Cl2 с NH3 образуется реакционноспособное вещество – монохлорамин, атом хлора которого является активным. Он активно воздействует на микроорганизмы, производя дезинфекацию воды. Такой активный хлор называется связанным.
Однако после обработки воды хлором она приобретает хлороформенный запах, который удаляется активированным углем.
|
|
|

Наброски и зарисовки растений, плодов, цветов: Освоить конструктивное построение структуры дерева через зарисовки отдельных деревьев, группы деревьев...

История развития пистолетов-пулеметов: Предпосылкой для возникновения пистолетов-пулеметов послужила давняя тенденция тяготения винтовок...

Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ - конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!