Теория координационных соединений, предложенная А. Вернером в 1893 году, до сих пор является основной теорией координационных соединений (для комплексов определенного вида). Рассмотрим ее основные положения.
1. Большинство элементов проявляет два типа валентности – главную и побочную.
2. Атом элемента стремится насытить не только главные, но и побочные валентности.
3. Побочные валентности атома строго фиксированы в пространстве и определяют геометрию комплекса и его различные свойства.
В современной химии синонимом главной валентности является степень окисления элемента (обозначим ее сплошной линией), а побочная валентность определяется как координационное число, то есть количество атомов непосредственно связанных с металлом при насыщении его побочной валентности (обозначим ее пунктирной линией).
В соответствии с изложенными представлениями Вернера строение первого из указанных в таблице 1 комплексов выглядело так, как показано ниже. Для остальных соединений стехиометрическое соотношение исходных веществ таково, что молекул аммиака не хватает для насыщения всех шести побочных валентностей и их насыщают ионы хлора. При этом хлор, насыщающий эти валентности меняет свое состояние и уже не может обмениваться в реакциях ионного обмена. Те же ионы хлора, которые насыщают только главные валентности имеют те же свойства, что и в исходном хлориде кобальта и, как и в последнем, могут замещаться или обеспечивать электропроводность комплекса.



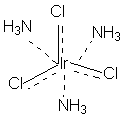
В последнем соединении все три хлора участвуют не только в насыщении главной, но и побочных валентностей. В связи с этим в нем нет «подвижных» ионов хлора и он не способен на ионные реакции и не проводит электрический ток.
Главная валентность обусловлена, как уже упоминалось, степенью окисления кобальта (+3), то есть электростатическим притяжением трех однозарядных ионов хлора и одного трехзарядного иона кобальта. Побочная же валентность обусловлена так называемым явлением координации, которое, с современных позиций, может иметь различную природу. Те ионы, атомы, молекулы, которые координируются ионом металла называют лигандами; вместе с ионом металла они образуют так называемую внутреннюю координационную сферу. Не трудно заметить, что, несмотря на различие в строении комплексов, количество лигандов в каждом случае равно шести, однако в первом из соединений ни один из ионов хлора не является лигандом, так как не входит во внутреннюю координационную сферу, а образует так называемую внешнюю сферу противоионов, которая для последнего из соединений в ряду полностью отсутствует.
Ионы, не входящие во внутреннюю координационную сферу, при растворении комплекса обуславливают его электропроводность. В соответствии с этим диссоциацию комплексов можно записать так:
[Co(NH3)6]Cl3 ↔ [Co(NH3)6]3+ + 3Cl-
[Co(NH3)5Cl]Cl2 ↔ [Co(NH3)5Cl]2+ + 2Cl-
[Co(NH3)4Cl2]Cl ↔ [Co(NH3)4Cl2]+ + Cl-
[Ir(NH3)3Cl3] – не диссоциирует
Таким образом, первые два тезиса теории Вернера закрывают вопросы 1 – 3. Остановимся подробнее на третьем тезисе теории Вернера, а именно на том, что побочные валентности фиксированы в пространстве и определяют геометрию комплекса и его стереохимию.
При координационном числе 6, возможны три способа расположения шести точек в пространстве, относительно центра координации – то есть атома металла. Это правильный шестиугольник, правильный (или искаженный) октаэдр и центрированная правильная трехгранная призма, изображенные на рисунке 1.



Возможные фиксированные положения лигандов в пространстве
при координационном числе шесть – шестиугольник, призма и октаэдр.
1.Если во внутренней сфере комплексного соединения лигандами являются полярные молекулы аммиака (или различные амины), то такие соединения называются аммиакатами (или аминатами). Связь с центральным ионом-комплексообразователем у этих лигандов осуществляется через азот.
В комплексе молекула NH3 занимает одно координационное место, а число лигандов зависит от центральвого иона. В некоторых аммиакатах оно доходит до 8, напримёр [Ca(NH3)8]Cl2. Молекулы гидроксиламина также занимают одно координационное место, например [Ni(NH20H)e]S04. Молекулы гидразина могут занимать одно и два координационных места: [Pt(NH3)2(N2H4)2]Cl2, [Ni(N2H4)3]S04.
2. Комплексные соединения, содержащие нейтральные молекулы воды как во внутренней сфере (аквасоединения), так и во внешней (кристаллогидраты),- называются гидратами. Например [Fe(H20)e]Cl3, [Cu(H20)JS04 • Н20.
3. Комплексные соединения, в которых центральный ион координирует вокруг себя отрицательно заряженные кислотные остатки, являются ацидокомплексами. Например Кз1Со(М02)в], Na[AgCl2], (NH4)2[Ca(S04)2].
Для растворов комплексных соединений характерно четыре вида равновесий:
а) диссоциация на комплексный и внешнесферный ноны,
б) диссоциация комплексного нона (или замещение лигандов молекулами растворителя),
в) диссоциация лигандов и
г) окислительно- восстановительное равновесие (в случае, когда атом комплексообразователь проявляет переменную -валентность).















