Электролитическаядиссоциация — процесс распада электролита на ионы при его растворении или плавлении. Диссоциация в растворах: Диссоциация на ионы в растворах происходит вследствие взаимодействия растворённого вещества срастворителем.Это взаимодействие носит в значительной мере химический характер. Диссоциация при плавлении: Под действием высоких температур ионы кристаллической решётки начинают совершать колебания, кинетическая энергия повышается, и наступает такой момент (при температуре плавления вещества), когда она превысит энергию взаимодействия ионов. Результатом этого является распад вещества на ионы. Степеньдиссоциации электролитов на ионы зависит от ряда факторов, в основе которых лежит соотношение между силами и характером внутримолекулярного и межмолекулярного взаимодействия растворителя и растворенного вещества, поэтому степень диссоциации зависит: во-первых, от природы растворителя, во-вторых, от природы растворенного вещества и, в-третьих, — от концентрации раствора.Из механизма диссоциации ясно также, что диссоциировать будут вещества, обладающие ионной или полярной связью, поэтому степень диссоциации зависит от природы растворенного вещества, вернее, от типа связи в его молекулах.По характеру диссоциации электролиты можно разделить на кислоты, основания и соли, а по степени диссоциации — на сильные и слабые электролиты. Диссоциациякислот: Кислотами называются электролиты, при диссоциации которых в качестве катионов образуются только катионы водорода. Н3РО4 = Н+ + Н2РО-4(первая ступень); Н2РО-4 = Н+ + НPO4(вторая ступень); НРО2-4 = Н+ PОЗ-4 (третья ступень). Диссоциация многоосновной кислоты протекает главным образом по первой ступени, в меньшей степени по второй и лишь в незначительной степени по третьей. Поэтому в водном растворе, например, фосфорной кислоты наряду с молекулами H3PO4 имеются ионы (в последовательно уменьшающихся количествах) Н2РО2-4, НРО2-4 и РО3-4. Диссоциацияоснований: Основаниями называются электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы. KOH = K+ + OH-; NH4OH = NH+4 + OH- .Основания, растворимые в воде называются щелочами (основания щелочных и щелочноземельных металлов, а также NH4OH) Диссоциациясолей: Соли — это электролиты, которые диссоциируют на катионы металлов (или катионы аммония NH4+) и анионы кислотных остатков. Независимо от состава средние соли диссоциируют нацело, в одну стадию. Например, диссоциацию фосфата натрия и сульфата алюминия можно представить в виде уравнений: Na3PO4 = 3Na+ + PO43–;Al2(SO4)3 = 2Al3+ + 3SO42–.В отличие от средних, кислые соли (в их состав входят гидроанионы) и основные соли (в составе которых есть гидроксокатионы) диссоциируют ступенчато. Например, диссоциация кислой соли — дигидрофосфата натрия:NaH2PO4=Na++H2PO4–;H2PO4=H++HPO42–; HPO42–=H++PO43–
Ионные реакции.
Ионные реакции — реакции между ионами в растворе. Например, реакциюAgNO3 + NaCl = NaNO3 + AgClможно представить в ионном виде (реакция расписывается на ионы, не расписываются осадки, газы, вода, слабые кислоты и основания, а также малорастворимые и нерастворимые соединения) например AgCl нерастворим в воде и на ионы не расписывается:Ag+ + NO3− + Na+ + Cl− = AgCl + Na+ + NO3−Одинаковые ионы сокращаются и получается сокращенное ионное уравнение. Так как взаимодействие произошло между ионами Ag+ и ионами Cl−, то выражение Ag+ + Cl− = AgClи есть ионное уравнение рассматриваемой реакции. Оно проще молекулярного и в то же время отражает сущность происходящей реакции.
Условия необратимости ионной реакции: 1. Если в результате реакции выделяется малодиссоциирующее вещество – вода. Молекулярное уравнение реакции щелочи с кислотой:  Неизменность степеней окисления элементов во всех веществах до и после реакции говорит о том, что реакции обмена не являются окислительно-восстановительными.Полное ионное уравнение реакции:K+ + OH– + H+ + Cl– = K+ + Cl– + H2O.Cокращенное ионное уравнение реакции: H+ + OH– = H2O. Молекулярное уравнение реакции основного оксида с кислотой: CaO + 2HNO3 = Ca(NO3)2 + H2O.Полное ионное уравнение реакции:
Неизменность степеней окисления элементов во всех веществах до и после реакции говорит о том, что реакции обмена не являются окислительно-восстановительными.Полное ионное уравнение реакции:K+ + OH– + H+ + Cl– = K+ + Cl– + H2O.Cокращенное ионное уравнение реакции: H+ + OH– = H2O. Молекулярное уравнение реакции основного оксида с кислотой: CaO + 2HNO3 = Ca(NO3)2 + H2O.Полное ионное уравнение реакции:
 Cокращенное ионное уравнение реакции: CaO + 2H+ = Ca2+ + H2O. Молекулярное уравнение реакции нерастворимого основания с кислотой: 3Mg(OH)2 + 2H3PO4 = Mg3(PO4)2
Cокращенное ионное уравнение реакции: CaO + 2H+ = Ca2+ + H2O. Молекулярное уравнение реакции нерастворимого основания с кислотой: 3Mg(OH)2 + 2H3PO4 = Mg3(PO4)2  + 6H2O. Полное ионное уравнение реакции:
+ 6H2O. Полное ионное уравнение реакции:  В данном случае полное ионное уравнение совпадает с сокращенным ионным уравнением. Молекулярное уравнение реакции амфотерного оксида с кислотой: Al2O3 + 6HCl = 2AlCl3 + 3H2O.Полное ионное уравнение реакции:Al2O3 + 6H+ + 6Cl– = 2Al3+ + 6Cl– + 3H2O. Cокращенное ионное уравнение реакции:Al2O3 + 6H+ = 2Al3+ + 3H2O.
В данном случае полное ионное уравнение совпадает с сокращенным ионным уравнением. Молекулярное уравнение реакции амфотерного оксида с кислотой: Al2O3 + 6HCl = 2AlCl3 + 3H2O.Полное ионное уравнение реакции:Al2O3 + 6H+ + 6Cl– = 2Al3+ + 6Cl– + 3H2O. Cокращенное ионное уравнение реакции:Al2O3 + 6H+ = 2Al3+ + 3H2O.
2. Если в результате реакции выделяется нерастворимое в воде вещество. Молекулярное уравнение реакции растворимой соли со щелочью: CuCl2 + 2KOH = 2KCl + Cu(OH)2  .Полное ионное уравнение реакции: Cu2+ + 2Cl– + 2K+ + 2OH– = 2K+ + 2Cl– + Cu(OH)2
.Полное ионное уравнение реакции: Cu2+ + 2Cl– + 2K+ + 2OH– = 2K+ + 2Cl– + Cu(OH)2  .
.
Cокращенное ионное уравнение реакции: Cu2+ + 2OH– = Cu(OH)2  . М олекулярное уравнение реакции двух растворимых солей: Al2(SO4)3 + 3BaCl2 = 3BaSO4
. М олекулярное уравнение реакции двух растворимых солей: Al2(SO4)3 + 3BaCl2 = 3BaSO4  + 2AlCl3.Полное ионное уравнение реакции:
+ 2AlCl3.Полное ионное уравнение реакции:  Cокращенное ионное уравнение реакции:
Cокращенное ионное уравнение реакции: 
Молекулярное уравнение реакции нерастворимого основания с кислотой: Fe(OH)3 + H3PO4 = FePO4  + 3H2O. Полное ионное уравнение реакции:
+ 3H2O. Полное ионное уравнение реакции:  В данном случае полное ионное уравнение реакции совпадает с сокращенным. Эта реакция протекает до конца, о чем свидетельствуют сразу два факта: образование вещества, нерастворимого в воде, и выделение воды.
В данном случае полное ионное уравнение реакции совпадает с сокращенным. Эта реакция протекает до конца, о чем свидетельствуют сразу два факта: образование вещества, нерастворимого в воде, и выделение воды.
3. Если в результате реакции выделяется газообразное вещество. Молекулярное уравнение реакции растворимой соли (сульфида) с кислотой: K2S + 2HCl = 2KCl + H2S  .Полное ионное уравнение реакции: 2K+ + S2– + 2H+ + 2Cl– = 2K+ + 2Cl– + H2S
.Полное ионное уравнение реакции: 2K+ + S2– + 2H+ + 2Cl– = 2K+ + 2Cl– + H2S  . Cокращенное ионное уравнение реакции: S2– + 2H+ = H2S
. Cокращенное ионное уравнение реакции: S2– + 2H+ = H2S  . М олекулярное уравнение реакции растворимой соли (карбоната) с кислотой: Na2CO3 + 2HNO3 = 2NaNO3 + H2O + CO2
. М олекулярное уравнение реакции растворимой соли (карбоната) с кислотой: Na2CO3 + 2HNO3 = 2NaNO3 + H2O + CO2  Полное ионное уравнение реакции:
Полное ионное уравнение реакции:  Cокращенное ионное уравнение реакции:
Cокращенное ионное уравнение реакции:  О протекании данной реакции до конца свидетельствуют два признака: выделение воды и газа – оксида углерода(IV). Молекулярное уравнение реакции нерастворимой соли (карбоната) с кислотой: 3СaCO3 + 2H3РO4 = Са3(PO4)2
О протекании данной реакции до конца свидетельствуют два признака: выделение воды и газа – оксида углерода(IV). Молекулярное уравнение реакции нерастворимой соли (карбоната) с кислотой: 3СaCO3 + 2H3РO4 = Са3(PO4)2  + 3H2O + 3CO2
+ 3H2O + 3CO2  Полное ионное уравнение реакции:
Полное ионное уравнение реакции: 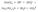 В данном случае полное ионное уравнение реакции совпадает с сокращенным уравнением. Эта реакция протекает до конца, о чем свидетельствуют сразу три признака: выделение газа, образование осадка и выделение воды.
В данном случае полное ионное уравнение реакции совпадает с сокращенным уравнением. Эта реакция протекает до конца, о чем свидетельствуют сразу три признака: выделение газа, образование осадка и выделение воды.



 Неизменность степеней окисления элементов во всех веществах до и после реакции говорит о том, что реакции обмена не являются окислительно-восстановительными.Полное ионное уравнение реакции:K+ + OH– + H+ + Cl– = K+ + Cl– + H2O.Cокращенное ионное уравнение реакции: H+ + OH– = H2O. Молекулярное уравнение реакции основного оксида с кислотой: CaO + 2HNO3 = Ca(NO3)2 + H2O.Полное ионное уравнение реакции:
Неизменность степеней окисления элементов во всех веществах до и после реакции говорит о том, что реакции обмена не являются окислительно-восстановительными.Полное ионное уравнение реакции:K+ + OH– + H+ + Cl– = K+ + Cl– + H2O.Cокращенное ионное уравнение реакции: H+ + OH– = H2O. Молекулярное уравнение реакции основного оксида с кислотой: CaO + 2HNO3 = Ca(NO3)2 + H2O.Полное ионное уравнение реакции: Cокращенное ионное уравнение реакции: CaO + 2H+ = Ca2+ + H2O. Молекулярное уравнение реакции нерастворимого основания с кислотой: 3Mg(OH)2 + 2H3PO4 = Mg3(PO4)2
Cокращенное ионное уравнение реакции: CaO + 2H+ = Ca2+ + H2O. Молекулярное уравнение реакции нерастворимого основания с кислотой: 3Mg(OH)2 + 2H3PO4 = Mg3(PO4)2  + 6H2O. Полное ионное уравнение реакции:
+ 6H2O. Полное ионное уравнение реакции:  В данном случае полное ионное уравнение совпадает с сокращенным ионным уравнением. Молекулярное уравнение реакции амфотерного оксида с кислотой: Al2O3 + 6HCl = 2AlCl3 + 3H2O.Полное ионное уравнение реакции:Al2O3 + 6H+ + 6Cl– = 2Al3+ + 6Cl– + 3H2O. Cокращенное ионное уравнение реакции:Al2O3 + 6H+ = 2Al3+ + 3H2O.
В данном случае полное ионное уравнение совпадает с сокращенным ионным уравнением. Молекулярное уравнение реакции амфотерного оксида с кислотой: Al2O3 + 6HCl = 2AlCl3 + 3H2O.Полное ионное уравнение реакции:Al2O3 + 6H+ + 6Cl– = 2Al3+ + 6Cl– + 3H2O. Cокращенное ионное уравнение реакции:Al2O3 + 6H+ = 2Al3+ + 3H2O. Cокращенное ионное уравнение реакции:
Cокращенное ионное уравнение реакции: 
 В данном случае полное ионное уравнение реакции совпадает с сокращенным. Эта реакция протекает до конца, о чем свидетельствуют сразу два факта: образование вещества, нерастворимого в воде, и выделение воды.
В данном случае полное ионное уравнение реакции совпадает с сокращенным. Эта реакция протекает до конца, о чем свидетельствуют сразу два факта: образование вещества, нерастворимого в воде, и выделение воды. .Полное ионное уравнение реакции: 2K+ + S2– + 2H+ + 2Cl– = 2K+ + 2Cl– + H2S
.Полное ионное уравнение реакции: 2K+ + S2– + 2H+ + 2Cl– = 2K+ + 2Cl– + H2S  Cокращенное ионное уравнение реакции:
Cокращенное ионное уравнение реакции:  О протекании данной реакции до конца свидетельствуют два признака: выделение воды и газа – оксида углерода(IV). Молекулярное уравнение реакции нерастворимой соли (карбоната) с кислотой: 3СaCO3 + 2H3РO4 = Са3(PO4)2
О протекании данной реакции до конца свидетельствуют два признака: выделение воды и газа – оксида углерода(IV). Молекулярное уравнение реакции нерастворимой соли (карбоната) с кислотой: 3СaCO3 + 2H3РO4 = Са3(PO4)2 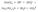 В данном случае полное ионное уравнение реакции совпадает с сокращенным уравнением. Эта реакция протекает до конца, о чем свидетельствуют сразу три признака: выделение газа, образование осадка и выделение воды.
В данном случае полное ионное уравнение реакции совпадает с сокращенным уравнением. Эта реакция протекает до конца, о чем свидетельствуют сразу три признака: выделение газа, образование осадка и выделение воды.


