Реакция протекает так же, как и при взаимодействии с азотистой кислотой алифатических первичных аминов - выделяется азот, а аминогруппа замещается на гидроксильную группу:
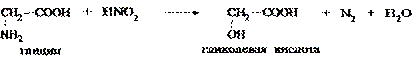
Таким образом можно установить структурное родство аминокислот с соответствующими оксикислотами. По объёму выделившегося азота определяют количество α-аминокислоты, вступившей в реакцию (метод Ван-Слайка).
Взаимодействие с альдегидами
α-Аминокислоты, подобно первичным аминам, реагируют с альдегидами, образуя замещенные имины (основания Шиффа). Реакция протекает через стадию образования карбиноламинов.

При взаимодействии α-аминокислот с формальдегидом образуются относительно устойчивые карбиноламины - N-метилольные производные, свободная карбоксильная группа которых может быть оттитрована щелочью.
Формальдегид, взятый в избытке, способствует отщеплению протона от NH3+ группы биполярного иона и легко соединяется со свободной (непротонированной) аминогруппой, образуя устойчивое метилольное производное.

Титрование аминокислоты в избытке формальдегида (формольное титрование) представляет собой аналитический метод (метод Серенсена), при помощи которого прослеживается, в частности, образование свободных аминокислот в процессе гидролиза белков.
Взаимодейстивие с динитрофторбензолом (ДНФБ)
Важной реакцией α-аминогруппы является её реакция с
2,4-динитрофторбензолом (ДНФБ) в слабощелочном растворе, которую впервые использовал Фредерик Сенгер для количественного введения метки в аминогруппы аминокислот и пептидов. Эта реакция протекает по механизму нуклеофильного замещения.

Продукт реакции окрашен в интенсивно желтый цвет. Эта реакция представляет исключительную ценность для идентификации N-концевых аминокислот полипептидных цепей.
Все вышеперечисленные реакции аминогруппы аминокислот можно представить следующей схемой:

Качественные реакции. Особенность химии аминокислот и белков заключается в использовании многочисленных качественных (цветных) реакций, составлявших ранее основу химического анализа. В настоящее время, когда исследования проводятся с помощью физико-химических методов, многие качественные реакции продолжают применять для обнаружения α-аминокислот, например, в хроматографическом анализе.
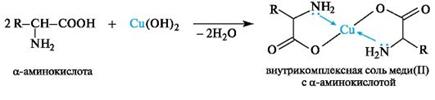
Хелатообразование. С катионами тяжелых металлов α-аминокислоты как бифункциональные соединения образуют внутрикомплексные соли, например, со свежеприготовленным гидроксидом меди (II) в мягких условиях получаются хорошо кристаллизующиеся хелатные соли меди (II) синего цвета (один из неспецифических способов обнаружения α-аминокислот).
Нингидринная реакция. Общая качественная реакция α-аминокислот - реакция с нингидрином. Продукт реакции имеет синефиолетовый цвет, что используется для визуального обнаружения аминокислот на хроматограммах (на бумаге, в тонком слое), а также для спектрофотометрического определения на аминокислотных анализаторах (продукт поглощает свет в области 550-570 нм).

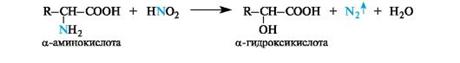
Дезаминирование. В лабораторных условиях эта реакция осуществляется при действии азотистой кислоты на α-аминокислоты. При этом образуется соответствующая α-гидроксикислота и выделяется газообразный азот, по объему которого судят о количестве вступившей в реакцию аминокислоты (метод Ван-Слайка).
Ксантопротеиновая реакция. Эта реакция используется для обнаружения ароматических и гетероциклических аминокислот - фенилаланина, тирозина, гистидина, триптофана. Например, при действии концентрированной азотной кислоты на тирозин образуется нитропроизводное, окрашенное в желтый цвет. В щелочной среде окраска становится оранжевой в связи с ионизацией фенольной гидроксильной группы и увеличением вклада аниона в сопряжение.

Биуретовая реакция. Служит для обнаружения пептидных связей. В биуретовую реакцию вступают пептиды, содержащие не менее двух пептидных связей. Пептиды и белки щелочном растворе с сульфатом меди образуют комплексы, окрашенные в сине-фиолетовый цвет.
Существует также ряд частных реакций, позволяющих обнаруживать отдельные аминокислоты.
• Триптофан обнаруживают при помощи реакции с п-диметиламино-бензальдегидом в среде серной кислоты по появляющемуся красно-фиолетовому окрашиванию (реакция Эрлиха). Эта реакция используется для количественного анализа триптофана в продуктах расщепления белков.
• Цистеин обнаруживают с помощью нескольких качественных реакций, основанных на реакционной способности содержащейся в нем меркаптогруппы. Например, при нагревании раствора белка с ацетатом свинца (СНзСОО)2РЬ в щелочной среде образуется черный осадок сульфида свинца Pb S, что указывает на присутствие в белках цистеина.
Биологически важные реакции аминокислот. Образование аминокислот в результате восстановительного аминирования и реакции трансаминирования















