Величина падения напряжения в электролите существенно зависит от конструкции электролизера, его геометрических размеров, удельной электропроводимости электролита. Омические составляющие напряжения на электролизере рассчитывают по закону Ома [5].
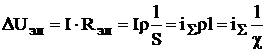 (10)
(10)
где ρ – удельное сопротивление электролита, Ом*м;
χ – удельная электропроводность электролита, См/м;
l – расстояние между катодом и анодом, м;
S – площадь проходного сечения электролита, м2;
iΣ–средняя плотность тока, А/м2.
Расстояние между катодом и анодом рассчитали следующим образом. Ширина ванны составляет 730 мм. Расстояние от края ванны до анодной штанги 80 мм. Следовательно, расстояние между катодом и анодом можно принять равным 300 мм.
Для расчета падения напряжения в электролите использовали величину средней плотности тока, которая учитывает прохождение тока между электродами разной площади.
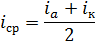
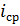 =
= 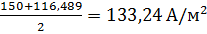
Для расчета χ необходимо определить эквивалентные электропроводности при суммарной эквивалентной концентрации электролита.
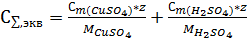 (12)
(12)
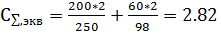 моль-экв/л
моль-экв/л
3.2 Расчет удельной электропроводности для 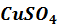
По справочным данным составим таблицу 4.
Таблица 4 – Эквивалентная электропроводность сульфата меди [6]
| Сэ,моль-экв/л
| λ18,См/м2·моль
|
| 0,1
| 0,004386
|
| 0,5
| 0,0031
|
|
| 0,002583
|
|
| 0,002015
|
Построим график зависимостиСэ(CuSO4)-λ(рисунок 1).
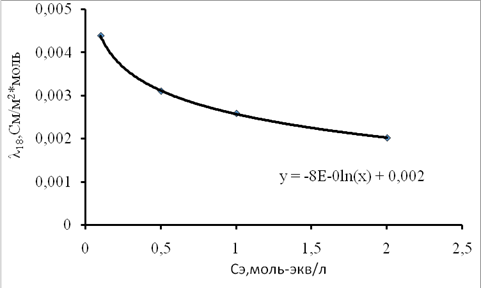
Рисунок 3 – Зависимость эквивалентной электропроводности сульфата меди от концентрации
По логарифмическому уравнению найдем эквивалентную электропроводность при заданной концентрации (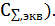
λ = (-8*10^ (-4) *ln (2,8244) + 0,0026) *10-4=0,0017 См*м2/моль
Рассчитаем удельную электропроводность при температуре 18оС:
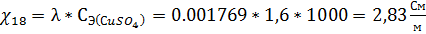 (12)
(12)
Пересчитаем 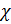 при рабочей температуре электролита в 23оС:
при рабочей температуре электролита в 23оС:
α, при молярной концентрации 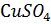 =1,6 моль/л, равен 0,021.
=1,6 моль/л, равен 0,021.
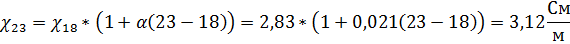
3.3 Расчет удельной электропроводности для 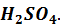
Методика расчета электропроводности для серной кислоты состоит из следующих последовательно идущих операций
1. Из справочника [7] необходимо взять значения плотностей растворов серной кислоты и соответствующие им процентные концентрации. Эти данные необходимы для пересчета процентной концентрации в эквивалентную.
2. Также из справочника [6] возьмём значения удельной электропроводности растворов серной кислоты и соответствующие им процентные концентрации.
3. Исходя из того, что значения плотностей и электропроводностей в справочной литературе даны при разных концентрациях, строим зависимость ρH2SO4 – ω%. (Рисунок 2),для определения плотностей растворов серной кислоты при концентрации соответствующей справочным значениям удельной электропроводности и заносим их в таблицу 6.
4. Затем выполняем пересчет процентной концентрации в эквивалентную и также заносим их в таблицу 6.
5. По данным из таблицы 6 строим зависимость СЭ- λ 
6. По линии тренда зависимости СЭ- λ  определяем удельную электропроводность раствора серной кислоты при концентрации 2,82 моль-экв./л.
определяем удельную электропроводность раствора серной кислоты при концентрации 2,82 моль-экв./л.
Таблица 5 – Плотность серной кислоты [7]
| P, кг/м3
| ω, %
|
|
| 6,956
|
|
| 7,704
|
|
| 8,415
|
|
| 9,129
|
|
| 9,843
|
|
| 10,56
|
|
| 11,26
|
|
| 11,96
|
|
| 12,66
|
|
| 13,36
|
|
| 14,04
|
|
| 14,73
|
|
| 15,41
|
|
| 16,08
|
|
| 16,76
|
|
| 17,43
|
|
| 18,09
|
|
| 18,76
|
|
| 19,42
|
|
| 23,93
|
|
| 24,58
|
|
| 25,21
|
|
| 25,84
|
|
| 26,47
|
|
| 27,1
|
|
| 27,72
|
|
| 28,83
|
|
| 29,57
|
|
| 30,18
|
Пример расчета плотности электролита для концентрации соответствующей концентрации при которой дана электропроводность.
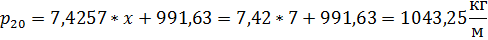
Далее произведем пересчет плотности при 20оС в плотность при 25оС по следующему уравнению
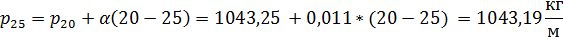
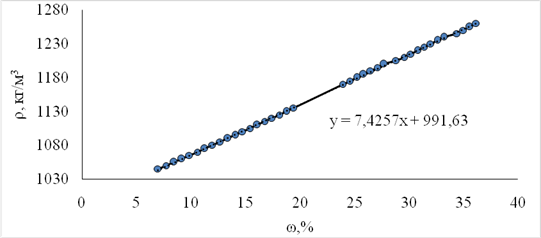
Рисунок 4 – Зависимость плотности серной кислоты от концентрации
По справочным и расчетный данным составляем таблицу 6.
Таблица 6 – Эквивалентная электропроводность серной кислоты [6]
| ω, %
| p, кг/м3 при Т=250С
| p, кг/м3 при Т=200С
| Сэ, моль-экв/л
| λ, См*м2/моль
|
|
| 1043,196
| 1043,2725
| 0,745178929
| 0,02069
|
|
| 1065,61
| 1065,6894
| 1,087413265
| 0,01964
|
|
| 1095,496
| 1095,579
| 1,565072857
| 0,018
|
|
| 1132,854
| 1132,9357
| 2,196455255
| 0,0156
|
|
| 1177,683
| 1177,7667
| 3,004432398
| 0,01314
|
|
| 1207,569
| 1207,6535
| 3,573579745
| 0,01135
|
|
| 1244,926
| 1245,012
| 4,319321837
| 0,009365
|
|
| 1282,284
| 1282,3713
| 5,103183827
| 0,007585
|
По данным из таблицы 6 строим зависимость эквивалентной электропроводности серной кислоты от концентрации (рисунок 3). По уравнению линии тренда найдем эквивалентную электропроводность при суммарной эквивалентной концентрации электролита:
λ = -0,0031*(x)+0,0227=-0,0031*2,8244+0,0176= 0,0189 См*м2/моль
Рассчитаем удельную электропроводность при температуре 25оС:
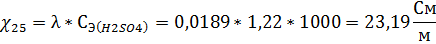
Пересчитаем 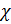 при рабочей температуре электролита в 23оС:
при рабочей температуре электролита в 23оС:
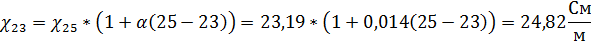
Найдем 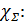
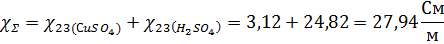
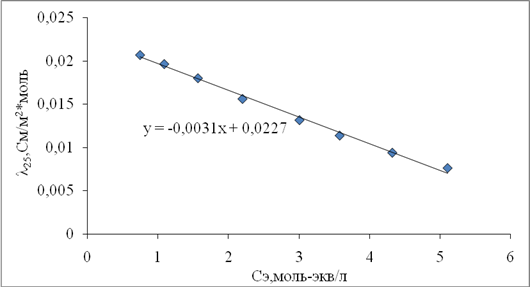
Рисунок 5 – Зависимость эквивалентной электропроводности серной кислоты от концентрации
Рассчитаем падение напряжения в электролите ΔUэл:
ΔUэл= 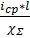 (14)
(14)
l- расстояние между катодом и анодом равное 300 мм.
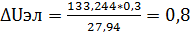 В
В
Падение напряжения в контактах принимают равным 10-15 % от рассчитанного общего напряжения.
Рассчитаем общее падение напряжения в теле электрода:
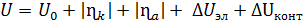
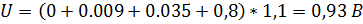
Выбор источника тока
Выбором источника тока нужно учесть падение напряжения в проводящих проводах от выпрямителя до гальванической ванны. Его принимают равным 15% напряжения на ванне. С учетом этой составляющей U= 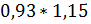 = 1,06В.
= 1,06В.
Следовательно, выпрямительный агрегат должен поддерживать ток силой 182,65А при напряжении 1,06В. По результатам расчета выбираем ближайший по техническим характеристикам выпрямительный агрегат В-ТПЕ-200-12-01УХЛ4; номинальная сила тока 200А; номинальное напряжение 12В.
Заключение
Медь по праву можно назвать незаменимым металлом в гальваническом производстве. Покрытия из меди применяют во многих отраслях промышленности как в качестве подслоя для нанесения других металлов, так и в качестве самостоятельного покрытия в производстве печатных плат. Толстые медные покрытия используют в гальванопластике для производства металлических копий.
В расчетной части были найдены, электропроводность электролита, величины анодного и катодного перенапряжений, а также габаритные размеры ванны. Полученные данные были использованы для расчета электрического баланса ванны гальванического меднения.
Для электроосаждения медных покрытий была выбрана ванна с габаритными размерами 1000 х 1000 х 730 мм. На основании результатов расчета электрического баланса установлено, что для нормальной работы гальванической ванны необходим выпрямительный агрегат марки В-ТПЕ-200-12-01УХЛ4; номинальная сила тока 200А; номинальное напряжение 12 В.
Библиографический список
1. Дасоян, М.А. Технология электрохимических покрытий / М.А. Дасоян, И.Я. Пальмская, Е.В. Сахарова. – Л.: Машиностроение, 1989. – 391 с.
2. Федотьев, Н.П. Прикладная электрохимия/Н.П. Федотьев, А.Ф. Алабышев, А.Л. Рогинян. – СПб.: Госхимиздат, 1962. – 641 с.
3. Томилов, А.П. Прикладная электрохимия / А.П.Томилов, Р.И. Агладзе, Н.Т. Гофман.– М.: Химия 1984. – 517 с.
4. Кудрявцев, Н.Т. Электролитические покрытия металлами/Н.Т. Кудрявцев. – М.: Химия,1979. –352 с.
5. Рудой, В. М. Методы исследования кинетики электродных процессов: учебно- методическое пособие / В. М. Рудой, Т. Н. Останина, И. Б. Мурашова, А. Б. Даринцева.– Екатеринбург.: Изд – во Урал. Ун - та, 2013. - 112 с.
6. Справочник по электрохимии / Под ред. Сухотина А.М. – М. - Л.: Химия, 1981. - 488 с.
7. Справочник химика. Т.З. /Под ред. Б.Н Никольского. – 2-е издание. - М.: Химия, 1964. - 1000 с.



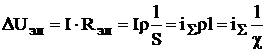 (10)
(10)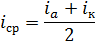
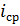 =
= 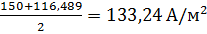
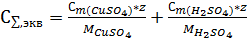 (12)
(12)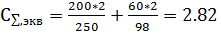 моль-экв/л
моль-экв/л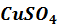

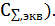
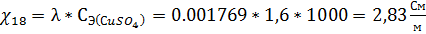 (12)
(12)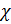 при рабочей температуре электролита в 23оС:
при рабочей температуре электролита в 23оС: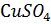 =1,6 моль/л, равен 0,021.
=1,6 моль/л, равен 0,021.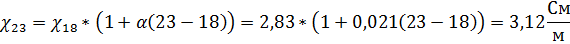
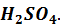

 определяем удельную электропроводность раствора серной кислоты при концентрации 2,82 моль-экв./л.
определяем удельную электропроводность раствора серной кислоты при концентрации 2,82 моль-экв./л.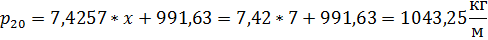
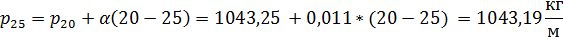

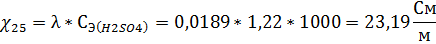
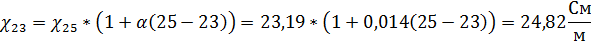
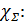
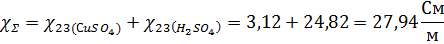

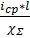 (14)
(14)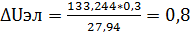 В
В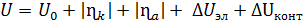
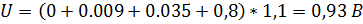
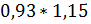 = 1,06В.
= 1,06В.


