

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...
Топ:
Основы обеспечения единства измерений: Обеспечение единства измерений - деятельность метрологических служб, направленная на достижение...
Методика измерений сопротивления растеканию тока анодного заземления: Анодный заземлитель (анод) – проводник, погруженный в электролитическую среду (грунт, раствор электролита) и подключенный к положительному...
Эволюция кровеносной системы позвоночных животных: Биологическая эволюция – необратимый процесс исторического развития живой природы...
Интересное:
Принципы управления денежными потоками: одним из методов контроля за состоянием денежной наличности является...
Национальное богатство страны и его составляющие: для оценки элементов национального богатства используются...
Мероприятия для защиты от морозного пучения грунтов: Инженерная защита от морозного (криогенного) пучения грунтов необходима для легких малоэтажных зданий и других сооружений...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
(практическое задание №3)
Цель работы: расчет равновесных составов и окислительно-восстановительных свойств газовых атмосфер при высоких температурах.
Основными газовыми реакциями в металлургических процессах являются реакции горения СО и Н2.
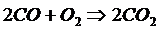 (3.1)
(3.1)
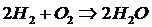 (3.2)
(3.2)
Термодинамические потенциалы этих реакций имеют вид:
 (3.3)
(3.3)
 (3.4)
(3.4)
Для реакций (3.1, 3.2) константы равновесия определяются по формулам.
 (3.5)
(3.5)
 (3.6)
(3.6)
Влияние давления на равновесие определяем на основе парциальных Pi компонентов и числа молей:
 (3.7)
(3.7)
Для определения числа молей можно использовать степень диссоциации a (отношение числа распавшихся молей к исходному числу). Допустим, что 1 моль СО2 (реакция 1) диссоциирует на a молей СО. Тогда образуется 0,5a молей О 2 и остаток нераспавшихся молей CO2 равен 1–a. Суммарное число молей может быть выражено для реакций (3.1) и (3.2) следующим образом:
 (3.8)
(3.8)
Тогда из (3.7) можно определить парциальные давления каждой фазы
 (3.9)
(3.9)
 (3.10)
(3.10)
 (3.11)
(3.11)
После подстановки (3.9…3.11) в уравнение (3.5) получим, что константа равновесия определяется как
 (3.12)
(3.12)
При температурах Т £ 2273 К считается, что для вышеописанных реакций a << 1. В этом случае
 (3.13)
(3.13)
Для оценки окислительно-восстановительных свойств газовой фазы используют химический потенциал киалорода, определяемый как
 (3.14)
(3.14)
С учетом (3.5) можно получить П 0, выраженное через парциальные давления  и
и  :
:
 (3.15)
(3.15)
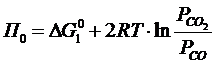 (3.16)
(3.16)
где DG1 – потенциал (3.3); R – газовая постоянная; П 0 – химический потенциал кислорода.
Аналогично запишем для реакции (3.2):
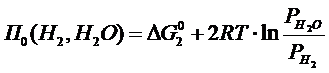 (3.17)
(3.17)
Если исходный фазовый состав газовой фазы отличается от равновесного, то направление превращений определяют с помощью уравнения изотермы реакции:
 (3.18)
(3.18)
где 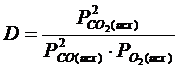 .
.
Если D G < 0, то превращения должны происходить слева направо.
|
|
Если D G > 0, то превращения происходят в противоположном направлении. При D G = 0 наступает равновесие.
Примеры расчета
(практическое задание №3)
Постановка задачи 1. Определить направление реакции взаимодействия (3.1) при Т = 2273 К при исходном составе газовой фазы 70 % СО2, 20 % СО и 10 % О2. Найти константу равновесия при Р = 1.
Решение.
По уравнению (3.18) определили D G, учитывая (3.3)
 (3.19)
(3.19)

Так как D G < 0, то реакция идет в сторону образования СО 2 с горением СО.
Константа равновесия определятся как
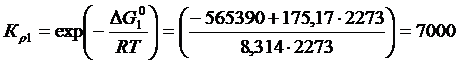
Постановка задачи 2. Определить равновесный состав газовой фазы, образующейся в результате диссоциации СО 2 при Т = 2273 К и Р = 1. Определить кислородный потенциал газовой фазы.
Решение.
Реакция имеет вид (3.1). Задача сводится к определению парциальных давлений (3.9…3.11). Однако предварительно вычислив a (степень диссоциации), воспользовавшись (3.13) и значением константы равновесия, вычисленной из предыдущей задачи, получим:

Подставляя a в(3.9…3.11), получим следующие парциальные давления:
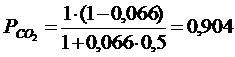


Таким образом, состав газовой фазы будет следующим:
90,4 % СО 2 + 6,4 % СО +3,2 % О 2
Кислородный потенциал газовой фазы рассчитываем с помощью (3.14)

|
|
|

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни...

Состав сооружений: решетки и песколовки: Решетки – это первое устройство в схеме очистных сооружений. Они представляют...

Типы оградительных сооружений в морском порту: По расположению оградительных сооружений в плане различают волноломы, обе оконечности...

Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!