Лекарственная форма - придаваемое лекарственному препарату состояние, соответствующее пути его введения и способу применения и обеспечивающее достижение необходимого лечебного эффекта. Все лекарственные формы по агрегатному состоянию делят на 4 группы: твердые, жидкие, мягкие, газообразные.
Аэрозолями называются дисперсные системы с газообразной дисперсионной средой и твердой или жидкой дисперсной фазой. Лекарственные аэрозоли - это искусственные аэродисперсные системы, в которых высокодисперсной фазой являются лекарственные вещества в виде той или иной лекарственной формы, а дисперсионной средой - сжатый или сжиженный газ - пропеллент.Аэрозоли как форма применения различных лекарственных веществ имеет много достоинств. Основное из них заключается в высокой дисперсности и легкой подвижности частиц дисперсной фазы - факторов, в значительной степени повышающих фармакологическую активность лекарственных веществ. Размер частичек дисперсной фазы варьирует в пределах 0,5-5 мкм. При вдыхании аэрозоля лекарственные вещества не претерпевают тех изменений, которые имеют место при приеме лекарственных форм внутрь, т. е. отсутствуют факторы воздействия желудочного и кишечного сока с их активными ферментами. Аэрозоли можно получить и с помощью химических реакций, протекающих в газовой фазе. По агрегатному состоянию частиц аэрозоли классифицируют на туманы (ж/г) – дисперсная система состоит из капелек жидкости, дымы (т/г) – аэрозоли с твердыми частицами конденсационного происхождения, пыли (т/г) – твердые частицы, образованные путем диспергирования. Возможны системы смешанного типа, когда на твердых частицах конденсируется влага. Так возникает «смог» – туман, образовавшийся на частицах дыма.
Суспензии – очень распространенные микрогетерогенные системы с жидкой средой твердой и твердой дисперсной фазой с размерами частиц выше, чем в коллоидных системах, т.н. в диапазоне 10–6 – 10–4 м. Наиболее грубодисперсные системы называют взвесями. К ним относятся глинистые, цементные и известковые «растворы», масляные краски. Отличаясь от лиофобных коллоидов в основном только более низкой степенью дисперсности, суспензии, в принципе, могут быть получены как конденсационными, так и диспергационными методами. Благодаря низкой степени дисперсности в суспензиях слабо проявляются или отсутствует такое молекулярно-кинетическое свойство, как броуновское движение, а значит и диффузия. Осмотическое давление, в суспензиях практически не обнаруживается, так как частичная концентрация в них еще меньше, чем в лоифобных коллоидах. Вязкость разбавленных суспензий мало отличается от вязкости дисперсионной среды. Эмульсии – система, состоящая из двух жидких фаз, одна из которых диспергирована в виде капелек в другой. Жидкость, раздробленная на капельки, называется дисперсной фазой, а жидкость, заполняющая объем между капельками,- дисперсионной средой. Для существования устойчивой эмульсии необходимо, чтобы жидкости, образующие эмульсию, была практически взаимно нерастворимы или обладали достаточно малой растворимостью. Размер частиц дисперсной фазы эмульсий колеблется в пределах от 10–7 до 10–5м, и поэтому их можно отнести к микрогетерогенным системам. Характерной чертой эмульсий является то, что в зависимости от условий возникновения любая из двух жидкостей, образующих дисперсионную систему, может оказаться как дисперсной фазой, так и дисперсионной средой. Наиболее частый случай – эмульсия воды (В) и нерастворимой в ней органической жидкости (например масло, бензол, хлороформ), которую условно называют маслом (М). Возможны два типа таких эмульсий: эмульсии в которых дисперсионной средой является масло, и эмульсии с водой дисперсной фазой. Первый тип эмульсий называют эмульсией масла в воде (сокращенно М/В) или эмульсиями первого рода (прямые). Второй тип – эмульсии воды в масле (В/М) или эмульсии второго рода (обратные).
БЛОК
Билет 31
Органические соединения, органические вещества — класс химических соединений, в состав которых входит углерод (за исключением карбидов, угольной кислоты, карбонатов, оксидов углерода и цианидов). Органические соединения, кроме углерода, чаще всего содержат элементы водород, кислород, азот, значительно реже — серу, фосфор, галогены и некоторые металлы (порознь или в различных комбинациях)
Функциональная группа — это совокупность атомов, определяющая характерные химические свойства целого класса веществ.
Иногда к понятию функциональной группы относят также понятие радикал (метил, этил, пропил и т. д.). Однако хотя это и близкие понятия, но отличительным свойством функциональной группы является наличие одинаковых химических свойств, характерных для всего класса веществ, имеющих такую группу в своей структуре. С этой точки зрения алкильные радикалы такими свойствами не обладают.
По типу функциональных групп органические соединения делят на следующие классы (R-предельный углеводородный радикал):
| Функциональна группа
| Класс соединений
| Общая формула
|
| Отсутствует
| Углеводороды
| R–H
|
| Галоген –F, –Cl, –Br, –I
| Галогеноводороды
| R–Hal
|
| Гидроксильная –OH
| Спирты
| R–OH
|
| фенолы
| Ar–OH (Ar=C6H5C6H5-)
|
| Алкоксильная –OR
| Простые эфиры
| R–O–R'
|
| Амино –NH2–NH2, –NH–, =N0
| Амины
| R–NH2,R2NH,R3NR–NH2,R2NH,R3N
|
| Нитро –NO2–NO2
| Нитросоединения
| R–NO2R–NO2
|
| Карбонильная >C=O
| Альдегиды
| 
|
| Кетоны
|
Карбоксильная  (-COOH) (-COOH)
| Карбоновые кислоты
|

|
Алкоксикарбонильная  (-COOR) (-COOR)
| Сложные эфиры
|

|
Карбоксамидная  (-CONH2CONH2) (-CONH2CONH2)
| Амиды карбоновых кислот
|

|
| Тиольная –SH
| Тиолы
| –RSH
|
| Сульфо –SO3H–SO3H
| Сульфоновые кислоты
| –RSO3H
|
Билет 32
СПИРТЫ (алкоголи) – класс органических соединений, содержащих одну или несколько группировок С–ОН, при этом гидроксильная группа ОН связана с алифатическим атомом углерода (соединения, у которых атом углерода в группировке С–ОН входит в состав ароматического ядра, называются фенолами)
Классификация спиртов разнообразна и зависит от того, какой признак строения взят за основу.
1. В зависимости от количества гидроксильных групп в молекуле спирты делят на:
а) одноатомные (содержат одну гидроксильную ОН-группу), например, метанол СН3ОН, этанол С2Н5ОН, пропанол С3Н7ОН
б) многоатомные (две и более гидроксильных групп), например, этиленгликоль
HO–СH2–CH2–OH, глицерин HO–СH2–СН(ОН)–CH2–OH, пентаэритрит С(СН2ОН)4.
Соединения, в которых у одного атома углерода  есть две гидроксильных группы, в большинстве случаев нестабильны и легко превращаются в альдегиды, отщепляя при этом воду: RCH(OH)2 ® RCH=O + H2O
есть две гидроксильных группы, в большинстве случаев нестабильны и легко превращаются в альдегиды, отщепляя при этом воду: RCH(OH)2 ® RCH=O + H2O
Спирты, содержащие три группы ОН у одного атома углерода  , не существуют.
, не существуют.
2. По типу атома углерода, с которым связана группа ОН, спирты делят на:
а) первичные, у которых ОН-группа связана с первичным атомом углерода. Первичным называют атом углерода (выделен красным цветом), связанный всего с одним углеродным атомом. Примеры первичных спиртов – этанол СH3– C H2–OH, пропанол СH3–CH2– C H2–OH.
б) вторичные, у которых ОН-группа связана с вторичным атомом углерода. Вторичный атом углерода (выделен синим цветом) связан одновременно с двумя атомами углерода, например, вторичный пропанол, вторичный бутанол (рис. 1).

Рис. 1. СТРОЕНИЕ ВТОРИЧНЫХ СПИРТОВ
в) третичные, у которых ОН-группа связана с третичным атомом углерода. Третичный углеродный атом (выделен зеленым цветом) связан одновременно с тремя соседними атомами углерода, например, третичный бутанол и пентанол (рис. 2).
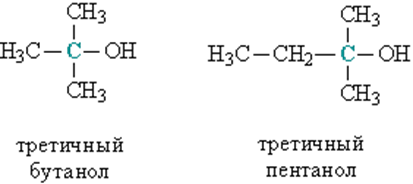
Рис. 2. СТРОЕНИЕ ТРЕТИЧНЫХ СПИРТОВ
В соответствии с типом углеродного атома присоединенную к нему спиртовую группу также называют первичной, вторичной или третичной.
У многоатомных спиртов, содержащих две или более ОН-групп, могут присутствовать одновременно как первичные, так и вторичные НО-группы, например, в глицерине или ксилите (рис. 3).

Рис. 3. СОЧЕТАНИЕ В СТРУКТУРЕ МНОГОАТОМНЫХ СПИРТОВ ПЕРВИЧНЫХ И ВТОРИЧНЫХ ОН-ГРУПП.
3. По строению органических групп, связанных ОН-группой, спирты подразделяют на предельные (метанол, этанол, пропанол), непредельные, например, аллиловый спирт СН2=СН–СН2–ОН, ароматические (например, бензиловый спирт С6Н5СН2ОН), содержащие в составе группы R ароматическую группу.
Непредельные спирты, у которых ОН-группа «примыкает» к двойной связи, т.е. связана с атомом углерода, участвующим одновременно в образовании двойной связи (например, виниловый спирт СН2=СН–ОН), крайне нестабильны и сразу же изомеризуются (см.ИЗОМЕРИЗАЦИЯ) в альдегиды или кетоны:
CH2=CH–OH ® CH3–CH=O
Номенклатура спиртов. Для распространенных спиртов, имеющих простое строение, используют упрощенную номенклатуру: название органической группы преобразуют в прилагательное (с помощью суффикса и окончания «овый») и добавляют слово «спирт»:
| СН3ОН
| метиловый спирт
|
| С2Н5ОН
| этиловый спирт
|
| (Н3С)2СНОН
| изопропиловый спирт
|
| С4Н9ОН
| бутиловый спирт
|
В том случае, когда строение органической группы более сложное, используют общие для всей органической химии правила. Названия, составленные по таким правилам, называют систематическими. В соответствии с этими правилами, углеводородную цепь нумеруют с того конца, к которому ближе расположена ОН-группа. Далее используют эту нумерацию, чтобы указать положение различных заместителей вдоль основной цепи, в конце названия добавляют суффикс «ол» и цифру, указывающую положение ОН-группы (рис. 4):

СИСТЕМАТИЧЕСКИЕ НАЗВАНИЯ СПИРТОВ. Функциональные (ОН) и замещающие (СН3) группы, а также соответствующие им цифровые индексы выделены различающимися цветами.
Систематические названия простейших спиртов составляют по тем же правилам: метанол, этанол, бутанол. Для некоторых спиртов сохранились тривиальные (упрощенные) названия, сложившиеся исторически: пропаргиловый спирт НСєС–СН2–ОН, глицерин HO–СH2–СН(ОН)–CH2–OH, пентаэритрит С(СН2ОН)4, фенетиловый спирт С6Н5–CH2–CH2–OH.
Физические свойства спиртов. Спирты растворимы в большинстве органических растворителей, первые три простейших представителя – метанол, этанол и пропанол, а также третичный бутанол (Н3С)3СОН – смешиваются с водой в любых соотношениях. При увеличении количества атомов С в органической группе начинает сказываться гидрофобный (водоотталкивающий) эффект, растворимость в воде становится ограниченной, а при R, содержащем свыше 9 атомов углерода, практически исчезает.
Благодаря наличию ОН-групп между молекулами спиртов возникают водородные связи.





 (-COOH)
(-COOH)

 (-COOR)
(-COOR)

 (-CONH2CONH2)
(-CONH2CONH2)

 есть две гидроксильных группы, в большинстве случаев нестабильны и легко превращаются в альдегиды, отщепляя при этом воду: RCH(OH)2 ® RCH=O + H2O
есть две гидроксильных группы, в большинстве случаев нестабильны и легко превращаются в альдегиды, отщепляя при этом воду: RCH(OH)2 ® RCH=O + H2O , не существуют.
, не существуют.







