Содержание
Стр.
Содержание. 2
Занятие 1. 2
I. Основные типы реакций поликонденсации. 2
1. Полиэтерификация. 2
Примеры полимеров, получаемых по реакции полиэтерификации. 2
1.1. Полиэтиленгликольтерефталат (ПЭТФ) 2
1.2. Поликарбонаты (ПК) 2
Занятие №2 + К/р №4. 2
1.3. Олигомалеинаты (ОМ) 2
1.4. Олигоакрилаты (ОА). 2
Занятие №3. 2
1.5. Алкидные смолы. 2
2. Реакции полиамидирования. 2
2.1. Полиамид 66. 2
2.2. Полиамид 610. 2
2.3. Ароматические полиамиды. Фенилон (Номикс – США) 2
Занятие №4. 2
3. Реакции образования полиимидов (полициклоконденсация). 2
3.1. Линейные полиимиды. 2
Сетчатые полиимиды.. 2
3.2. Бисмалеинимиды и их отверждение. 2
3.3. Полиимидные смолы марок PMR и их отверждение (Алициклические полиимиды). 2
Занятие №5 + к.р. №5. 2
4. Получение фенолоальдегидных олигомеров. 2
4.1. Резольные олигомеры. 2
4.2. Новолачные олигомеры. 2
4.3. Отверждение резольных смол. 2
4.4. Отверждение новолачных смол. 2
Занятие №6. 2
5. Реакции образования и отверждения эпоксидных олигомеров и смол. 2
5.1. Образование эпоксидных смол. 2
5.2. Отверждение эпоксидных смол. 2
Занятие №7. 2
6.Реакции образования теплостойких термопластов. 2
6.1. Полифениленоксид. 2
6.2. Полифениленсульфид. 2
6.3. Полисульфон. 2
7. Реакции образования линейных и сетчатых полиуретанов. 2
7.1. Линейные полиуретаны.. 2
7.2. Разветвленные и сетчатые полиуретаны.. 2
Занятие №8 + к.р. №6. Ошибка! Закладка не определена.
Занятие 1.
I.Основные типы реакций поликонденсации.
Полиэтерификация.
1. Полиэтерификация – это реакция образования сложных полиэфиров при взаимодействии двух- или поли атомных спиртов и двух- или полиосновных карбоновых кислот.
Общий вид реакции:
1. 
Реакция полиэтерификацииподобно многим другим реакциям поликонденсации является равновесной (обратимой), поэтому для достижения высоких степеней завершенности реакции и достижения высокой молекулярной массы необходимо непрерывно удалять побочный продукт (воду) из объема реакционной смеси. Во избежании нежелательных побочных реакций, например дегидратации спирта, необходимо тщательно соблюдать температурный режим реакции.
Реакция катализируется кислотами, поэтому введение кислотного катализатора увеличивает её скорость.Отсутствие катализатора влияет на скорость реакции. Но не влияет на равновесную степень полимеризации. В отсутствии добавок сильной кислоты (катализатора) реакция самокатализируется благодаря присутствию оксикислот в реакционной смеси,т.е. реакция относится к так называемымсамокатализируемым реакциям.
Самокатализируемая реакция полиэтерификации является реакцией третьего порядка и уравнение ее имеет вид::
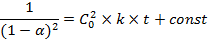
Где: k – константа скорости реакции;
Α – степень конверсии карбоновых групп.
Полиэтерификация, катализируемая кислотами (H2SО4, HCl, или др.) описывается уравнением второго порядка:

В целом реакция достаточно медленная. k' = 10-4c-1; энергия активации ∆Е≈120 кДж/моль.
Для увеличения скорости реакции и регулирования (уменьшения) количества низкомолекулярных компонентов, а так же обеспечения удаления их из реакционно-способной системы вместо карбоновых кислот используют их ангидриды или хлорангидриды:
2. Ангидриды: 
3. Хлорангидриды:

Эта реакция необратима, т.к. хлористый водород улетучивается изсостава реакционной смеси.
Уменьшения количества низкомолекулярных продуктов можно добиться, используя так же оксикислоты:
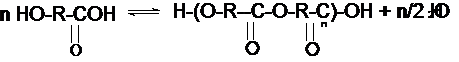
4. На практике для получения сложных полиэфиров часто используют реакцию переэтерификации, при этом взаимодействуют ди- или полиатомные спирты и моно- или диэфиры карбоновых кислот:

R’’OH – одноатомный спирт.
Примеры полимеров, получаемых по реакции полиэтерификации.
Поликарбонаты (ПК)
Поликарбонаты – это сложные полиэфиры угольной кислоты и диоксисоединений. Общей формулой:
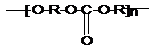
В зависимости от природы Rполикарбонаты могут быть алифатическими или ароматическими,а в зависимости от функциональности исходных компонентов: линейными, разветвленными или сетчатыми. Наибольшее практическое применение получили линейные ароматические поликарбонаты, в частности получаемые на основе дифенилолпропана (бисфенол-А) и дихлорангидрида угольной кислоты (фосген). В промышленности такие поликарбонаты получают фосгенированиембисфенола-А в газообразной среде, в присутствии пиридина или раствором фосгена в инертном органическом растворителе (например метиленхлориде).
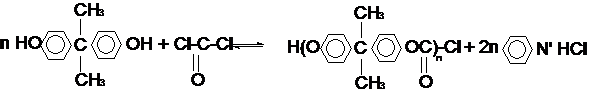
Реакция в среде пиридина между бисфенолом А и фосгеном протекает в высокой скоростью при комнатной или даже более низкой температурой. Для получения поликарбоната с высокомолекулярной массой и оптимальными свойствами необходимо растворить его в пиридине, который берут в большом избытке. Дополнительно в реакционную смесь вводят инертный растворитель – метиленхлорид, бензол, толуол и др. К полученному в процессе реакции вязкому раствору поликарбоната после отмывки хлоргидрата пиридина при перемешивании добавляют осадитель (например, гептан), после чего отфильтровывают получившийся тонкодисперсный порошок, который сушат в и вакууме его при 1200С. В результате получают полимер с ММ = 60000 ÷ 80000 атм. ед.
Занятие №2+ К/р №4
Олигомалеинаты (ОМ)
Олигомалеинаты – это продукты взаимодействия малеиновой кислоты, или её ангидрида, с двухатомными спиртами (гликолями). Часто при получении олигомалеинатовв дополнении к малеиновой кислоте добавляют, так называемые модифицирующие кислоты илиангидриды:
- фталевый ангидрид; - изо-, терефталевые кислоты; - гекса-, тетрагидрофталевый; - эндиковый ангидриды- и др.
Из двухатомных спиртов используют:- моно-, ди-, триэтиленгликоли; - 1,2 пропиленгликоль; - производные дифенилолпропана
Олигомалеинаты получают поликонденсацией в расплаве при 1700÷ 2300С, либо в растворе 1000-1500С концентрация раствора 10-20%, растворитель – толуол, ксилол и др.
Если в синтезе используют ангидриды двухосновных кислот, то процесс образования олигомалеинатов протекает в две стадии:
На 1 стадии происходит присоединение малеинового ангидрида к гликолю с образованием кислых моно- и диэфиров.
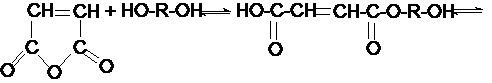 кислый моноэир кислый моноэир
|
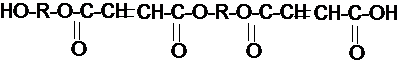 диэфир диэфир
|
Эта реакция протекает с большой скоростью при температуре 50 ÷ 150 0Си сопровождается выделением тепла (экзотермическая реакция), ее тепловой эффект равен 25 ÷ 28 кдж/моль.
На 2 стадии (поликонденсация, эндотермическая реакция) происходит взаимодействие кислых моно- и диэфиров между собой и с модифицирующей кислотой (либо её ангидридом), а так же с гликолем, не вступившим в реакцию на первой стадии.
В результате получают относительно низкомолекулярные продукты (олигомеры), которые различаются по молекулярной массе обычно:n≈1÷5; m≈0÷5; x≈1÷20
Вторая стадия этой реакции собственно реакция поликонденсации, относится к реакциям второго порядка при 200 0С. k~(30÷120)×10-3г/моль×с., ∆Е~50:84 кДж×моль. Для ускорения реакции используют катализаторы: HCl, ацетат натрия, n - толуолсульфокислоту и др. Продолжительность синтеза 6 ÷ 20 часов. Синтез сопровождается побочными реакциями: превращением эфиров малеиновый кислоты в фурматы (цис- и транс изомеризация), присоединением гликолй по двойным связям и др.
Олигомалеинаты могут быть превращены в сетчатые полимеры по реакциям трехмерной радикальной полимеризации.
Олигоакрилаты (ОА).
Олигоакрилаты – это продукты взаимодействия гликолей (полиолов, бисфинолов) с насыщенными двухосновными кислотами (ангидридами) и ненасыщенными одноосновными кислотами.
Для синтеза ОА используют:- моно-, ди-, триэтиленгликоли:
- 1,3пропан-, 1,4 бутан-, 1,6 гександиолы; - триметилолпропан; - глицерин; - бисфенол-А
- и др.
Из насыщенных (двухосновных) кислот используют:
- изо- или терефталевые кислоты; либо фталевый ангидрид.
Из ненасыщенных (одноосновных) кислот:
- акриловую кислоту или- метакриловую кислоту, которые содержат одну функциональную группу (СООН), принимающую участие в реакции поликонденсации. Эти кислоты способствуют регулированию роста цепи – после вступления ее в реакцию рост цепи прекращается. Такие вещества называются телогены.
Такую реакцию называют конденсационной теломеризацией.
Средняя степень полимеризации при синтезе олигоакрилатовопределяется концентрацией сходных компонентов, прежде всего одно- и двухосновных кислот.
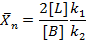
[L], [B] – число молей двух- и одноосновных кислот
k1 – константа скорости роста цепи при взаимодействии бифункциональных мономеров
k2 – rонстанта скорости обрыва цепи при реакции с монофункциональным соединением (телогеном). Для получения олигоакрилатов с n =1 при функциональности гликоля (полиола) f>2 исходные компоненты должны быть взяты в соотношении: [L]: [D]: [B] = n: (n+1): 2 (f-1)
Где: [D] – число молей гликоля (полиола).
Для получения более высокомолекулярных олигоакрилатов компоненты необходимо брать в соотношении: [L]: [D]: [B] = n: (n+1): [n (f-2) +f]
Синтез олигоакрилатов обычно проводят при 800-1400С в среди инертных растворителей (ароматические углеводороды, хлорпроизводные ароматических и алифатических углеводородов). В качестве катализатора используют минеральные и органически сульфокислоты. Варьируя соотношение компонентов и используя катализаторы получают олигоакрилаты с ММ от 300 до 5000 атм. ед.
Олигоакрилаты могут быт превращены в сетчатые полимеры по реакциям трехмерной радикальной полимеризации.
Занятие №3
Алкидные смолы.
Алкидные смолы (АС) – это продукты взаимодействия многоосновных кислот, многоатомных спиртов и одноосновных высших жирных кислот.
Наиболее широкое распространение получилиалкидные смолы, получаемые на основе фталевой кислоты (её ангидрида) и глицерина (их называют глифталевые алкидные смолы), либо пентаэритрита(их называют пентафталевые алкидные смолы).
В качестве одноосновной жирной кислоты используют олеиновую кислоту
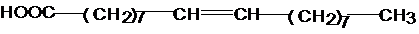
Основная реакция при синтезе алкидных смол – полиэтерификация. Поскольку в этой реакции наряду с монофункциональной (жирная кислота) и бифункциональной (фталевая кислота или её ангидрид) участвует полифункциональный мономер глицерин (f=3), либо пентаэритрит (f=4), то такая реакция является трехмерной. Однако, на практике алкидные смолы получают таким образом, чтоб на первой стадии получался не сетчатый, а разветвленный полимер, за счет подбора соотношения компонентов.
Избежать гелеобразования удается подбором соотношения фталевой кислоты (ее ангидрида) полиола: и введением одноосновной жирной кислоты, выполняющей роль телогена – регулятора роста.
Степень полиэтерификации, достигаемая на заключительных стадиях реакции, во многом зависит от избытка одного из полифункциональных реагентов. На практике синтез алкидных смол проводят в избытке многоатомного спирта – 20-30%. Степень полиэтерификации на заключительных стадиях реакции возрастает с увеличением количества в реакционной смеси монофункционального компонента – жирной кислоты.
Поскольку при синтезе алкидных смолобычноиспользуют ненасыщенные жирные кислоты, то в конце реакции на концах молекул имеются двойные связи.Благодаря этому алкидные смолы могут быть легко превращены в сетчатые полимеры по реакциям трехмерной полимеризации.
Реакции полиамидирования.
Полиамидированием называют реакции образования полиамидов при взаимодействии ди- и полиосновных карбоновых кислот (или их эфиров) с ди- или полиаминами.
В общем случае образование полиамида описывается следующим уравнением:

Полиамиды могут быть так же образованы из бифункциональных мономеров, содержащих карбоксильную и аминогруппу, то есть из аминокарбоновых кислот.

Полиамидирование являетсясамокаталитической реакцией третьего порядка и в отличие от реакции этерификации – равновесие в этой реакции сдвинуто в сторону образования полимера. Поэтому при амидировании вплоть до заключительных стадий не заботятся о сдвиге равновесия в строну образования полимера. Реакцию проводят под давление в автоклавах до достижения 80-90% степени конверсии реакционноспособных групп без удаления выделяющегося при реакции воды, и только затем температуру поднимают до 2700-3000С и путем непрерывного отвода паров воды доводят реакцию до конца. Начальную стадию реакции проводят в растворе, а заключительную в расплаве, т.к. реакцию проводят при температурах выше плавления полиамида.
Для получения высокомолекулярного полимера исходный компонент необходимо брать в строго эквимольном соотношении. Избыток одного из компонентов приводит к образованию низкомолекулярного вещества с концевыми группами мономера взятого в избытке. В случае использования аминокислот эквимольное соотношение поддерживается автоматически.
В зависимости от природы диамина и кислоты получают алифатические и ароматические полиамиды.
Название полиамида складывается из приставки «поли» и двух корней, первый из которых обозначает диаминовый компонент, а второй – кислотный, и окончания «амид».
Пример 1: Полиамид, полученный из гексаметилендиамина (ГМДА) и адипиновой кислоты, называют: полигексаметиленадипинамид.
Пример 2: Метафенилендиамин и изофталевая кислота: Полиметафениленизофталамид.
Полиамиды, полученные из полиаминокислот, после приставки «поли» следующий корень, обозначает аминокислоту.
ε -аминокапроновая, поли – ε -капроамид.
Для обозначения химического состава алифатических полиамидов рядом со словом полиамид ставят одну или несколько цифр, обозначающих число атомов углерода в исходных продуктах: ГМДА+адипиноая кислота = ПА66; ε – аминокапроновая кислота = ПА-6.
Примеры полимеров, получаемых по реакциям полиамидирования:
Полиамид 66
Это алифатический полиамид, полученный полиамидированием ГМДА и адипиновой кислоты. Реакцию проводят в две стадии:
1 стадия: Взаимодействием60 – 80 % метанольного раствора ГМДА и 20% метанольного раствора адипиновой кислоты (при 500С и рН=7,6). Получаемый продукт называется соль АГ: Необходимо соблюдать стехнометрическое соотношение компонентов.
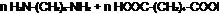 ® +H3N(CH2)6NH3+
® +H3N(CH2)6NH3+
- OOC-(CH2)4COO-
Соль АГ плохо растворяется в метаноле и после холодной промывки растворителем и сушки практически не содержит примесей. Соль АГ плавится при 202 ÷ 205 0С. Представляет собой белый кристаллический порошок.
2 стадия: Проводится в автоклаве под давлением. Используют 60% раствор соли, к которому добавляют регулятор длины цепи – уксусную кислоту. Температуру плавно повышают до 2100С и проводят реакцию при этой температуре несколько часов под давлением 17,5 атм. Затем температуру медленно повышают до 2750С и потом медленно понижают в течение 2-х часов..

Полиамид 610
Это алифатический полиамид, получаемыйполиамидированием ГМДА и себациновой кислоты, он имеет название: полигексаметиленсебацинамид.
Синтез ПА610 проводят аналогично синтезу ПА66, получая на первой стадии соль СГГМДА и себациновой кислоты, а затем проводя поликонденсацию.
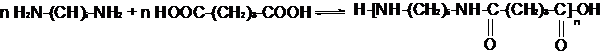
Соль СГ – кристаллический порошок белого цвета с Тпл = 170 0C. При нагревании растовряется в метаноле и этаноле.
Ароматические полиамиды. Фенилон (Номикс – США)
Это ароматический полиамид, полученный полимидированием МФДА (мефенилендиамид) и дихлорангидридаизофталевой кислоты.

Его получают методом межфазной поликонденсации или поликонденсацией в растовре:
Способ 1 - растворная технология: водный раствор МФДА и раствор соды перемешивают при температуре 50-100С в течение нескольких минутсрастворомдихлорангидридаизофталевой кислоты в тетрагидрофуране. Полимер образуется в виде порошинок размером 20 ÷ 200 мкм и выпадает в осадок.
Способ 2 (низкотемпературная поликонденсация). Охлажденный до -100…-150С раствор МФДА в диметилацетамиде перемешивают в течение часа с твердым дихлорангидридомизофталевой кислоты. Диметилацетамид выполняет роль растворителя образующегося полиамида, а также акцептора выделяющегося хлористого водорода. Образующийся полимер находится в 18 ÷ 25 % растворе диметилацетамида, содержащего 5 ÷ 10% хлористого водорода.
Аналогичным образом получают и сополимеры (смешанные полиамиды), заменяя часть МФДАна ПФДА или часть изофталевой кислоты заменяя на терефталевую кислоту. Степень замещения может составлять от 5 до 50 %. Полимер, получаемый на основе ПФДА и терефталевой кислоты выпускают под маркой «Терлон» (Россия), «Кевлар» - США.
Занятие №4
3. Реакции образования полиимидов (полициклоконденсация).
Полиимиды – это полимеры, содержащие в основной или боковой цепях макромолекул циклическую имидную группу. 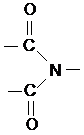 Наибольшее распространение имеют полиимиды, полученные с имидной группой в основной цепи.
Наибольшее распространение имеют полиимиды, полученные с имидной группой в основной цепи.
По химической природе полиимиды могут быть: алифатические, алициклические, ароматические. Наибольшее практическое значение имеют – ароматические.
По топологии цепи полиимиды могут быть: линейные и сетчатые, причём линейные используются для получения пленок, а сетчатые для композиционных материалов (КМ).
Линейные полиимиды.
Их получают полициклоконденсацией ароматических тетракарбоновых кислот или их производных (диангидридов или кислых диэфиров) с ароматическими (реже алифатическими) диаминами.
Используют кислоты:- пиромелитовую; - 3,3’,4,4’ бензофенонтетракарбоновую; - дифенилоксидтетракрбоновую; - дифенилтетракарбоновую
Используют диамины:- мета- и парафенилендиамин; - бензидин; - диаминодифенилоксид; - диаминодифенилсульфон
Синтез ароматических линейных полиимидов проводят в две стадии:
1. На первой стадии получают полиамидокислоту (форполимер):
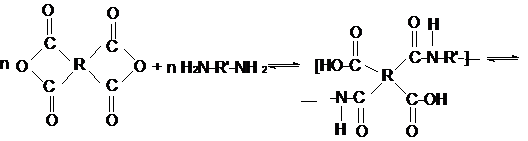
Для этого к раствору ароматического диамина в полярном растворителе при 150-350С добавляют эквимольное количество порошкообразного диангидридатетракарбоновой кислоты. Полученная полиамидокислота (ПАК) имеет 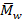 ~15000÷55000.при комнатной температуре может происходить ее самопроизвольная реакция. Поэтому ПАК хранят при температуре < 00С.
~15000÷55000.при комнатной температуре может происходить ее самопроизвольная реакция. Поэтому ПАК хранят при температуре < 00С.
2. Осуществляют реакцию имидизации ПАК путем нагревания ПАК от 2000до 300 - 4000С в вакууме или инертной среде.
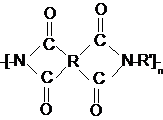
Сетчатые полиимиды
Резольные олигомеры.
Резольные олигомеры(смолы) получают нагревом фенола с молярным избытком формальдегида, в щелочной среде. Для создания щелочной среды в реакционную смесь добавляют NaOH, Ba(OH)2и др. При взаимодействии фенола с формальдегидом в таких условиях первоначально образуются фенолоспирты:

Следующим этапом реакции является взаимодействие фенолоспиртов между собой или с фенолом с образованием димеров, содержащих метиленовые мостики:

По сравнению с присоединением формальдегида к фенолу или фенолоспиртам конденсация фенолоспиртов между собой протекает сравниетльно меделенно в щелочной среде. Поэтому в молекулах образующихся олоигомеров сохраняется значптельное число метилольных групп, способных к дальнейшим превращениям. Мономеры и димеры продолжают взаимодействовать, образуя олигомеры более высокой степени полимеризации.

Скорость реакции пропорциональна концентрации ионов ОН-. Общее уравнение получения резольных олигомеров может быть представлена следующим образом:
(n+m+1)C6H5OH+(2n+m)CH2®щелочная средаH[C6H2(OH)-(CH2OH)-CH2-]n-[-C6H3(OH)-CH2-]m-С6Н3ОН (CH2OH) + (n+m) H20
Или:

Где: n– среднее число звеньев, содержащих метилольную группу;
M – среднее число звеньев, не содержащих метилольную группу.
Образующиеся олигомеры представляют собой смесь линейных и разветвленных полимер гомологов, для которых характерно наличие реакционноспособных СН2ОН групп. Среднее число фенольных ядер в молекулах олигомера (n + m + 1) находится в пределах от 4 до 10. Число метилольных групп от 2 до 5. В некоторых случаях олоигомеры могут содержать также диметиленэфирные мостики –CH2-O-CH2- между фенольными ядрами. Содержание метилольных групп и степень разветвленности цепей возрастает с увеличением избытка формальдегида (CH20) в реакционной смеси. Такие олигомеры называются резольными смолами или резолами.
Новолачные олигомеры.
Новолачные олигомеры (смолы) получают при нагревании фенола с формальдегидом в кислой среде. Причем в отличии от синтеза резольных смол в молярном избытке берется фенол, а не формальдегид.
При реакции фенола с формальдегидом в кислой среде на начальной стадии также образуются фенолоспирты, которые быстро взаимодействуют с фенолом, превращаясь в диоксидифенил метаны:

Диоксиддифенил метаны взаимодействуют с формальдегидом или фенолоспиртами. Дальнейший рост линейной цепи, в которой фенольные ядра связаны метиленовыми мостиками, происходит в результате последовательного протекания реакций присоединения и конденсации, причем скорость поликонденсации намного выше, чем присоединения, вследствие чего в молекулах олигомеров, образующихся в кислой среде, содержится лишь небольшое количество СН2ОН групп. Скорость реакции пропорционально концентрации ионов H+.
Общее уравнение реакции получения новолачных олигомеров имеет вид:
(x+1)C6H5OH+xCH2O®кислая средаH-[C6H3(OH)-CH2-]- C6H4OH+xH2O
Или:

Где: n≈4 ÷ 8.
При поликонденсации в кислой среде и молярном избытке фенола образуются олигомеры преимущественно линейного строения. Такие олигомеры называются новолачными смолами или новолаками.
В молекулах новолаков возможны три изомерных положения метиленовых мостиков: орто – орто; пара – пара; орто – пара. На изомерный состав олигомеров существенно влияют условия поликонденсации, и, в первую очередь, рН реакционной среды. Пир рН 1 – 2 образуются новолаки, в молекулах которых преимущественно содержатся мостики орто – пара. При более высоких значениях рН преобладают орто – орто связи, а при меньших значениях рН – связи пара – пара.
Отверждение резольных смол.
Резольные смолы обычно отверждают путем нагрева. Поскольку при отверждении происходит фактически продолжение поликонденсации, резолы часто называют одностадийными смолами. Различают 3 этапа отверждения резольных смол:
- А (начальныйэтап) образуется продукт–резол;
- В (промежуточный) образуется продукт – резитол;
- С (конечный) образуется продукт – резит.
На этапеА смола плавится и может растворяться, на стадии В – смола находится в резинообразном состоянии, сохраняет способность набухать в растоврителе, но не растворяться, а на стадии С она превращается в твердый материал, который не набухает и не растворяется, а при нагреве лишь частично размягчается.
При отверждении резольных смол наиболее существенную роль играют реакции конденсации, приводящие к образованию метиленовых мостиков между фенольными ядрами:
1.  + Н2О
+ Н2О
Наряду с этим при 80 ÷160 0С метилольные группы взаимодействуют между собой с образованием диметиленэфирных мостиков, которые при более высоких температурах превращаются в метиленовые мостики.:
2.  → ---СН2--- + Н20.
→ ---СН2--- + Н20.
В присутсвтвии воды протекают также ионные реакции, а после ее испарения – преимущественно свободнорадикальные реакци, приводящие к распаду диметиленэфирных мостиков. При нагревании выше 170 0С. смолы окрашиваются в красно-коричневый цвет.
Резольнгые смолы можно отверждать не только при нагревании, но и при конматной температуре. Однако для этого необходимо использовать кислотный катализатор (n- толуол сульфокислоту, НCl и др.), который обычно вводится в количестве 10 ÷ 30 % от массы смолы. При этом реакция сопрвождается выделением значительного количества тепла. Отверждение в присутствии кислот происходит с гораздо большей скоростью, чем термическое, однако эксплуатационные свойства образующихся полимеров невысоки.
Занятие №6
5. Реакции образования и отверждения эпоксидных олигомеров и смол.
Образование эпоксидных смол.
Эпоксидными называются олигомеры, создающих в молекуле не менее двух эпоксидных  или глицидиловых групп
или глицидиловых групп  .
.
Эпоксидные группы могут находиться в алифатических циклах или цепях, а глицидиловые группы чаще всего на концах цепей.
Наиболее широкое практическое применение нашли эпоксидные олигомеры, содержащие глицидиловые группы на концах цепей. Такие олигомеры получают путем взаимодействия эпихлоргидрина (3 хлор-1,2-эпоксипропана) с соединениями, содержащими активный атом водорода, например спиртами, фенолами, кислотами, аминами, амидами:
Эпихлоргидрин взаимодействует по эпоксидной группе с активным атомом водорода.Образующийсяхлоргидрин, под действием щелочи подвергается дегидрохлорированию с образованием новой эпоксидной группы.
Выделяющийся при этом HCl связывается щелочью:
Далее глицидиловая производная реагирует с активным атомом водорода другой молекулы:
Затем опять следует присоединение молекулы эпихлоргидрина и т.д.. Образующийся в результате олигомер имеет следующую структуру:
n=0 ¸ 3
В качестве катализатора при синтезе эпоксидных олигомеров используют основания, кислоты или соли металлов. Если реакцию проводят в присутствии кислот, то на концах молекул остаются хлоргидриновыегруппы, поэтому для осуществления дегидрохллорирования добавляют щелочь.
Молекулярная масса эпоксидных олигомеров определяется соотношением исходных компонентов. Из-за протекания побочных реакций (гидролиза эпихлорогидирина до глицерина, изомеризации эпоксидных групп в карбоксильные и др.) количество эпоксидных групп в молекулах получившихся олигомеров всегда меньше теоретического
Наиболее широко распространены эпоксидные олигомеры (смолы) на основе дифенилолпропана (бисфенола-А). Такие смолы называются диановые (диан – одно из названий бисфенола А). Формулу смол этого типа можно записать следующим образом:

Эпоксидные смолы получают низкой, средней и высокой молекулярной массы.
Эпоксидные смолы с низкоймолекулярной массой(350:450) получают, растворяя дифенилолпропан (1 моль)в эпихлоргидирине (8 – 10 моль), нагревают до кипения и постепенно (5-6 час) к нему добавляют водный раствор NaOH (2,2 моль). При этом неперывно отгоняют воду в виде изотропной смеси с эпихлоргидрином, который после отделения воды возвращают в реактор. После окончания процесса непрореагировавший эпихлоргидрин удаляют под вакуумом. Эпоксидную смолу растворяют в толуоле, после чего толуольный раствор промывают водой для удаления NaCl. Затем толуол отгоняют, сначала при атмосферном давлении, а потом полд вакуумом при температуре до 140 ÷ 1500С.
Смолы со средней молекулярной массой (500÷1000) получают аналогичным образом, но при молярном соотношении дифенилолпропана и эпихлоргидирина 1: (1,5 ÷ 1,9), причем процесс ведут в среде растворителя (ксило, толуол, их смесм с бутаном и др.)
Смолы с высокоймолекулярной массой (1000 ÷ 3500) синтезируют взаимодействием низкомолекулярной эпоксидной смолы с дифенилопропаном в расплаве при 140 ÷ 210 0С (катализаторы – трет- амины, мочевина, Na2CO3) или дифенилолпропана с эпихлоргидирном в присутствии щелочи в гетерогенных условиях (в системах вода органический растворитель – изопропанол, бутанол) при 70 ÷ 80 0С. Во втором случае в меньшей степени протекают побочные реакции, а эпоксидные смолы имеют более узкое ММР.
Кроме диановых, широкое распространение получили следующие эпоксидные смолы:
Ø Глицидиловые производные новолачных фенолоформальдегидных смол:

Ø Глицидиловые производные галогенированногодифенилолпропана:

Ø Глицидиловые производные ароматических аминов анилина:

Ø Глицидиловые производные (дихлор) диаминодифенилметана:

Ø Глицидиловые производные гликолей:

Причем Х = Н или СН3 , а n= 1 ÷20.
Занятие №7
6.Реакции образования теплостойких термопластов
Полифениленоксид
Полифениленоксиды это простые ароматические полиэфиры с общей формулой  или
или  , где:
, где:
Ar илиAr’ -  причем R – алкил, гологен, фенил или отсутствует.
причем R – алкил, гологен, фенил или отсутствует.
Наиболее широкое распространение получил полимер поли-2,6-диметил парафениленоксид (торговая марка. Арилокс, Норил). Для синтеза полимера используют 2,6 – диметилфенол, реже n-галоген 2,6 диметилфенол.
Получают его по реакции окислительной дегидрополимеризации. Проводят ее в инертном органическом растворителе (метанол – толуол), а окислителем служит кислород вместе с катализатором, в качестве которого используют комплексы солей металлов переменной валентности с алифатическими аминами, пиридином или диметилформамидом, а также MnO4,PbO2, AgO. Процесс проводят при 28 ÷ 32 0С в течение 40 ÷ 60 мин.

Полифениленсульфид
Полифениленсульфидыэто ароматические полиэфиры общей формулой  Где: R – нет или – CH3.
Где: R – нет или – CH3.
Полифениленсульфидыполучают поликонденсацией ди- или полигологенароматических соединений с сульфидами щелочных металлов.

Исходное соединение – парадихлорбензол.
Процесс осуществляют в растворе (например - метиллпиролидоне) при 125 ÷ 450 0С в инертной среде, используя сульфит Na (Na2S) или его кристаллогидрат (Na2S 9 HO)/ Соотношение Na2Sи n- дихлорбензола варьируется от 1: 0,9 до 1: 2.
Полимер используют в качестве связующего доя композиционных материалов, химически стойких покрытий. Марка в США – «Райтон».
Полисульфон
Полисульфонами называют полимеры, содержащие в основной цепи макромолекулы сульфоновые группы (-SO2-). В зависимости от того, к каким радикалам присоединена группа –S02- различают:
Ø Алифатические;
Ø Ароматическиеполисульфоны.
Алифатические полисульфоны термически и химически неустойчивы и используются редко. Наибольшее распространение получили ароматические полисульфоны.
Их получают по реакциям поликонденсации щелочных солей бисфенолов с ароматическими дигологенидами, в которых атомы галогена активированы электроноакцепторной группой –SO2-. Схема реакции имеет вид:

Обычно используют динатриевые и дикалиевые соли бисфеноловMe=Na илиK, а X=Cl. Реакцию проводят вапротонных биполярных растворителях (диметилсульфоксиде или тетраметиленсульфоне) при 130 ÷ 140 0С в отсутствие катализатора. Реакция протекает быстро и практически не сопровождается побочными процессами. Наличие примесей воды приводит к снижению молекулярной массы образующегося полимера.
На основе динатриевых солей бисфенола А получеютполисульфон А следующей структуры:

n= 60 ÷ 100.
7. Реакции образования линейных и сетчатых полиуретанов.
Полиуретанами называют полимеры, содержащие в основной цепи макромолекулы уретановые группы: 
В зависимости от типа исходных соединений в макромолекуле полиуретана могут, помимо уретановых групп, присутствовать амидные, мочевиновые, простые и сложные эфирные группы. Иногда содержание уретановых групп незначительно по сравнению с содержанием других функциональных групп, но основные свойства этих полимеров определяются именно наличием уретановых уретановых групп.
Полиуретаны получают по реакциям поликонденсации без выделения низкомолекулярных веществ (реакция полиприсоединения). В реакции участвуют ди- и полиизоцианаты, содержащие не менее двух гидроксильных групп в молекуле или иногда не менее двух аминных групп.
Исходные соединения для получения полиуретанов.
1. ДиизоцианатыOCN-R-NCO: ТДИ

| 2,4-, 2,5-, 2,6 толуилендиизоцианат
|
Диизоцианаты 4, 4' дифенилметандиизоцианат;

| 1,6 гексадиизоцианат или гексаметилендиизоцианат
|
2. Гликоли: моно-, ди- и триэтиленгликоли, бутилгликоли и др. На их основе получают линейные полиурета




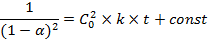



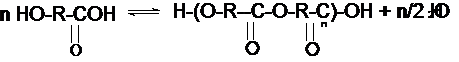

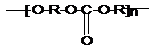
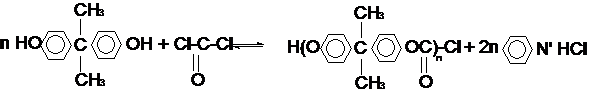
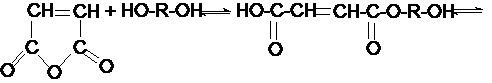 кислый моноэир
кислый моноэир
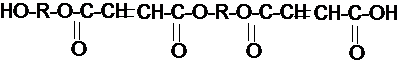 диэфир
диэфир

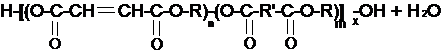
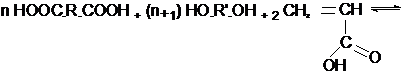
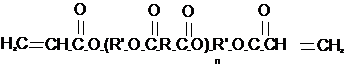
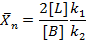
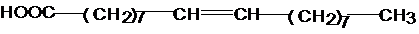
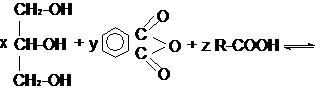
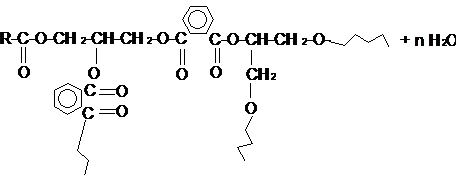


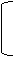
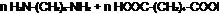 ® +H3N(CH2)6NH3+
® +H3N(CH2)6NH3+

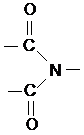 Наибольшее распространение имеют полиимиды, полученные с имидной группой в основной цепи.
Наибольшее распространение имеют полиимиды, полученные с имидной группой в основной цепи.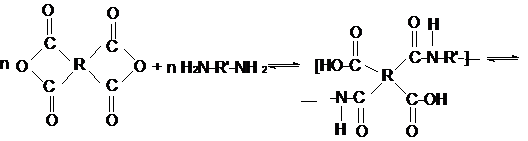
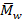 ~15000÷55000.при комнатной температуре может происходить ее самопроизвольная реакция. Поэтому ПАК хранят при температуре < 00С.
~15000÷55000.при комнатной температуре может происходить ее самопроизвольная реакция. Поэтому ПАК хранят при температуре < 00С.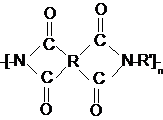






 + Н2О
+ Н2О → ---СН2--- + Н20.
→ ---СН2--- + Н20. или глицидиловых групп
или глицидиловых групп  .
.









 или
или  , где:
, где: причем R – алкил, гологен, фенил или отсутствует.
причем R – алкил, гологен, фенил или отсутствует.
 Где: R – нет или – CH3.
Где: R – нет или – CH3.








