.a–аминокислоты – кристаллические вещества, растворимые в воде. Часть из них обладает сладким вкусом. Основным источником a–аминокислот для живого организма служат пищевые белки. Многие a–аминокислоты синтезируются в организме, некоторые же необходимые для синтеза белков a–аминокислоты не синтезируются в организме и должны поступать извне. Такие аминокислоты называют незаменимыми: валин, лейцин, изолейцин, лизин, треонин, метионин, фенилаланин, триптофан
1) Свойства по группе –СООН:




 а) образование амидов
а) образование амидов
 SN(H+)
SN(H+)


 R – CH – C – OH + H – N – X R – CH – C – N – X + H2O
R – CH – C – OH + H – N – X R – CH – C – N – X + H2O
амидная связь
X – остаток другой a–аминокислоты, алифатический или ароматический радикал.
Амидная связь прочная, гидролизуется только в сильнокислой или сильнощелочной среде. Амидной связью соединены остатки a–аминокислот в пептидах и белках.



 б) образование эфиров
б) образование эфиров
 HCl сух. + NH3
HCl сух. + NH3




 R – CH – C – OH + H – OCH3 R – CH – C – O – CH3 R – CH – C – O – CH3
R – CH – C – OH + H – OCH3 R – CH – C – O – CH3 R – CH – C – O – CH3
 – Н2О – NH4Cl
– Н2О – NH4Cl
смесь a–аминокислот сложно-эфирная связь

 в) декарбоксилирование (удаление группы –СООН из a–аминокислотного фрагмента) «in vivo» идет под действием ферментов декарбоксилаз и кофермента пиридоксальфосфата. В результате образуются биогенные амины. Декарбоксилирование возможно из-за электроноакцепторного влияния –NH3+ в a–положении.
в) декарбоксилирование (удаление группы –СООН из a–аминокислотного фрагмента) «in vivo» идет под действием ферментов декарбоксилаз и кофермента пиридоксальфосфата. В результате образуются биогенные амины. Декарбоксилирование возможно из-за электроноакцепторного влияния –NH3+ в a–положении.
фермент

 – СН2 – СН – СОО– – СН2 – СН2 – NH2
– СН2 – СН – СОО– – СН2 – СН2 – NH2
– СО2
Гистамин – биогенный амин, имеет отношение
гистидин к аллергическим реакциям организма.

 фермент
фермент

 – СН – СОО– – СН2 – СН2 – NH2
– СН – СОО– – СН2 – СН2 – NH2
– СО2
Триптофан Триптамин токсичен
фермент a b g

 НООС – СН2 – СН2 – СН – СОО– НООС – СН2 – СН2 – СН2 – NH2
НООС – СН2 – СН2 – СН – СОО– НООС – СН2 – СН2 – СН2 – NH2
– СО2 g–аминомасляная (ГАМК) является
Глутаминовая нейромедиатором головного мозга.

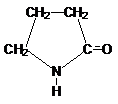 ГАМК под названием гаммалон или аминалон применяется при лечении нервно-психических заболеваний. При нагревании ГАМК подобно g–оксикислотам подвергается внутримолекулярной циклизации с образованием лактама. Лактамы – это циклические амиды, гидролизуются в кислой и щелочной среде.
ГАМК под названием гаммалон или аминалон применяется при лечении нервно-психических заболеваний. При нагревании ГАМК подобно g–оксикислотам подвергается внутримолекулярной циклизации с образованием лактама. Лактамы – это циклические амиды, гидролизуются в кислой и щелочной среде.

 to
to
–H2O g-бутиро лактам (пирролидон–2)

На основе пирролдиона–2 синтезированы замещенные по N лактамы:
пирацетам (ноотропил) – поливинилпирролидон –
влияет на мышление эффективный заменитель плазмы крови


 Для незамещенных по N лактамов характерна лактам–лактимная таутомерия – динамическое равновесие между лактамной и лактимной формой, вызванное свободной обратимой миграцией Н между N и О в фрагменте цикла – N – C –
Для незамещенных по N лактамов характерна лактам–лактимная таутомерия – динамическое равновесие между лактамной и лактимной формой, вызванное свободной обратимой миграцией Н между N и О в фрагменте цикла – N – C –
лактам лактим
2) Свойства a–аминокислот по группе –NH2:
А) образование оснований Шиффа (иминов) с альдегидами (присоединение – отщепление).




 d–
d–
 d+ AN Е
d+ AN Е



 R – C + H – N – CH – COOH R – C – N – CH – COOH
R – C + H – N – CH – COOH R – C – N – CH – COOH
– Н2О
альдегид a–аминокислота карбиноламины неустойчивы

 R – CH = N – CH – COOH Имин (основание Шиффа)
R – CH = N – CH – COOH Имин (основание Шиффа)





 d–
d–

 d+ +NaOH
d+ +NaOH




 H – C + H – N – CH – COOH CH2 – N – CH – COOH CH2 – N – CH – COONa
H – C + H – N – CH – COOH CH2 – N – CH – COOH CH2 – N – CH – COONa
– H2O
формальдегид a–аминокислота устойчивый карбиноламин натриевая соль
a–аминокислоты
б ) дезаминирование (удаление NH2–группы) – важная реакция организма. Так снижается избыток a–аминокислот в организме. (Пути образования NH3 в организме).
 Неокислительное (без О2) дезаминирование «in vivo» встречается в грибах, бактериях, ведет к образованию непредельных a- и b- кислот.
Неокислительное (без О2) дезаминирование «in vivo» встречается в грибах, бактериях, ведет к образованию непредельных a- и b- кислот.
аспартаза


 НООС – СН – СН – СООН С = С
НООС – СН – СН – СООН С = С

аспарагиновая фумаровая кислота
 Окислительное дезаминирование «in vivo» идет с участием дегидрогеназ и кофермента НАД+ или НАДФ+ и ведет к образованию токсического NH3, который включается в организме в цикл мочевины.
Окислительное дезаминирование «in vivo» идет с участием дегидрогеназ и кофермента НАД+ или НАДФ+ и ведет к образованию токсического NH3, который включается в организме в цикл мочевины.
ф-т + Н2О




 R – C – COOH + НАД+ НАДН + Н+ + R – C – COOH R – C – COOH + NH3
R – C – COOH + НАД+ НАДН + Н+ + R – C – COOH R – C – COOH + NH3
окислен. восстан.
a–аминокислота форма форма a–иминокислота a–оксокислота аммиак
Дезаминирование «in vitro» с азотной кислотой (HNO2) используют для количественного определения a–аминокислот (метод Ван-Слайка).


 R – CH – COOH + HNO2 R – CH – COOH + H2O + N2
R – CH – COOH + HNO2 R – CH – COOH + H2O + N2
a–аминокислота a–гидроксикислота по количеству N2 судят о
количестве a–аминокислоты
3).
Обратное окисление тиогрупп лежит в основе ряда окислительно-восстановительных процессов в клетке.

 HS – CH2 – CH – COOH S – CH2 – CH – COOH
HS – CH2 – CH – COOH S – CH2 – CH – COOH

 окисление
окисление

 HS – CH2 – CH – COOH восстановление S – CH2 – CH – COOH
HS – CH2 – CH – COOH восстановление S – CH2 – CH – COOH
Цистеин цистин
Превращение цистеина в цистин приводит к образованию дисульфидных мостиков, которые участвуют в формировании третичной структуры белка.
Благодаря легкому окислению тиольных групп, цистеин выполняет защитную функцию при действии на организм окислителей.






 SN(H+)
SN(H+)


 HCl сух. + NH3
HCl сух. + NH3 


 – Н2О – NH4Cl
– Н2О – NH4Cl

 – СН2 – СН – СОО– – СН2 – СН2 – NH2
– СН2 – СН – СОО– – СН2 – СН2 – NH2



 ГАМК под названием гаммалон или аминалон применяется при лечении нервно-психических заболеваний. При нагревании ГАМК подобно g–оксикислотам подвергается внутримолекулярной циклизации с образованием лактама. Лактамы – это циклические амиды, гидролизуются в кислой и щелочной среде.
ГАМК под названием гаммалон или аминалон применяется при лечении нервно-психических заболеваний. При нагревании ГАМК подобно g–оксикислотам подвергается внутримолекулярной циклизации с образованием лактама. Лактамы – это циклические амиды, гидролизуются в кислой и щелочной среде.
 to
to




 Для незамещенных по N лактамов характерна лактам–лактимная таутомерия – динамическое равновесие между лактамной и лактимной формой, вызванное свободной обратимой миграцией Н между N и О в фрагменте цикла – N – C –
Для незамещенных по N лактамов характерна лактам–лактимная таутомерия – динамическое равновесие между лактамной и лактимной формой, вызванное свободной обратимой миграцией Н между N и О в фрагменте цикла – N – C –





 d–
d–
 d+ AN Е
d+ AN Е


 R – CH = N – CH – COOH Имин (основание Шиффа)
R – CH = N – CH – COOH Имин (основание Шиффа)
 d+ +NaOH
d+ +NaOH


 Неокислительное (без О2) дезаминирование «in vivo» встречается в грибах, бактериях, ведет к образованию непредельных a- и b- кислот.
Неокислительное (без О2) дезаминирование «in vivo» встречается в грибах, бактериях, ведет к образованию непредельных a- и b- кислот.

 НООС – СН – СН – СООН С = С
НООС – СН – СН – СООН С = С
 Окислительное дезаминирование «in vivo» идет с участием дегидрогеназ и кофермента НАД+ или НАДФ+ и ведет к образованию токсического NH3, который включается в организме в цикл мочевины.
Окислительное дезаминирование «in vivo» идет с участием дегидрогеназ и кофермента НАД+ или НАДФ+ и ведет к образованию токсического NH3, который включается в организме в цикл мочевины.



 R – C – COOH + НАД+ НАДН + Н+ + R – C – COOH R – C – COOH + NH3
R – C – COOH + НАД+ НАДН + Н+ + R – C – COOH R – C – COOH + NH3

 R – CH – COOH + HNO2 R – CH – COOH + H2O + N2
R – CH – COOH + HNO2 R – CH – COOH + H2O + N2

 окисление
окисление




