

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

История развития хранилищ для нефти: Первые склады нефти появились в XVII веке. Они представляли собой землянные ямы-амбара глубиной 4…5 м...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

История развития хранилищ для нефти: Первые склады нефти появились в XVII веке. Они представляли собой землянные ямы-амбара глубиной 4…5 м...
Топ:
Комплексной системы оценки состояния охраны труда на производственном объекте (КСОТ-П): Цели и задачи Комплексной системы оценки состояния охраны труда и определению факторов рисков по охране труда...
Методика измерений сопротивления растеканию тока анодного заземления: Анодный заземлитель (анод) – проводник, погруженный в электролитическую среду (грунт, раствор электролита) и подключенный к положительному...
Эволюция кровеносной системы позвоночных животных: Биологическая эволюция – необратимый процесс исторического развития живой природы...
Интересное:
Берегоукрепление оползневых склонов: На прибрежных склонах основной причиной развития оползневых процессов является подмыв водами рек естественных склонов...
Уполаживание и террасирование склонов: Если глубина оврага более 5 м необходимо устройство берм. Варианты использования оврагов для градостроительных целей...
Лечение прогрессирующих форм рака: Одним из наиболее важных достижений экспериментальной химиотерапии опухолей, начатой в 60-х и реализованной в 70-х годах, является...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Задания с комментариями и решениями
Пример 8. Из числа указанных в ряду элементов
1) Na
2) К
3) Si
4) Mg
5) С
выберите два элемента, которые проявляют постоянную степень окисления равную +1.
Постоянную степень окисления +1 в соединениях имеют металлы IA группы. В приведенном ряду элементов металлами IA группы являются натрий и калий.
Ответ: 12
Пример 9. Из числа указанных в ряду элементов
1) Na
2) К
3) Si
4) Mg
5) С
выберите два элемента, которые могут проявлять отрицательную степень окисления.
Отрицательную степень окисления в соединениях могут проявлять только неметаллы. В приведенном ряду элементов неметаллами являются углерод и кремний.
Ответ: 35
Пример 10. Степень окисления +2 атом углерода имеет в соединении
1) СO2
2) СВr4
3) НСООН
4) СН3СООН
Определим степени окисления углерода в указанных соединениях с учетом того, что атом водорода в органических соединениях проявляет степень окисления +1, атом галогена -1, а атом кислорода -2. В молекулах СO2, CBr4, НСООН степень окисления углерода равна, соответственно, +4, +4 и +2. В молекуле уксусной кислоты атомы углерода имеют разные степени окисления: -3 и +3. Таким образом, степень окисления +2 имеет атом углерода в молекуле муравьиной кислоты.
Ответ: 3
Пример 11. Установите соответствие между химической формулой соединения и степенью окисления фосфора в нем.
ХИМИЧЕСКАЯ ФОРМУЛА

| СТЕПЕНЬ ОКИСЛЕНИЯ ФОСФОРА 1) +1 2) +3 3) +5 4) -1 5) -3 |
Определим степень окисления фосфора в каждом из соединений, указанных в первом множестве. Это можно сделать, используя правило электронейтральности: алгебраическая сумма степеней окисления всех элементов равна нулю. Например, для кислоты Н3РO2 имеем:

|
|
Следовательно, степень окисления фосфора в этом соединении равна +1.
Затем установим соответствие между элементами обоих множеств:
A) Н3РO3 - ответ 2;
Б) Н3РO4 - ответ 3;
B) Н3РO2 - ответ 1;
Г) Н4Р2O7 - ответ 3.
Полученную последовательность цифр запишем в таблицу
| А | Б | В | Г |
Ответ: 2313
Пример 12. Установите соответствие между формулой соли и степенью окисления углерода в ней.
ФОРМУЛА СОЛИ

| СТЕПЕНЬ ОКИСЛЕНИЯ УГЛЕРОДА 1) -4 2) -2 3) 0 4) +2 5) +3 6) +4 |
Вспомним, что такие элементы как калий, кальций и натрий проявляют постоянную степень окисления (+1, +2, +1, соответственно). Кислород, как правило, имеет степень окисления -2. Водород, как правило, +1. Поскольку сумма всех степеней окисления в молекуле равна нулю, то в первом соединении углерод должен иметь степень окисления +4, во втором также +4, в третьем +2, в последнем +3. Покажем на примере соединения NaHC2O4как найти степень окисления углерода.
Обозначим степень окисления как q. Тогда, с учётом выше сказанного, можем записать:
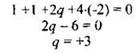
Ответ: 6645
Задания для самостоятельной работы
26. Наименьшую степень окисления сера имеет в соединении

Ответ: 
27. В каких из перечисленных соединений фосфор проявляет максимальную степень окисления?

Ответ: 
28. Из числа указанных в ряду элементов
1) N
2) Аl
3) Li
4) Р
5) С
выберите два элемента, которые в летучих водородных соединениях проявляют степень окисления равную -3.
Ответ: 
29. Из числа указанных в ряду элементов
1) N
2) Аl
3) Li
4) Р
5) С
выберите два элемента, которые в соединениях проявляют постоянную степень окисления.
Ответ: 
30. Из числа указанных в ряду элементов
1) N
2) Аl
3) Li
4) Р
5) С
выберите два элемента, которые образуют оксиды общей формулы ЭO2.
Ответ: 
31. Какие из приведенных неметаллов не проявляют высшей степени окисления, равной номеру группы?
1) N
2) S
3) F
4) Вr
5) O
Ответ: 
32. Из числа указанных в ряду элементов
1) N
2) Аl
3) Li
4) Р
5) С
выберите два элемента, образующих бинарные соединения с водородом, в которых степень окисления водорода равна -1.
|
|
Ответ: 
33. Степень окисления, равную +3, железо имеет в соединениях:

Ответ: 
34. Степень окисления +7 иод имеет в соединениях

Ответ: 
35. Какие из приведенных элементов проявляют степень окисления +7?
1) N
2) Fe
3) Мn
4) Вr
5) F
Ответ: 
36. Установите соответствие между формулой частицы и степенью окисления азота в ней.
ФОРМУЛА ЧАСТИЦЫ

| СТЕПЕНЬ ОКИСЛЕНИЯ АЗОТА 1) -3 2) -2 3) +2 4) +3 5) +4 6) +5 |
Ответ:
| А | Б | В | Г |
37. Установите соответствие между формулой вещества и степенью окисления углерода в нем.
ФОРМУЛА ВЕЩЕСТВА
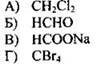
| СТЕПЕНЬ ОКИСЛЕНИЯ УГЛЕРОДА 1) -4 2) -2 3) 0 4) +2 5) +4 |
Ответ:
| А | Б | В | Г |
38. Установите соответствие между формулой иона и степенью окисления центрального атома в нём.
ФОРМУЛА ИОНА

| СТЕПЕНЬ ОКИСЛЕНИЯ 1) +7 2) +2 3) +3 4) +4 5) +5 6) +6 |
Ответ:
| А | Б | В | Г |
39. Установите соответствие между формулой вещества и степенью окисления азота в нем.
ФОРМУЛА ВЕЩЕСТВА

| СТЕПЕНЬ ОКИСЛЕНИЯ АЗОТА 1) -3 2) -2 3) +2 4) +3 5) +4 6) +5 |
Ответ:
| А | Б | В | Г |
1.1.4. Ковалентная химическая связь, её разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь
Задания с комментариями и решениями
Пример 13. В каком ряду находятся соединения только с ионной связью?

Ионная связь реализуется в двух случаях. Во-первых, в бинарных соединениях, образованных типичным (активным) металлом и типичным неметаллом, например, КСl, LiBr, CaF2. В этом случае разность в значениях электроотрицательностей достаточна для образования ионной связи. Во-вторых, ионная связь реализуется между сложными (составными) ионами, например, в соединениях NH4Cl (есть сложные ионы аммония NH4+ и хлорид-ионы Сl-) или NaNO3 (есть ионы натрия Na+ и сложные нитрат-анионы NO3-). Следовательно, ионная связь имеется во всех соединениях второго ряда.
Ответ: 2.
Пример 14. Ковалентную полярную и ковалентную неполярную связь имеют соответственно:
1) вода и сероводород
2) бромид калия и азот
3) аммиак и водород
4) кислород и метан
Ковалентная химическая связь образуется за счет общих электронных пар. Между атомами одного и того же элемента образуется ковалентная неполярная связь. Между атомами разных элементов, отличающихся по электроотрицательности, - ковалентная полярная связь. Это положение является основанием для выбора правильного ответа.
|
|
При этом следует обратить внимание на слово «соответственно» в условии задания, которое означает, что сначала надо выбрать соединение с ковалентной полярной связью, а затем - соединение с неполярной связью. Кроме того, чтобы предупредить возможную ошибку при выборе ответа, следует обратить внимание на название веществ и по нему судить о их составе. В этом случае будет ясно, что бромид калия в своем составе имеет ионы металла К+, что свидетельствует о ионном характере связи в этом соединении.
Ответ: 3
Пример 15. Водородная связь образуется между молекулами
1) С6Н6
2) С2Н5ОН
3) С2Н5ОС2Н5
4) НСООС2Н5
Водородная связь - это особый вид межмолекулярного взаимодействия.
Водородная связь образуется между атомом водорода одной молекулы и неподелённой парой электронов электроотрицательного элемента (например, F, О, N) другой молекулы. Такая связь не образуется между молекулами углеводородов, простых и сложных эфиров (ответы 1, 3 и 4), т.к. в их молекулах полярность связи С-Н выражена недостаточно. В молекуле спирта С2Н5ОН атом кислорода, имеющий частичный отрицательный заряд, может взаимодействовать с атомом водорода другой молекулы, имеющим некоторый положительный заряд в результате частичного смещения электронов к атому кислорода:
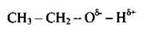
Ответ: 2
Пример 16. Во всех соединениях какого ряда имеется ионная связь?

В бинарных соединениях, образованных типичным (активным) металлом и типичным неметаллом, например, КСl, LiBr, CaF2 связь ионная. В этом случае разность в значениях электроотрицательностей элементов достаточна для образования ионной связи. Ионная связь образуется также между сложными ионами, например в соединениях NH4Cl (есть сложные ионы аммония NH4+ и хлорид-ионы Сl-) или NaNO3 (есть ионы натрия Na+ и сложные нитрат-анионы NO3-). Следовательно, ионная связь имеется во всех соединениях второго ряда.
Ответ: 2
Задания для самостоятельной работы
40. Из предложенного перечня веществ выберите два соединения, в которых присутствует ионная химическая связь.
|
|
1) NaF
2) HF
3) Сl2
4) СаСl2
5) NH3
Ответ: 
41. Водородная связь образуется между
1) атомами водорода в молекуле Н2
2) молекулами H2S
3) атомами О и Н в молекуле воды
4) молекулами СН3ОН в жидком метаноле
Ответ: 
42. В аммиаке и хлориде бария химическая связь соответственно
1) ионная и ковалентная полярная
2) ковалентная полярная и ионная
3) ковалентная неполярная и металлическая
4) ковалентная неполярная и ионная
Ответ: 
43. Веществами с ковалентной связью являются
1) СаСl2
2) KI
3) NH3
4) SO2
5) LiF
Ответ: 
44. Химическая связь в молекуле брома
1) ионная
2) ковалентная полярная
3) металлическая
4) ковалентная неполярная
Ответ: 
45. Химическая связь между молекулами воды
1) ковалентная полярная
2) ковалентная неполярная
3) водородная
4) ионная
Ответ: 
46. По донорно-акцепторному механизму образована одна из ковалентных связей в частице:
1) Н2O
2) NH4+
3) NH3
4) Н2O2
Ответ: 
47. В молекулах хлороводорода и брома химическая связь соответственно
1) ковалентная полярная и ковалентная неполярная
2) ионная и ковалентная полярная
3) ковалентная неполярная и ковалентная полярная
4) ионная и ковалентная неполярная
Ответ: 
48. Химическая связь в бромиде натрия
1) ионная
2) ковалентная полярная
3) металлическая
4) ковалентная неполярная
Ответ: 
49. Водородные связи образуются между молекулами
1) этана
2) этановой кислоты
3) этилена
4) этилацетата
5) этанола
Ответ: 
|
|
|

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Индивидуальные очистные сооружения: К классу индивидуальных очистных сооружений относят сооружения, пропускная способность которых...

Археология об основании Рима: Новые раскопки проясняют и такой острый дискуссионный вопрос, как дата самого возникновения Рима...

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!