КАФЕДРА БИОХИМИИ И МОЛЕКУЛЯРНОЙ БИОЛОГИИ
ЛЕЧЕБНОГО ФАКУЛЬТЕТА
_____________________________________________________________________________________
Карбышев М.С., Абдуллаев Ш.П.
БИОХИМИЯ ОКСИДАТИВНОГО
СТРЕССА
УЧЕБНО-МЕТОДИЧЕСКОЕ ПОСОБИЕ
Под общей редакцией проф. Шестопалова А.В.
Москва
ISBN
УДК 577.1.616.31
ББК
НАЗВАНИЕ ПОСОБИЯ: Биохимия оксидативного стресса.
Учебно-методическое пособие для самостоятельной работы студентов по специальности «Лечебное дело» под общей редакцией д.м.н., проф. Шестопалова А.В. заведующего кафедрой Биохимии и молекулярной биологии лечебного факультета ФГБОУ ВО РНИМУ имени Н.И. Пирогова Минздрава России, Москва, Издательство……………………………………………2017 г., с.53
Пособие «Биохимия оксидативного стресса» предназначено для студентов медицинских вузов, обучающихся по специальности «Лечебное дело». Задача пособия помочь студентам овладеть весьма сложным материалом курса «Биохимия».
При подготовке пособия большое внимание было уделено биохимии окислительного стресса, компонентам антиоксидантной системы и роли системы окислительного стресса в норме и при патологии. Пользование пособием возможно после освоения основ биохимии. Пособие составлено в соответствии с действующим ФГОС по специальности «Лечебное дело»
Составители: к.б.н. Карбышев М.С., Абдуллаев Ш.П.*,
*-аспирант кафедры фармакологии ФФМ ФГБОУ ВО МГУ им. М.В. Ломоносова
Рецензенты:А.Г. Мустафин - зав. кафедрой биологии ФГБОУ ВО РНИМУ им. Н.И.Пирогова Минздрава России, д.м.н., профессор
Ж.М. Салмаси – профессор кафедры патофизиологии и клинической патофизиологии ФГБОУ ВО РНИМУ им. Н.И.Пирогова Минздрава России
Рекомендовано к печати ЦКМС
ББК
УДК
ФГБОУ ВО «РНИМУ им. Н.И.ПИРОГОВА», 2017 год
Оглавление
I. Оксидативный стресс. 4
II. Активные формы кислорода. 5
III. Неферментативные пути образования АФК.Химизм процессов СРО. 7
IV. Ферментативные пути образования активных форм кислорода. 9
Микросомальные монооксигеназы. 10
Ксантиноксидоредуктаза. 10
NADPH-оксидаза. 12
NО-синтаза. 13
Миелопероксидаза. 13
V. Механизмы повреждающего действия окислительного стресса. 15
Повреждение ДНК.. 15
Повреждение белков. 16
Перекисное окисление липидов. 17
Образование комплексов. 21
VI. Антиоксидантная система организма, роль, компоненты.. 22
VII. Антиоксиданты неферментативной природы.. 26
Аскорбиновая кислота. 27
Токоферол. 27
Каротиноиды.. 29
Коэнзим Q10. 30
Тиоредоксин.. 31
Металлотионеины.. 32
XI. Ферментные системы антиоксидантной защиты.. 33
Супероксиддисмутаза. 33
Каталаза. 34
Глутатионпероксидаза. 35
Глутатион-S-трансферазы. 38
Церулоплазмин.. 40
Трансферрин.. 41
VIII. Свободнорадикальное окисление, фагоцитоз и воспаление. 42
IX. Дополнительный материал. 48
Окислительный стресс и апоптоз. 48
Окислительный стресс и канцерогенез. 50
Свободные радикалы при ишемии-реперфузии повреждения миокарда. 52
Вопросы для самоконтроля. 54
Литература. 58
I. Оксидативный стресс.
Кислород — один из самых распространенных химических элементов в природе. Реакция восстановления кислорода является основой биоэнергетики всех аэробных форм жизни.
Молекулярный кислород (О2) обладает уникальной электронной конфигурацией. Кислород имеет два неспаренных электрона и представляет собой бирадикал. Согласно теории валентных связей, молекула кислорода представляет собой два атома, объединенные двойной связью (О=O). Однако высокую реакционная способность молекулы кислорода объясняет теория молекулярных орбиталей, согласно которой кислород имеет тройную связь(•О≡О•).
Окислительный стресс – это резкое усиление окислительных процессов в организме при недостаточном функционировании антиоксидантной системы. Сигналом для запуска стресс-реакции может служить некое стереотипное изменение внутренней среды клетки. Таким сигналом вполне может являться смещение прооксидантно-антиоксидантного равновесия (или перекисного гомеостаза) в направлении активации окислительных процессов. Сбалансированность между обеими частями этой системы является необходимым условием для поддержания нормальной жизнедеятельности клетки.
Нарушение баланса, обусловленное стимуляцией свободнорадикального окисления (СО) и снижением активности антиоксидантов (АО), может привести к накоплению продуктов СО и в силу их высокой реакционной способности вызвать изменение структуры нуклеопротеидов, белков, липидов и других важнейших соединений, что чревато развитием в организме патологических процессов.
Ксантиноксидоредуктаза.
Ксантиноксидаза (КО) - Mo-, Fe- и Cu- содержащий флавопротеин, катализирующий у человека конечную стадию окисления пуринов, а также окислительную трансформацию птеридинов и некоторых алифатических и ароматических альдегидов.
В нормальных условиях КО находится в дегидрогеназной форме и катализирует окисление ксантина с участием NAD+ в качестве акцептора электронов с образованием мочевой кислоты.
Однако при некоторых патологических состояниях, в частности при ишемии органов, в результате активирования внутриклеточных Ca2+-зависимых протеаз ксантиндегидрогеназа подвергается протеолизу с отщеплением короткого пептида и необратимо превращается оксидазную форму. Акцептором электронов в оксидазной реакции выступает кислород.
Рис.5. Образование мочевой кислоты и супероксидного анион-радикала при окислении пуринов в ксантиноксидоредуктазной реакции.
КО содержит I молибденовый центр, два железосерных центра и I FAD. На молибденовом центре происходит восстановительная полуреакция каталитического цикла, когда ксантин превращается в мочевую кислоту, на FAD-центре молекулярный кислород превращается в пероксид водорода или супероксид-ион в зависимости от уровня восстановленности фермента.
Наибольшая активность КО у человека определяется в тканях печени и слизистой тонкого кишечника.
NADPH-оксидаза.
Наряду с ксантиноксидазой мощным продуцентом супероксидного анион-радикала является NADPH -оксидаза фагоцитирующих клеток.
NADPH-оксидаза катализирует восстановление молекулярного кислорода до супероксидного радикала, который затем превращается в перекись водорода и другие токсичные формы кислорода (гидропероксидный и гидроксидный радикалы). Перекись водорода, хлор и миелопероксидаза нейтрофила образуют систему, вырабатывающую чрезвычайно токсичные вещества: гипохлорит и молекулярный хлор. NADPH-оксидаза - это мультикомпонентная система, представляющая собой часть дыхательной цепи митохондрий и состоящая в исходном неактивном состоянии из флавопротеида и цитохрома. Компонентами NADPH-оксидазы являются четыре белка, которые образуют фермент после того, как собираются вместе в клеточной мембране. Два из них - относятся к мембранным белкам и образуют гетеродимер цитохром b558. Два других белка - цитоплазматические. Они соединяются с цитохромом b558 после активации фагоцита. В результате возникает NADPH-оксидаза, необходимая для образования супероксидного анион-радикала.
Генерация супероксидного анион-радикала при активации фагоцитов играет важную роль в реализации их микробицидного, цитотоксического и иммунорегуляторного действия. В результате дисмутации супероксидный анион-радикал образует перекись водорода, которая используется миелопероксидазой фагоцитов для производства гипохлорит-ионов, обладающих высокой реакционной способностью; перекись водорода при взаимодействии с ионами двухвалентого железа дает гидроксильный радикал, а при реакции с оксидом азота образуется пероксинитрит. Таким образом, супероксидный анион-радикал, генерируемый активными фагоцитами, служит основой для образования других активных свободных радикалов, обеспецивающих микробицидное действие.
5. Активные формы хлора и азота. Ферментативные реакции их образования
NО-синтаза.
Ферментативным путем образуется и азотсодержащий радикал кислорода - оксид азота (NO∙). Синтез оксида азота в организме человека и животных происходит при ферментативном окислении L-аргинина. Процесс является довольно сложным и катализируется специфическими ферментами NO-синтазами (NOS), кофакторами выступают NADPH, тетрагидробиоптерин, флавинадениндинуклетотид и флавинмононуклеотид.
Оксид азота обладает широким спектром биологического действия:
1. Играет ключевую роль в регуляции сосудистого тонуса.
2. Расслабляет гладкую мускулатуру.
3. Предотвращает агрегацию тромбоцитов и адгезию нейтрофилов к эндотелию.
4. Является важным нейромедиатором.
5. Обладает цитотоксической и микробицидной активностью.
В практическом здравоохранении широко используются нитратсодержащие противоангинальные препараты (нитроглицерин, нитросорбид, амилнитрит и др.), лечебный эффект которых обосновано связывают с их способностью высвобождать в организме оксид азота.
Миелопероксидаза.
При взаимодействии перекиси водорода с ионами хлора образуется высокоактиный гипохлорит-ион. Реакция катализируется миелопероксидазой (МПО), которая локализуется в азурофильных гранулах нейтрофильных гранулоцитов. МПО (Н2О2-оксидоредуктаза) представляет собой гемопротеин, состоящий из двух тяжелых (β) и двух легких (α) субъединиц; β-субъединицы соединены одной дисульфидной связью и содержат 2 ковалентно связанные железосодержащие простетические группы.
Первичным продуктом, образующимся при окислении хлоридов миелоперксидазой, является хлорноватистая (гипохлорная) кислота (HOCl), которая находится в равновесии с гипохлорит-ионом (OCl-):
 Н2О2 + Cl−МПОHOCl +OH-
Н2О2 + Cl−МПОHOCl +OH-
HOCl → H+ +OCl-
Стимуляция фагоцитоза, сопровождающаяся дегрануляцией нейтрофилов, приводит к высвобождению МПО и образованию гипохлорит иона, являющего важным микробицидным фактором полиморфноядерных лейкоцитов. Гипохлорит-ион является сильным окислителем, он накапливается и хранится в нейтрофилах в специальных гранулах, мембрана которых предохраняет клеточные структуры от повреждающего воздействия гипохлорит-иона.
Гипогалоиды представляют собой мощные токсины, чрезвычайно реакционоспособные в химическом отношении и взаимодействуют с органическими молекулами, либо галогенируя их, либо окисляя. При взаимодействии с гипогалоидами в первую очередь окисляются сульфгидрильные и тиоэфирные группы белков, поэтому наличие в среде белковых молекул, содержащих подобные группы, существенно снижает цитотоксическое действие гипогалоидов. Так, основным сывороточным ингибитором гипогалоидов считается альбумин.
Гипогалоиды способны окислять железосерные центры и гемовые группы ферментов. Гипогалоиды могут как индуцировать, так и ингибировать процессы перекисного окисления липидов (ПОЛ). Индукция ПОЛ может быть вызвана освобождением железа в каталитически активной форме (Fe2+), одновременно гипохлорит может взаимодействовать с Fe2+ с образованием гидроксильного радикала:
Fe2+ + OCl- + H+→ Fe3++ OH∙+ Cl-
Установлено, что гипохлорит-ион легко проникает в поверхностный фосфолипидный слой циркулирующих в крови липопротеидов низкой плотности и, вызывая их окисление, индуцирует тем самым эффективный захват окисленных липопротеинов макрофагами через «скэвэнджер»-рецепторы.
V.Механизмы повреждающего действия окислительного стресса: повреждение белков, нуклеиновых кислот, деградация мембранных фосфолипидов, образование межмолекулярных комплексов.
Активные формы кислорода химически очень агрессивны: они повреждают белки и ДНК и, главное, вызывают перекисное окисление липидов - самоподдерживающийся процесс, ведущий к тяжелому повреждению мембран
Повреждение ДНК
Молекула ДНК может повреждаться напрямую, в основном - гидроксид-радикалом и (в гораздо меньшей степени) супероксид-анионом кислорода. Гидроксид-радикал HO∙ может действовать на пуриновые и пиримидиновые основания, а также на остатки рибозы и дезоксирибозы.
Супероксид-анион обладает избирательным действием, взаимодействуя с гуаниновыми основаниями, в результате чего образуются их разнообразные окисленные производные, в том числе и конечный продукт окисления гуаниновых оснований, 7,8-дигидро-8-гидроксигуанозин. Радикалы, образующиеся при перекисном окислении липидов, также повреждают молекулы ДНК. В ряде экспериментов было показано, что митохондриальная ДНК (мтДНК) подвергается окислительному действию АФК даже в большей степени, чем ядерная, так как она находится в непосредственной близости от источников АФК и не защищена гистонами. При взаимодействии перекиси водорода, образующейся в дыхательной цепи с ионами Fe2+ и Сu2+, которые присутствуют в митохондриальных мембранах, образуется гидроксид-радикал, который и повреждает мтДНК. Она может повреждаться также и при действии перекиси водорода, образующейся в моноаминооксидазной реакции. Повреждение мтДНК приводит к неправильному синтезу компонентов дыхательной цепи, вследствие чего нарушается дыхательная цепь митохондрий и усиливается утечка супероксид-аниона. Повреждение ДНК происходит и в результате действия эндонуклеаз, которые активируются при повышении концентрации внутриклеточного Ca2+, наблюдаемом в ходе окислительного стресса.
В результате действия АФК на молекулу ДНК возникают хромосомные аберрации, которые представляют собой нарушения структуры хромосомы.
Повреждение белков
Наиболее распространенный и легко обнаруживаемый тип повреждения белков - образование карбонильных групп при окислении аминокислот: лизина, аргинина и пролина. В условиях окислительного стресса происходит окислительная модификация белков. Свободные радикалы атакуют белки по всей длине полипептидной цепи, нарушая не только первичную, но и вторичную, и третичную структуру белков, что приводит к агрегации или фрагментации белковой молекулы. Многие ферменты, содержащие SH-группы, такие как АТФазы или дегидрогеназы, легко окисляются в результате свободнорадикальной атаки.
В процессе окислительной модификации белка образуются различные стабильные метаболиты аминокислот.
Обсуждение возможной окислительной деструкции белков в организме до последнего времени носило, в основном, теоретический характер. В ряде исследований этот процесс рассматривается как одна из возможных причин инактивации ферментов, изменения структурной организации белков при состоянии окислительного стресса. Примером окислительной модификации белков является фермент - ксантиндегидрогеназа, которая превращает ксантин (и гипоксантин) в мочевую кислоту, а мочевая кислота, в свою очередь, выступает как неферментативный компонент антиоксидантной системы. В результате действия АФК происходит окисление SH-групп этого белка и превращение ксантиндегидрогеназы в ксантиноксидазу. Последняя, одновременно с мочевой кислотой, начинает образовывать супероксид-анион кислорода, что вызывает дополнительное увеличение концентрации свободных радикалов в тканях.
Если белок содержит металл с переменной валентностью, в присутствии перекиси водорода образуется гидроксид-радикал, окисляющий аминокислоты в активном центре фермента, что может привести к его инактивации. Так, в организме мышей, мутантых по гену Mn-СОД, где супероксид-анион не утилизируется в достаточной степени, повреждение комплекса I митохондрий, сукцинатдегидрогеназы и ферментов, содержащих железосерные кластеры, приводит к нарушению функции цикла трикарбоновых кислот и работы митохондриальной дыхательной цепи.
Карбоксильные группы белков под действием АФК превращаются в карбонильные группы, которые, в свою очередь, могут взаимодействовать с аминогруппами, образуя Шиффовы основания, приводящие в конечном итоге к образованию поперечных сшивок между белковыми молекулами и нарушению их активности. Процесс химического сшивания наблюдается и при гликировании белков, который существенно активируется при окислительном стрессе.
Образование комплексов.
ПОЛ влияет и на белковые молекулы. Наиболее важные изменения в белковых молекулах, вызываемые окисленными липидами, заключаются в образовании комплекса белок-окисленный липид, полимеризации белковых молекул и полимеризации фосфолипидов.
Образование белок-липидных комплексов может быть обусловлено возникновением прочной химической связи между свободными аминогруппами аминокислот и альдегидными или карбоксильными группами окисленных липидов, либо за счёт гидрофобных взаимодействий. Наиболее важную роль в образовании комплексов играет малоновый диальдегид (МДА) –один из конечных продуктов ПОЛ.
МДА образует шиффовы основания, взаимодействуя с ε-аминогруппами лизина или N-концевыми остатками аминокислот в молекуле белка. Реакцию образования внутримолекулярных и поперечных межмолекулярных сшивок можно представить следующим образом:
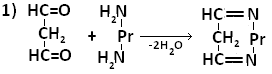


Таким образом, МДА может образовывать межлипидные, межбелковые и белок-липидные комплексы. Если такие комплексы образуют функциональные белки (ферменты, рецепторы), активность их резко изменяется. Кроме того, образование комплексов делает клеточные мембраны более ригидными, что резко затрудняет работу ферментов, т.е. активные центры оказываются как бы замурованными, и конформационные изменения, лежащие в основе изменения активности ферментов осуществляются с трудом.
Аскорбиновая кислота
Антиоксидантные свойства аскорбата основаны на существовании одноэлектронных циклических переходов между дигидро-, монодегидро- и дегидроаскорбатными формами. Именно поэтому первой мерой для повышения сопротивляемости заболеваниям, которую рекомендуют врачи – прием ударной дозы аскорбиновой кислоты. Но в присутствии ионов металлов переменной валентности аскорбат обладает прооксидантным эффектом.
Как антиоксидант аскорбат реагирует с супероксидом кислорода, перекисью водорода и радикалом токоферола, при этом окисляясь до монодегидроаскорбиновой кислоты (МДГА) или дегидроаскорбиновой кислоты (ДГА). Окисленные формы превращаются в аскорбат с помощью редуктаз МДГА и ДГА соответственно. В первом случае используется восстановленный эквивалент NADPH+H+, а во втором – глутатион.
Токоферол
Витамин Е представлен несколькими гомологами (α, β, γ- токоферолами) из которых наибольшей антиоксидантной активностью обладает α-токоферол. Эффективность действия α-токоферола, как природного антиоксиданта, обусловлена его исключительно высокой антирадикальной активностью (константа скорости его взаимодействия с перекисными радикалами составляет 3,10,3 106 л/моль с, что на 1 - 2 порядка выше соответствующих констант скоростей для многих известных синтетических и биоантиоксидантов) и стабилизацией липидного бислоя мембран путем образования прочных комплексов с полиеновыми жирными ацилами липидов. α-Токоферол взаимодействует с перекисными радикалами в качестве донора водорода:
ROO• + α-ТФ-ОН →ROOH + α-ТФ-О•

Рис 6. Механизм антиоксидантного действия витамина Е.
Токофеноксильный радикал (α-ТФ-О∙) взаимодействует с аскорбиновой кислотой (НО-АК-ОН), в результате чего радикал альфа-токоферола восстанавливается, но возникает свободный радикал полувосстановленной формы аскорбиновой кислоты – семидегидроаскорбат (НО-АК-О ∙), при взаимодействии которого с новой молекулой токофеноксильного радикала образуется дегидроаскорбиновая кислота (О=АК=О):
α-ТФ-О∙ + НО-АК-ОН → α-ТФ-ОН + НО-АК-О∙
α-ТФ-О∙ +НО-АК-О∙→ α-ТФ-ОН + О=АК=О

Рис.7. Восстановление радикала альфа-токоферола
Восстановление аскорбиновой кислоты и ее полувосстановленной формы - семидегидроаскорбиновой кислоты осуществляется в различных компартаментах клетки (микросомы, митохондрии, цитозоль) с участием NADPH+ и G-SH-зависимых редуктаз. Окисленный глутатион (GS – SG) быстро регенерируется под влиянием глутатионредуктазы, источником которого является пентозофосфатный цикл.
Представленная на схеме система регенерирующих циклов фактически исключает побочные реакции токоферилрадикала, обусловливая не только высокую антирадикальную, но и антиоксидантую активность, прерывая развитие цепей перекисного окисления липидов.
Время полураспада α-токоферола, определенное с помощью изотопной метки варьирует от 5 дней в печени и эритроцитах до 30 дней в клетках головного мозга.
Каротиноиды
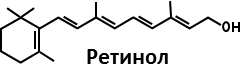
К гидрофобным антиоксидантам также относятся витамины группы А: А1 (ретинол), А2 и цис-форма витамина А1, отличающиеся дополнительными двойными связями в кольце ионона. Все соединения представляют собой циклический непредельный одноатомный спирт, состоящий из 6-членного кольца (ионон), двух остатков изопрена и первичной спиртовой группы:
 .
.
Всасывание происходит в кишечнике в присутствие липидов. В организме легко окисляются с образованием цис- (сетчатка глаза) и транс-альдегидов (остальные ткани); откладываются про запас в печени в форме более устойчивых сложных эфиров: ретинилпальмитат, ретинилацетат и ретинилфосфат. Известны также предшественники (провитамины) витамина А - каротины. Различают α и β-каротины. Наибольшей биологической активностью обладает β-каротин, поскольку он содержит два -иононовых кольца и при расщеплении в кишечнике, и возможно в печени, при участие -каротин-диоксигеназы, в присутствие молекулярного О2, из него образуются две молекулы витамина А:
 .
.
Повышенное содержание β-каротина в пищевом рационе и плазме крови оказывает профилактическое действие в отношении целого ряда заболеваний. Существует предположение, что благодаря наличию двойных связей в молекуле, витамин А может участвовать в окислительно-восстановительных реакциях, поскольку он способен образовывать перекиси, которые в свою очередь увеличивают активность антиоксидантных ферментов в клетке. Также предполагается участие витамина А в делении и дифференцировке клеток, обусловленного его действием на инициацию репликации; на рост костной ткани - участие в синтезе хондроитинсульфата. Неотъемлемым является участие витамина А в фотохимическом акте зрения.
Коэнзим Q10
КоэнзимQ10(Q10)–жирорастворимоевитамино подобное вещество. Q10 встречается в организме человека буквально повсюду, с чем связано его второе официальное название – «убихинон» (от лат.ubique–везде,повсюду). Внутри клеток Q10 в основном содержится в митохондриях. В сердечной мышце этого вещества вдвое больше, чем в любом другом органе или ткани. Сегодня известны две основные функции Q10 в живых организмах. Q10 участвует в выработке энергии в любой из клеток. Коэнзим Q10 в митохондриях участвует в синтезе АТФ как переносчик электронов, сопрягающий процессы электронного транспорта и окислительного фосфорилирования. Он является необходимым звеном для передачи электронов с комплексов I и II на комплекс III дыхательной цепи. При недостатке Q10 (затруднении в передаче электронов по дыхательной цепи) комплексы I и III становятся основными генераторами супероксид-радикалов.
Q10 – единственный жирорастворимый антиоксидант, способный синтезироваться в организме человека и животных, а также постоянно регенерировать из окисленной формы с помощью ферментных систем. Непосредственное (прямое) антиоксидантное действие Q10 заключается в улавливании свободных радикалов. Q10 способен предупреждать развитие цепных реакций свободнорадикального окисления, в том числе перекисного окисления фосфолипидов клеточных мембран и липопротеинов плазмы.
Еще одно уникальное свойство коэнзима Q10 – постоянная регенерация его окисленной формы с помощью ферментных систем организма и антиоксидантов неферментной природы (аскорбата, альфа-токоферола), что возвращает ему антиоксидантную активность.
Опосредованное (непрямое) антиоксидантное действие Q10 состоит в предупреждении образования феноксил-радикалов альфа-токоферола, то есть в недопущении возможного прооксидантного действия альфа-токоферола
Тиоредоксин
Тиоредоксины — дисульфид-содержащие редокс-активные небольшие (молекулярная масса 12 кДа, 105 остатков аминокислот) белковые молекулы, обнаруживаемые во всех аэробных организмах. Тиоредоксины выполняют функцию дисульфидоксидоредуктазы, восстанавливая NADPH-зависимым путем SH-группы различных белков и тем самым поддерживая их специфическую активность. Окисленные формы тиоредоксинов ретроредуцируются в активноесостояние тиредоксинредуктазой.

Рис. 8. Структурные переходы тиоредоксина-1
Металлотионеины
Металлотионеины – еще один класс соединений, обеспечивающих эффективное ингибирование свободнорадикальных процессов. Они представляют собой семейство низкомолекулярных белков, характеризующихся необычно высоким содержанием остатков аминокислоты цистеин (до 30% от общего количества аминокислотных остатков) и способностью связывать ионы двухвалентных металлов. Например, связывая и выделяя ионы Zn2+ металлотионеины регулируют уровень данного катиона в биологических системах.
Сульфгидрильные группы металлотионеинов могут восстанавливать супероксидный, гидроксильный радикалы и другие прооксиданты. При этом антиоксидантная активность металлотионеинов оказалась существенно выше, чем у цистеина, N-ацетилцистеина и глутатиона. Окисление SH-групп остатков аминокислоты цистеин металлотионеинов в процессе восстановления прооксидантов сопровождается выделением связанных ранее данным полипептидом ионов цинка, обладающих способностью стимулировать экспрессию металлотионеинов. Этот самооптимизирующийся процесс — важный элемент антиоксидантной защиты организма.
Супероксиддисмутаза
Супероксиддисмутаза (СОД) — важнейший энзим антирадикальной защиты. Фермент обнаружен во всех аэробных организмах. В организме млекопитающих идентифицировано две изоформы СОД: Mn-СОД (СОД2), локализованная в митохондриальном матриксе, и Cu2+/Zn+ -СОД двух типов, находящейся либо внутри клеток (в цитозоле и межмембранном пространстве митохондрий) в виде димера (СОД1), либо во внеклеточной жидкости (СОД3) в виде тетрамера. СОД на три-четыре порядка ускоряет реакцию диспропорционирования О2∙- (супероксидных анионов).
Реакция дисмутации с участием Cu,Zn-СОД идёт в две стадии, в ходе которых происходит перенос электронов с одного супероксидного анион-радикала на другой. Промежуточным акцептором этого электрона служит атом меди.
E- Cu2+ + О2∙- + H+® E-Cu+ + O2
E- Cu2+ + О2∙- + H+®E-Cu+ + H2O2
Супероксиддисмутазы обладают узкой субстратной специфичностью, действие их направлено только на полувосстановленную молекулу кислорода.
СОД может взаимодействовать также с пероксидом водорода и выступать в качестве прооксиданта, инициируя образование радикалов - супероксида и гидроксила:
Cu2+ -СОД + Н2О2® Сu+ -СОД + О2 ∙- + 2Н+;
Cu+ -СОД + Н2О2® Сu2+ -СОД + ОН-+ ·НО
Неорганические перекиси ингибируют СОД, необратимо восстанавливая медь в составе её активного центра. В отличие от неорганических липидные перекиси обратимо ингибируют СОД. Эффективным ингибитором фермента является гидроперекись линоленовой кислоты, снижающая её активность в 3,5 раза.
Супероксиддисмутаза играет важную роль в защите клеток от повреждающего действия супероксидного анион-радикала и по праву считается главным ферментом внутриклеточной АОС. СОД не только стабилизирует клеточные мембраны, предотвращая процессы перекисного окисления липидов. Снижая уровень О2∙-, она защищает от его дезактивирующего действия каталазу и глутатионпероксидазу.
Регулирующее влияние на активность СОД оказывают глутатион, цистеин, другие SH-содержащие соединения, а также опосредованно ферменты глутатионового обмена; последние, наряду с каталазой и пероксидазами различной субстратной специфичности, обеспечивают детоксикацию пероксида водорода.
Издержками этого ферментативного процесса является образование перекиси водорода, способной образовывать высокореакционные гидроксильные радикалы, но восстанавливаемая до воды в основном каталазой и глутатионпероксидазой.
Каталаза
Каталаза – хромопротеин с молекулярной массой около 240 кДа, состоит из 4 субъединиц, имеющих по одной группе гема, локализуется в основном в пероксисомах, частично – в микросомах и в меньшей мере – в цитозоле. Полагают, что каталаза не имеет высокого сродства к перекиси водорода и не может эффективно обезвреживать это соединение при низких концентрациях, имеющихся в цитозоле. В пероксисомах, где концентрация перекиси водорода высока, каталаза активно разрушает ее.
Разложение перекиси водорода каталазой осуществляется в два этапа:
Fe3+-каталаза + 2 H2O2→ окисленная каталаза + H2O2→ Fe3+-каталаза + H2O2+ O2
При этом в окисленном состоянии каталаза работает как пероксидаза. Субстратами в пероксидазной реакции могут быть этанол, метанол, формиат, формальдегид и другие доноры водорода.
Следует отметить, что около 0,5% кислорода, образующегося в результате разложения перекиси водорода, возникает в возбужденном, синглетном состоянии и таким образом в процессе разложения перекиси водорода вновь генерируются активные формы кислорода.
Каталаза в клетках, в частности, в эритроцитах, находится в едином комплексе с СОД, поэтому совместное действие этих антиоксидантных ферментов может быть представлено в виде единой реакции:

 O2-∙+ 2H+ СОД H2O2 каталазаН2О +О2
O2-∙+ 2H+ СОД H2O2 каталазаН2О +О2
Таким образом, совместное действие СОД и каталазы обеспечивает надежную защиту организма от токсического действия высоких концентраций супероксидного анион-радикала и перекиси водорода, но, в то же время, поддерживает минимальный (ниже 50,0 мкМ) контролируемый уровень этих соединений необходимых в физиологических условиях для осуществления многих клеточных процессов. В случае необходимости изменение активности одного из ферментов может резко изменить и уровень перекиси водорода. Так, например, при стимуляции фагоцитоза резко возрастает активность СОД, что приводит к образованию повышенных количеств перекиси водорода, которая используется для создания самых мощных деструктивных факторов фагоцитоза – гидроксильного радикала и гипохлорит-иона.
Глутатионпероксидаза
Глутатионпероксидаза (ГПО) -важнейший фермент, обеспечивающий инактивацию активных форм кислорода, так как разрушает и пероксид водорода и гидропероксиды липидов. Он катализирует восстановление пероксидов с помощью трипептида глутатиона (γ-глутамилцистеинилглицин). ГПО – гомотетрамерный селенопротеин, имеет молекулярную массу около 74 кДа, состоит из 4 идентичных субъединиц, в состав активного центра входит селен, который содержится в виде Se-цистеина. Селен необходим для синтеза глутатионпероксидазы.

Рис.9. Структурная формула глутатиона
Сульфгидрильная группа глутатиона (GSH) служит донором электронов и, окисляясь, образует дисульфидную форму глутатиона, в которой 2 молекулы глутатиона связаны через дисульфидную группу. Ген глутатионпероксидазы локализован в 3-й хромосоме. Глутатионпероксидаза катализирует реакции, в которых фермент восстанавливает пероксид водорода до воды, а также восстановление органических гидропероксидов (ROOH) до гидроксипроизводных, и в результате переходит в окисленную дисульфидную форму GS-SG:
2GSH + H2O2®GSSG + H2O
2GSH + ROOH®GSSG + ROH +H2O
Окисленный глутатион (GSSG) восстанавливается в глутатионредуктазной реакции с участием NADPH.

Рис. 10. Схема восстановления окисленного глутатиона.
Глутатионпероксидаза обезвреживает не только H2O2, но и разные органические липидные пероксилы, которые образуются в организме при активации ПОЛ. Такие как гидропероксиды линолевой и линоленовой кислот, холестерин-7β-гидропероксид и некоторые синтетические вещества (кумен-, трет-бутил-гидропероксиды). Глутатионпероксидаза защищает от окислительной атаки белки, липиды, никотинамидные коферменты, восстанавливает липидные перекиси.
Помимо способности восстанавливать пероксид водорода и гидропероксиды жирных кислот, ГОП обеспечиваетзащиту аэробных организмов и от чрезвычайно токсичного пероксинитритапутем восстановления его до нитрит-аниона:

Рис. 11. Предполагаемый каталитический механизм восстановления пероксинитрита глутатионпероксидазой.
Фермент глутатионпероксидаза локализирован в цитозоле в небольших количествах, а также в митохондриях. В тканях млекопитающих максимальная активность глутатионпероксидазы в печени, эритроцитах, надпочечниках. Активность фермента зависит от количества образованных пероксидов. Функционирует сопряженно сглутатионредуктазой.

Рис.12. Схема механизма работы глутатион-редокс системы.
Главной ферментативной системой плазмы крови является ГПО внеклеточных жидкостей и ГПО гидроперекисей липидов (ГПО 4), которая будучи липофильным соединением эффективно взаимодействует с гидроперекисями фосфатидилхолина, холестерина и эфиров холестерина в липопротеинах низкой плотности, восстанавливая их, следовательно, защищая от окислительной модификации. Кроме того, ГПО 4 совместно с токоферолом практически полностью подавляет ПОЛ в биологических мембранах благодаря тому, что витамин Е эффективно восстанавливает пероксирадикалы, а фермент разлагает гидроперекиси, препятствуя тем самым их вовлечению в окислительный цикл.
Глутатион-S-трансферазы.
Глутатион-S-трансферазы представлены суперсемейством мультифункциональных изоферментов, которые способствуют процессам детоксикации, используя различные механизмы, включая: 1) каталитическую




 Н2О2 + Cl−МПОHOCl +OH-
Н2О2 + Cl−МПОHOCl +OH-




 .
. .
.

 O2-∙+ 2H+ СОД H2O2 каталазаН2О +О2
O2-∙+ 2H+ СОД H2O2 каталазаН2О +О2






