[И.Т.Гороновский, Ю.М.Назаренко, Е.Ф.Некряч «Краткий справочник химика», Киев, 1974 г. C. 821.]
| Относительная плотность 25/125 С
| Весовой процент глицерина
| Вязкость, мПа×с
|
|
|
| 20°C
| 25°C
| 30°C
|
| 1,26201
|
| 1495,0
| 942,0
| 622,0
|
| 1,25945
|
| 1194,0
| 772,0
| 509,0
|
| 1,25685
|
| 971,0
| 627,0
| 423,0
|
| 1,25425
|
| 802,0
| 521,5
| 353,0
|
| 1,25165
|
| 659,0
| 434,0
| 295,8
|
| 1,24910
|
| 543,5
| 365,0
| 248,0
|
| 1,20925
|
| 61,8
| 45,72
| 34,81
|
| 1,12720
|
| 6,032
| 5,024
| 4,233
|
| 1,06115
|
| 2,089
| 1,805
| 1,586
|
| 1,02370
|
| 1,307
| 1,149
| 1,021
|
Лабораторная работа № 6
ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ УДЕЛЬНЫХ ТЕПЛОЕМКОСТЕЙ ГАЗА МЕТОДОМ АДИАБАТИЧЕСКОГО РАСШИРЕНИЯ
(метод Клемана и Дезорма)
Приборы и принадлежности: закрытый стеклянный баллон, водяной манометр, осушитель, насос.
Теория метода и описание установки
Экспериментальная установка состоит из стеклянного баллона (рис.1), соединенного с манометром М и с насосом (на рис. не показан). Посредством крана С баллон А может быть соединен с атмосферой. Если при помощи насоса накачать в баллон некоторое количество воздуха, то давление и температура воздуха внутри баллона повысятся. Вследствие теплообмена воздуха с окружающей средой через некоторое время температура воздуха, находящегося в баллоне, сравняется с температурой внешней среды t1. Давление, установившееся в баллоне,
 p1 = Н + h1,
p1 = Н + h1,
где Н – атмосферное давление, h1 – добавочное давление, измеряемое разностью уровней жидкости в манометре.
Таким образом, состояние воздуха внутри баллона, которое назовем I состоянием, характеризуется параметрами
p1 = Н + h1; V1 и t1.
Если открыть на короткое время кран С, то воздух в баллоне будет расширяться. Этот процесс расширения можно считать адиабатическим. Давление в сосуде установится равным атмосферному Н, температура газа понизится до t2, а объем будет равен V2.
Следовательно, в конце адиабатического процесса, что назовем II состоянием, параметры будут:
Н; V2 и t2 < t1.
Применяя к I и II состояниям уравнение адиабатического процесса (уравнение Пуассона)
 , (1)
, (1)
где  , а Ср и СV – удельные теплоемкости газа при постоянном давлении и объеме, соответственно, получим:
, а Ср и СV – удельные теплоемкости газа при постоянном давлении и объеме, соответственно, получим:
 ,
,
 . (2)
. (2)
Охладившийся при расширении воздух в баллоне через некоторое время вследствие теплообмена нагреется до температуры внешней среды t1: давление возрастет до некоторой величины
p2 = H + h2,
где h2 – новая разность уровней в манометре; объем воздуха не изменится и будет равен V2.
Таким образом, это состояние воздуха, которое назовем III состоянием, характеризуется параметрами
p2 = Н + h2; V2 и t1.
Так как в I и III состояниях воздух имеет одну и ту же температуру (процесс изотермический), то применяем закон Бойля-Мариотта (pV = const):
 ,
,
 . (3)
. (3)
Возведя обе части уравнения (3) в степень g
 (4)
(4)
и пользуясь выражением (2) и (4), получим:
 .
.
Логарифмируя последнее выражение и решая относительно g, находим:
 .
.
Так как давления H, H + h1 и H + h2 мало отличаются друг от друга, то разность логарифмов можно принять пропорциональными разностям самих давлений и приближенно положить
 ,
,
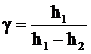 . (5)
. (5)
Порядок выполнения работы
1. Убедившись в том, что кран С закрыт, осторожно с помощью насоса нагнетают воздух в баллон до тех пор, пока разность уровней жидкости в манометре не достигнет 20–25 см.
2. Когда давление в баллоне полностью установится, показателем чего служит прекращение колебаний уровней жидкости в коленах манометра, производят по шкале отсчет разностей уровней жидкости в манометре h1.
3. Быстро открывают кран С и тотчас же (как только уровни жидкости в манометре сравняются) его закрывают. Когда давление окончательно установится, производят второй отсчет разностей уровней в манометре h2. Опыт повторяют 10 раз.
4. Подставляя в формулу (5) значения h1 и h2, взятые из каждого отдельного опыта, вычисляют g1, g2, g3 и т.д. Результаты измерений и вычислений заносят в таблицу.
| № опыта
| h1, мм
| h2, мм
| g
| 
| Dg
|  , % , %
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Контрольные вопросы
1. Что называется удельной теплоемкостью? Молярной теплоемкостью? Какова связь между ними?
2. Почему Ср > СV?
3. Какие процессы имеют место в эксперименте?
4. Почему экспериментальные результаты систематически меньше теоретически вычисленной величины?
Литература
1. Савельев И.В. Курс физики. – М.: Наука, 1989. – Т.1, §§ 68, 69.
2. Трофимова Т.И. Курс физики. – М.: Высшая школа, 1997. – §§ 53, 54, 55.
Лабораторная работа № 7



 p1 = Н + h1,
p1 = Н + h1, , (1)
, (1) , а Ср и СV – удельные теплоемкости газа при постоянном давлении и объеме, соответственно, получим:
, а Ср и СV – удельные теплоемкости газа при постоянном давлении и объеме, соответственно, получим: ,
, . (2)
. (2) ,
, . (3)
. (3) (4)
(4) .
. .
. ,
,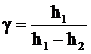 . (5)
. (5)
 , %
, %



