В химических системах вещества стремятся к минимуму внутренней энергии. Экзотермические реакции протекают самопроизвольно, так как вещества при их окончании достигают свой минимум внутренней энергии. Но также самопроизвольно протекают и эндотермические реакции - это растворение солей.Макросостояние системы тем более вероятно, чем большим числом микросостояний оно может быть описано. Условия самопроизвольного протекания реакций:
1. стремление системы к достижению минимального значения внутренней энергии
2. стремление системы к более вероятному своему состоянию.Но часто происходит столкновение этих двух определяющих факторов, и возникает состояние называемое химическим равновесием. Функция, которая учитывает оба этих фактора – энергия Гиббса. Самопроизвольно протекают те процессы, энергия Гиббса которых равна отрицательному значению.Если температура мала, то энтальпия равна энергии Гиббса и самопроизвольно протекают экзотермические реакции.Если высокая температура, то отрицательное значение имеет энергия Гиббса и реакции протекают самопроизвольно. Необратимые реакции протекают до полного израсходования одного из реагентов. Обратимые протекают во взаимопротивоположных направлениях.В состоянии химического равновесия система достигает своего минимального значения энергии и энергия Гиббса, как и константа химического равновесия, равна нулю.
31. Константа химического равновесия. Расчет Кр, Кс, Км Рассмотрим гомогенную хим.р-ю:  Р-и протекают до полного исчезновения исходных в-в, а останавливаются при достижении определенного сост.равн-я. Условия хим.равновесия:
Р-и протекают до полного исчезновения исходных в-в, а останавливаются при достижении определенного сост.равн-я. Условия хим.равновесия:  Равновесные давления участников реакции:
Равновесные давления участников реакции:  Согласно закону действ. масс
Согласно закону действ. масс 
 конст.равн-я, выраженная через парц.давл-я. Размерность
конст.равн-я, выраженная через парц.давл-я. Размерность 
 изм-е числа молей при протекании р-и.При написании конст.равновесия гетерогенных реакции учитываются парциальные давления только газообразных участников р-й, поскольку давления пара конденсированных фаз малы по сравнению с газообразными компонентами. Пример.
изм-е числа молей при протекании р-и.При написании конст.равновесия гетерогенных реакции учитываются парциальные давления только газообразных участников р-й, поскольку давления пара конденсированных фаз малы по сравнению с газообразными компонентами. Пример. 

 конст.равн-я, выраженная через концентрации.
конст.равн-я, выраженная через концентрации.  еще
еще  Соотн-я м/у конст-ми равновесия:
Соотн-я м/у конст-ми равновесия: 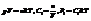


33.Принцип Ле-Шателье. При неизменных условиях химическое равновесие в системе может сохраняться сколь угодно долго. В случае же изменения условий (концентрация, температура, давление) одна из противоположно направленных реакций может ускориться, чем другая. После этого равновесие сместится, и установится новое состояние равновесия. ПринципЛе-Шателье: если на систему, находящуюся в истинном химическом равновесии, оказывают воздействие извне путем изменения какого-либо из условий, определяющих положение равновесия, то оно смещается в направлении той реакции, протекание которой ослабляет эффект произведенного воздействия. 1. Влияние температуры. Повышение температуры смещает равновесие в сторону процесса, идущего с поглощением тепла. 
 2. Влияние концентрации. При увеличении концентрации исходных веществ равновесие смещается в сторону реакции, потребляющей эти вещества (вправо).
2. Влияние концентрации. При увеличении концентрации исходных веществ равновесие смещается в сторону реакции, потребляющей эти вещества (вправо).  3. Влияние давления. Увеличение давления смещает равновесие в сторону меньшего числа молей, т.е. в сторону падения давления.Примечание. На реакцию, идущую без изменения числа молей, давление не влияет.
3. Влияние давления. Увеличение давления смещает равновесие в сторону меньшего числа молей, т.е. в сторону падения давления.Примечание. На реакцию, идущую без изменения числа молей, давление не влияет. 




 Р-и протекают до полного исчезновения исходных в-в, а останавливаются при достижении определенного сост.равн-я. Условия хим.равновесия:
Р-и протекают до полного исчезновения исходных в-в, а останавливаются при достижении определенного сост.равн-я. Условия хим.равновесия:  Равновесные давления участников реакции:
Равновесные давления участников реакции:  Согласно закону действ. масс
Согласно закону действ. масс 
 конст.равн-я, выраженная через парц.давл-я. Размерность
конст.равн-я, выраженная через парц.давл-я. Размерность 
 изм-е числа молей при протекании р-и.При написании конст.равновесия гетерогенных реакции учитываются парциальные давления только газообразных участников р-й, поскольку давления пара конденсированных фаз малы по сравнению с газообразными компонентами. Пример.
изм-е числа молей при протекании р-и.При написании конст.равновесия гетерогенных реакции учитываются парциальные давления только газообразных участников р-й, поскольку давления пара конденсированных фаз малы по сравнению с газообразными компонентами. Пример. 

 конст.равн-я, выраженная через концентрации.
конст.равн-я, выраженная через концентрации.  еще
еще  Соотн-я м/у конст-ми равновесия:
Соотн-я м/у конст-ми равновесия: 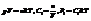



 2. Влияние концентрации. При увеличении концентрации исходных веществ равновесие смещается в сторону реакции, потребляющей эти вещества (вправо).
2. Влияние концентрации. При увеличении концентрации исходных веществ равновесие смещается в сторону реакции, потребляющей эти вещества (вправо).  3. Влияние давления. Увеличение давления смещает равновесие в сторону меньшего числа молей, т.е. в сторону падения давления.Примечание. На реакцию, идущую без изменения числа молей, давление не влияет.
3. Влияние давления. Увеличение давления смещает равновесие в сторону меньшего числа молей, т.е. в сторону падения давления.Примечание. На реакцию, идущую без изменения числа молей, давление не влияет. 




