За основу берется самая длинная цепь углеродных атомов и нумеруется с того конца, к которому ближе разветвление (для алканов) или краткая связь (для алкенов и алкинов). Цифрой указывается место заместителя и называется заместитель. Называется углеводород, которому соответствует длинная цепь.  Если углеводород непредельный, то в названии алкана окончание ан заменяется на ен (алкенов) и ин (алкинов) и цифрой указывается место (=) или (=) связи от начала цепи. Циклические углеводороды называются так же, только перед названием прибавляется приставка цикло -.
Если углеводород непредельный, то в названии алкана окончание ан заменяется на ен (алкенов) и ин (алкинов) и цифрой указывается место (=) или (=) связи от начала цепи. Циклические углеводороды называются так же, только перед названием прибавляется приставка цикло -.
2.2 Рациональная номенклатура (Р.н.) любой углеводород рассматривают как производный от простейшего представителя соответствующего ряда, у которого один и более атомов водорода замещены на радикалы (R). Называются R-лы в алфавитном порядке и в конце пишется название простейшего представителя данного ряда. Ароматические углеводороды рассматриваются как производные бензола, в молекуле которого один или несколько атомов Н замещены на радикалы.
Два радикала относительно друг друга находятся в положениях:
орто-(1,2) мета-(1,3) пара-(1,4)
2.3 Алкильные радикалы, алкилы (R). Для составления названия по номенклатурам органических соединений используются алкильные радикалы (R), получаемые «отнятием» атома водорода от молекулы алкана. Название алкилов производится от названия алкана с заменой окончания ан на окончание ил.
С
nH
2n+2 → С
nH
2n+1
алкан алкил
Например: СН
4 → СН
3 –; СН
3 – СН
3 → СН
3 – СН
2 –
метан метил этан этил
СН
3 – СН
2 – СН
3 → СН
3 – СН
2 – СН
2 –
 пропан пропил
пропан пропил
СН3 – СН – СН3 или СН3 – СН –

 изопропил СН3
изопропил СН3
 СН3 – СН2 – СН2 – СН2 –
СН3 – СН2 – СН2 – СН2 –
СН3 – СН2 – СН2 – СН3 первичный бутил
 СН3 – СН2 – СН – СН3
СН3 – СН2 – СН – СН3
вторичный бутил
 СН3 – СН – СН2 –
СН3 – СН – СН2 –
 первичный изобутил
первичный изобутил
СН3
СН3 – СН – СН3

СН
3

СН3 – С – третичный изобутил
 или третбутил
или третбутил
СН3
2.4 Вопросы для самоконтроля
- Какие соединения называются углеводородами?
- Правила названия по международной номенклатуре.
- Правила названия по рациональной номенклатуре алканов, алкенов, алкинов, аренов.
- Какие частицы называются радикалами?
2 .5 Обучающее задание №1
Охарактеризуйте и назовите данное соединение по М.н.
 СН3 – СН – СН2 – СН3
СН3 – СН – СН2 – СН3
СН3
Решение: данное соединение алкан, предельное разветвленное. Выбираем длинную цепь:
 СН3 – СН – СН2 – СН3
СН3 – СН – СН2 – СН3
Нумеруем с того конца, к которому ближе заместитель:



Указываем номер атома С, с которым связан заместитель (R), называем его и в конце названия пишем название алкана длинной цепи 2–метилбутан.
Обучающее задание №2.
Напишите структурную формулу: 2,2–диметил–5–этилгептана.
Решение: Данное соединение алкан, разветвленное. В основе длинной цепи лежит гептан, содержащий 7 атомов углерода, поэтому пишем углеродный скелет основной цепи:

Ко второму С атому приписываем два радикала СН3 – (метил), а к 5 муС атому радикал СН3 – СН2 – (этил).
 СН3
СН3

 С – С – С – С – С – С – С
С – С – С – С – С – С – С
СН3 СН2 – СН3
В конце приписываем атомы Н помня, что атом
С четырехвалентен:
 СН3
СН3

 СН3 – С – СН2 – СН2 – СН – СН2 – СН3
СН3 – С – СН2 – СН2 – СН – СН2 – СН3
СН3 СН2 – СН3
Обучающее задание №3.
Назовите углеводород по Р.н.
СН3


 СН3 – СН – С – СН2 – СН3
СН3 – СН – С – СН2 – СН3
СН3 СН3
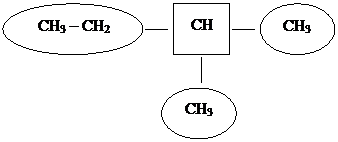
Решение: За основу берется простейший представитель алканов – метан, т.е. С атом, с которым больше всего связано радикалов, или у которого меньше находится атомов водорода и обводится в квадратик.
СН3

 СН3 – СН – – СН2 – СН3
СН3 – СН – – СН2 – СН3
СН3 СН3
Указываются радикалы в алфавитном порядке
СН3 – СН – СН3 – – СН2 – СН3
 метилэтил
метилэтил
СН3
изопропил
 Если одинаковых R-лов несколько, то их количество указывается приставками 2-ди, 3-три, 4-тетра. В конце пишется метан.
Если одинаковых R-лов несколько, то их количество указывается приставками 2-ди, 3-три, 4-тетра. В конце пишется метан.
изопропилдиметилэтилметан
Обучающее задание№4.
Напишите структурную формулу углеводорода вторбутилметилэтилметана, и назовите по М.н.
Решение: В начале пишите С атом (метан). В названии подсчитывается количество R-лов. Их три:
 СН3 – СН2 – СН –; СН3 –; СН3 – СН2 –
СН3 – СН2 – СН –; СН3 –; СН3 – СН2 –
метил этил
СН3
 вторбутил
вторбутил
Эти радикалы подписываются к основе
Простейшие R-лы пишутся вниз для удобства составления названия алкана, по М.н.






Называем по М.н. 3,4–диметилгексан.
Обучающее задание №5.
Охарактеризуйте и назовите данное соединение по М.н. и Р.н.

 СН3 – С = СН – СН2 – СН2 СН3
СН3 – С = СН – СН2 – СН2 СН3
С2Н5
Решение: Данное соединение алкен, непредельное, разветвленное. Называем по М.н. Выбираем самую длинную цепь. Нумеруем с того конца к которому ближе (=) связь



Указываем место и название заместителя: 3–метил, т.к. в длинной цепи 7 атомов углерода называем ее – гептен и указываем цифрой место (=) связи от начала цепи (от 3 го С атома) называем: 3–метилгептен–3.
Называем по Р.н. За основу берется простейший представитель алкенов – этилен (СН2 = СН2), обводим его и называем R-лы в алфавитном порядке, их три: (СН3 –) метил и
(СН3 – СН2 –) этил и пропил (СН3 – СН2 – СН2 –) в конце пишется этилен. Положения радикалов уточняются приставками α, β, обозначающими углеродные атомы этилена.

α-метил, этил-β-пропилэтилен
Обучающее задание №6.
Назовите по М.н. и Р.н. и охарактеризуйте данное соединение:
СН3

СН3 – СН2 – С – СН2 – С ≡ СН
СН3
Решение: Данное соединение относится к непредельным углеводородам – алкинам.
Называем по М.н. За основу берем самую длинную цепь, нумеруем с того конца, к которому ближе (≡) связь.





Указываем номер С атома, у которого стоят заместители (R-лы). В длинной цепи шесть С атомов, следовательно, это будет гексин, и цифрой указываем место (≡) связи (от 1 го С атома), называем: 4,4–диметилгексин–1.
Называем по Р.н. За основу берется простейший представитель алкинов – ацетилен (СН≡СН), обводим его и называем R. Так как в молекуле ацетилена всего два атома Н, которые могут быть замещены на R-лы, следовательно в данном соединении всего один R-л это первичный изогексил. Называем:

первичный изогексилацетилен
Обучающее задание №7.
Назовите данное соединение по М.н.
1,2–диметилциклопентан 1,1–диметилциклопропан
 Обучающее задание№8.
Обучающее задание№8.
Назовите соединение по Р.н. и М.н.
Решение: Данное соединение ароматическое, производное бензола, в молекуле которого 2 атома водорода замещены на радикалы (СН3 –) метил и (С2Н5 –) этил, находящиеся в пара – положении (1,4). Указываем положение заместителей, называем их, в конце пишем слово бензол.
По М.н. 1–метил–4–этилбензол
По Р.н. n–метилэтилбензол
2.6 Контрольное задание 1
| Какое из указанных соединений
|
| 1) предельное
2) непредельное
3) разветвленное
4) неразветвленное
5) циклическое
6) алкан
7) алкен
8) алкин
9) ароматическое (арен)
Назовите указанные соединения
| а) n – СН3 – С6Н4 – СН3
б) СН3 – С ≡ С – СН3
 в) СН3
СН3 – С – СН2 – СН3 в) СН3
СН3 – С – СН2 – СН3
СН3
г) СН3

СН2 = СН – С – СН3

СН3
д) С6Н6
е) С6Н12
ж) СН3 – С6Н5
|
Контрольное задание 2
| Каким соединениям соответствуют названия
|
1) СН3
 СН3 – СН – СН – СН3
СН3 – СН – СН – СН3
 С2Н5
2) СН3
С2Н5
2) СН3
 СН3 – СН2 – С – СН2 – СН3 СН3 – СН2 – С – СН2 – СН3
СН3
3) СН3 – СН = С – СН3

С2Н5
4) СН3

СН3 – С – СН2 – С ≡ СН

СН3
5) СН ≡ С – СН2 – СН – СН3

СН3
6)
7) СН3 –СН –СН – СН = СН2
СН3 СН3
 8) 8)
 9) СН3 9) СН3
 СН3 – СН – СН – СН3 СН3 – СН – СН – СН3
СН3
10) С5Н10
| А. 3,4–диметилпентен–1
Б. 2,3–диметилбутан
В. циклопентан
Г. м–ксилол (м–диметилбензол)
Д. 2,3–диметилпентан
Е. n–метилэтилбензол
Ж. 3,3–диметилпентан
З. 4–метилпентин–1
И. 4,4–диметилпентин – 1
К. 3–метилпентен–2
|
Глава 3. Алканы
Алканы – это предельные углеводороды, в молекулах которых все атомы связаны одинарными d (сигма) связями.
 Их также называют насыщенными, парафинами. углеводородами ряда метана. Опорная схема:
Их также называют насыщенными, парафинами. углеводородами ряда метана. Опорная схема:
Гомологический ряд
СН4 метан С7Н16 гептан
С2Н6 этан С8Н18 октан
С3Н8 пропан С9Н20 нонан
С4Н10 бутан С10Н22 декан
С5Н12 пентан С11Н24 ундекан
С6Н14 гексан С12Н26 додекан
Группа СН2 называется гомологической разностью
3.2 Строение. Атом углерода в алканах находится в состоянии sp3 – гибридизации, при этом «смешивается» одна S – орбиталь и три р – орбитали, образуются четыре гибридизованные орбитали, называемые sp3 орбиталями.

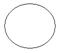

S-орбиталь p-орбиталь sp3-гибридизованная
орбиталь
Рисунок 8.
 sp3 орбитали располагаются относительно друг друга под тетраэдрическими углами. Валентный угол равен 109028’.
sp3 орбитали располагаются относительно друг друга под тетраэдрическими углами. Валентный угол равен 109028’.
Рисунок 9.
Гибридизованные орбитали, перекрываясь с орбиталями других углеродных атомов или с орбиталями атомов водорода, образуют d-связь.
Рисунок 10.
Химическая связь, образованная перекрыванием электронных орбиталей, когда центры связанных атомов находятся на одной прямой, называется d-связью. Длина d-связи равна 0,154 нм.
3.3 Изомерия. Первых три члена гомологического ряда С1 – С3 изомеров не имеют. Рассмотрим С4Н10. Напишем углеродный скелет: С – С – С – С
Как еще можно расположить углеродные атомы?
Ответ: С – С – С, т.е. разветвленная цепь
С
Добавьте к каждому С атому атомы водорода, помня, что атом углерода 4-х–валентен.
 СН3 – СН2 – СН2 – СН3; СН3 – СН – СН3
СН3 – СН2 – СН2 – СН3; СН3 – СН – СН3
Чем обусловлена изомерия алканов? СН3
Вывод. Изомерия алканов обусловлена строением углеродного скелета.
Для правильного написания изомеров более сложных алканов начинайте с написания углеродного скелета неразветвленной цепи. Например, напишите формулы изомеров состава С5Н12.
1) С – С –С–С–С Затем сокращаем эту цепь на один С
атом опуская его от 2-го С атома
 2) С – С – С – С Если переставить его к следующему
2) С – С – С – С Если переставить его к следующему
С атому, то будет то же самое, т.к.
С считать атомы углерода можно с
любого конца.
Затем сокращаем длинную цепь С атомов еще на один углероный атом, получаем 3-ий изомер.
3) С У более сложных алканов
 необходимо дальше сокращать цепь
необходимо дальше сокращать цепь
 С – С – С углеродных атомов.
С – С – С углеродных атомов.
 С
С
В конце добавляем атомы водорода

 1) СН3 – СН2 – СН2 – СН2 – СН3; 3) СН3
1) СН3 – СН2 – СН2 – СН2 – СН3; 3) СН3

 2) СН3 – СН – СН2 – СН3; СН3 – С – СН3
2) СН3 – СН – СН2 – СН3; СН3 – С – СН3
СН3 СН3
Напишите формулы всех возможных изомеров состава С6Н14. Проверьте, усвоили вы это понятие.
Как видно из предыдущих формул атомы углерода соединены с разным числом атомов углерода и водорода. Существует понятие, если С атом соединен непосредственно только с одним другим С атомом, то он называется первичным (I), если с 2-мя другими С атомами– вторичным (II),если с 3-мя – третичным (III).
Обозначается над С атомами римскими цифрами.
I II II III I
СН3 – СН2 – СН2 – СН – СН3
 I
I
СН3
3.4 Номенклатура. Первые четыре алкана имеют травиальные названия, т.е. исторически сложившиеся: метан, этан, пропан, бутан. Названия других алканов производится по двум номенклатурам.
Рациональная. Любой алкан по этой номенклатуре рассматривается, как производный от простейшего представителя – метана (СН4) в молекуле которого один, два, три или все четыре атома Н замещены на радикалы. За СН4 принимается тот С атом, в котором меньше всего атомов Н, например:
Этот С атом обводится в квадрат. От него отходят радикалы. Называются R–лы в алфавитном порядке. Если одинаковых R–лов несколько, то их количество указывается с помощью приставок: 2 – ди, 3 – три, 4 – тетра к названию радикала. В конце названия пишется слово метан. Называем: диметилэтилметан.
Дается название по Р.н.: бутилметилэтилметан. Составляем структурную формулу. Вначале пишем С атом, который принимаем за метан.В названии считаем радикалы, их всего три, следовательно от С атома отходят три связи на радикалы.
Подписываем к этим связям R–лы. Сложные R–лы пишем горизонтально, а простые вниз или вверх.
Закрепление: Назовите по Р.н.

 а) СН3 – СН – СН – СН3
а) СН3 – СН – СН – СН3
СН3 СН3

 б) СН3 – СН – СН – СН2 – СН3
б) СН3 – СН – СН – СН2 – СН3
СН3 СН2 – СН3
СН3 СН3

 в) СН3 – С – С – СН3
в) СН3 – С – С – СН3
СН3 СН3
Напишите структурные формулы:
а) изопропилэтилметана;
б) третбутилдиметилэтилметана;
в) диметилдиэтилметана.
1) Чем отличаются друг от друга изомеры, гомологи?
2) Найдите среди написанных формул изомеры и гомологи:

 СН3 СН3
СН3 СН3

а) СН3 – С – СН3; б) СН3 – (СН2)3 –СН3; в) СН3–СН – СН3

СН3
 г) СН3 – СН – СН2 – СН3; д) СН3 – СН2 – СН2 – СН3;
г) СН3 – СН – СН2 – СН3; д) СН3 – СН2 – СН2 – СН3;
СН3
 СН3
СН3
е) СН3 – СН2 – СН – СН3
3) Какие частицы называются радикалами? Приведите пример. Напишите формулу любого первичного, вторичного и третичного радикала.
4) Чем обусловлена структурная изомерия алканов?
5) Какие С атомы называются первичными, вторичными, третичными.
6) Укажите в формуле эти С атомы СН3–СН–СН–СН2–СН3
СН3 СН3
Международная номенклатура (JUPAK). В основе названия лежит название алкана самой длинной цепи атомов углерода. Эту цепь нумеруют с того конца, к которому ближе в этой цепи находятся R–лы.
5 4 3 2 1 1 2 3 4 5
С – С – С – С – С
С
Радикалы расположены выше или ниже основной цепи.
Затем указывают номер С атома, при котором находится радикал (2). Если одинаковых радикалов несколько, то перечисляют цифры, указывающие их положение через запятую
(2, 3).
5 4 3 2 1

 С – С – С – С – С
С – С – С – С – С
С С
После перечисленных цифр пишутся приставки ди, три, тетра, а затем пишется название радикала и в конце - название алкана длинной цепи.
5 4 3 2 1

 СН3 – СН2 – СН – СН – СН3
СН3 – СН2 – СН – СН – СН3
СН3 СН3 2, 3 – диметилпентан
Дано название, необходимо написать структурную формулу, например: 2, 2 – диметил – 3 – этилгептан
Необходимо начать писать формулу с основы, это гептан, в нем 7 углеродных атомов, следовательно пишется цепь из этих 7 С атомов, нумеруется слева неправо.
1 2 3 4 5 6 7
С – С – С – С – С – С – С
Затем в названии у 2-го С атома стоят два радикала – метила, а у 3-го – этил, подписываются.
СН3


 СН3 – С – СН – СН2 – СН2 – СН2 – СН3
СН3 – С – СН – СН2 – СН2 – СН2 – СН3
СН3 СН2 – СН3
Закрепление: Напишите структурные формулы и назовите:
1) 2, 3, 4 – триметилгексана назовите по Р.н.
2) изопропилметилметана по М.н.
3) назовите по 2-м номенклатурам
СН3 – СН – СН – СН2 – СН3
СН3 СН2 – СН2 – СН3
3.5 Способы получения алканов. Главными источниками получения алканов в промышленности являются нефть и природный газ, из которых получают алканы индивидуально состава С1 – С2.
Способы получения алканов делятся на 3 группы:
Реакции, не сопровождающиеся изменением числа углеродных атомов в молекуле.
Сисх=Скон
1) Гидрирование непредельных углеводородов
 СН2 СН2 + Н – Н ¾® СН3 – СН3
СН2 СН2 + Н – Н ¾® СН3 – СН3
 СН СН + 2Н – Н ¾® СН3 – СН3
СН СН + 2Н – Н ¾® СН3 – СН3
2) Восстановлением галогенопроизводных иодисто-водородной кислотой
СН3J + HJ ¾® СН4 + J2
Закрепление: а) получите по этому способу 2 – метилбутан.
б) какое иодопроизводное необходимо взять, чтобы получить 2-метилбутан?
Реакции, сопровождающиеся усложнением углеродного скелета.
Сисх<Скон
 1) Реакция Вюрца. Сущность реакции заключается в действии металлического натрия на гологенопроизводные (алкилгалогениды).
1) Реакция Вюрца. Сущность реакции заключается в действии металлического натрия на гологенопроизводные (алкилгалогениды).
СН3 J
+ 2Na ¾® СН3 – СН3 + 2NaJ
CH3 J
или 2СН3J + 2Na ® СН3 – СН3 + 2NaJ
Если вступают в реакцию разные молекулы галогенопроизводных, то при этом получаются три продукта.
 Например:
Например:
СН3 J
+ 2Na ¾® СН3 – СН2 – СН3 + 2NaJ
CН3 – СН2 J
Одновременно происходит образование веществ:
СН3 J
+ 2Na ¾® СН3 – СН3 + 2NaJ
CH3 J
 СН3 – СН2 J
СН3 – СН2 J
+ 2Na ¾® СН3 – СН2 – СН2 – СН3 + 2NaJ
СН3 – СН2 J
Закрепление: Получите по реакции Вюрца 2– метилпропан, подобрав галогенопроизводные. Сколько продуктов при этом получится?
2) Прямой синтез из элементов
С + 2Н2 ¾¾¾® СН4
8С + 9Н
2 ¾¾¾® С
8Н
18
3)
Каталитическое гидрирование (+Н2) оксида углерода
nCO + (2n+1)H2 ¾¾® CnH2n+2 + nH2O
8CO + 17H2 ¾¾® C8H18 + 8H2O
По этим способам в промышленности получают синтетический бензин.
Реакции, сопровождающиеся уменьшением числа углеродных атомов в молекуле.
Сисх>Скон

 1) Крекинг. При температуре более 4000С происходит разрыв С С связи. При этом получаются более простые насыщенные и ненасыщенные углеводороды.
1) Крекинг. При температуре более 4000С происходит разрыв С С связи. При этом получаются более простые насыщенные и ненасыщенные углеводороды.
 СН3 –СН2 – СН2 СН2 – СН3 ¾¾®СН3–СН2 –СН3+СН2=СН2 алкан алкен
СН3 –СН2 – СН2 СН2 – СН3 ¾¾®СН3–СН2 –СН3+СН2=СН2 алкан алкен
 CH3 –CH CH2– CH2 – CH3® CH3–CH2–CH3+CH2=CH–CH3
CH3 –CH CH2– CH2 – CH3® CH3–CH2–CH3+CH2=CH–CH3
CH3
При повышении температуры разрыв связи происходит ближе к концу:
t0 6000
 СН3 – СН2 – СН2 СН2 ¾¾®СН3 –СН=СН2 + СН4
СН3 – СН2 – СН2 СН2 ¾¾®СН3 –СН=СН2 + СН4
 2) Сплавление солей одноосновных карбоновых кислот с щелочами.
2) Сплавление солей одноосновных карбоновых кислот с щелочами.
Получите по этой реакции 2 – метилпропан. Какую соль необходимо взять, напишите. Вы должны догадаться, что написав формулу 2 – метилпропана, сообразите, что она должна быть увеличена на группу: – СООNа
Закрепление:
1) Всеми возможными способами получите: а) пропан;
б) 2, 2 – диметилпропан.
2) Какие галогенопроизводные необходимо взять, чтобы без побочных продуктов получить 2, 3 – диметилбутан по реакции Вюрца.
3) Какие из перечисленных ниже алкилгалогенидов необходимо использовать для получения:
а) бутана; б) пропана; в) 2 – метилбутана
 1) СН3J; 2)СН3 – СН2Сl; 3) СН3 – СНJ – СН3; 4) СН – СJ–СН3
1) СН3J; 2)СН3 – СН2Сl; 3) СН3 – СНJ – СН3; 4) СН – СJ–СН3
СН3
4) Какое вещество получится при сплавлении натриевых солей следующих кислот:

 О О
О О


 а) СН3 –СН2 – С б) СН3 – СН –С
а) СН3 –СН2 – С б) СН3 – СН –С
ОН ОН
СН3
 О
О
 в) СН3 – СН2 – СН2 – С
в) СН3 – СН2 – СН2 – С
ОН
5) Установите формулу алкана, если плотность паров его по воздуху равна 2,483.
3.6 Физические свойства алканов. Алканы состава С1 – С4 – газообразные вещества, С5 – С15 – жидкости, С16 и выше – твердые вещества. В гомологическом ряду алканов повышается tкип, tплавл., относительная плотность. Алканы с разветвленной цепью кипят при более низкой температуре, чем алканы нормального строения. Алканы нерастворимы в воде, растворяются в органических растворителях, спирте, эфире.
Алканы С1 – С2 – не имеют запаха.
Алканы С3 – С15 – имеют запах бензина, керосина.
Алканы с С16 – не имеют запаха.
Табл. №2
| Алкан
| Формула
| tпл
| tкип
| d420
|
| Метан
| CН4
| -182,5
| -161,5
| 0,4150
|
| Этан
| С2Н6
| -182,8
| - 88,6
| 0,5610
|
| Пропан
| С3Н8
| -187,7
| -42,0
| 0,5853
|
| Бутан
| С4Н10
| -138,3
| -0,5
| 0,600
|
| Пентан
| С5Н12
| -129,7
| +36,1
| 0,6262
|
| Гексан
| С6Н14
| -95,3
| +68,7
| 0,6594
|
| Гептан
| С7Н16
| -90,6
| +98,4
| 0,6838
|
3.7 Химические свойства. Алканы – неактивные вещества. За их пассивность русский химик М.И. Коновалов назвал их «химическими мертвецами». Их неактивность объясняется характером и прочностью связей С – Н (углерод-водородной) и С – С (углерод-углеродной). Прочность С – Н объясняется тем, что sp3 – орбиталь атома С подходит близко к ядру атома Н, т.к. в атоме водорода нет внутренних электронов, которые могли бы оттолкнуть электронное облако атома С.
Рисунок 11.
Прочность С – С связи обусловлена малым размером атома углерода и его тетраэдрической конфигурацией в состоянии sp3 – гибридизации. Это способствует максимальной концентрации электронного заряда между ядрами. На алканы не действуют при обычных температурах концентрированные сильные кислоты (H2SO4, HNO3 и др.), расплавленные и концентрированные щелочи (NaOH, KOH и др.) сильные окислители (KMnO4, K2Cr2O7 и др.) щелочные металлы (Na, K и др.). Поэтому металлы Na, K и другие щелочные металлы хранят в керосине. Они не выступают в реакции присоединения, в реакции гетеролитического разрыва связей. Для алканов возможен лишь гомолитический, радикальный разрыв связей С – С и С – Н и окисление частичное или полное.
 Реакции замещения, разрыв С Н.
Реакции замещения, разрыв С Н.
Эти реакции протекают по радикальному цепному характеру. Рассмотрим механизм реакции на примере хлорирования СН
4. В обычных условиях если смешать метан с хлором, то реакция не протекает. Для протекания реакции необходим инициатор, т.е. нужны атомы хлора, которые образуются при действии света или нагревания.
 Cl Cl ¾® 2Сl · (1)
Cl Cl ¾® 2Сl · (1)
Атом хлора отрывает водород от молекулы СН4.
Н3С: Н + Сl · ¾® CH3 · + HCl (2)
Образуется радикал метил (СН3 ·), который активно вступает в реакцию с молекулой Cl2.
СН3 · + Cl2 ¾® CH3Cl + Cl · (3)
хлористый
метил
Образуется хлористый метил и радикал Cl ·, который вновь реагирует с СН4 и т.д., т.е. реакции (2) и (3) повторяются, происходит рост цепи до тех пор, пока не произойдет обрыв цепи – уничтожение свободного радикала, т.е. радикалы взаимодействуя между собой образуют продукты реакции
Cl · + Cl · ® Cl2 (4)
CH3 · + ·CH3 ® CH3×CH3 (5)
CH3 · + Cl · ® CH3Cl (6)
Реакции галогенирования
СН4 + Cl2 ¾® CH3Cl + HCl
хлористый метил
СН3Cl + Cl2 ¾® CH2Cl2 + HCl
хлористый метилен
CH2Cl2 + Cl2 ¾® CHCl3 + HCl
хлороформ
СНCl3 + Cl2 ¾® CCl4 + HCl
четыреххлористый
углерод
Эти реакции используются в промышленности для получения указанных продуктов. Алканы вступают в реакции галогенирования с Сl2, Br2, F2. Фтор действует очень бурно и может разрушить органические молекулы. J2 – в реакцию не вступает. Хлорирование других алканов происходит в соответствии с правилом В.В. Марк



 Если углеводород непредельный, то в названии алкана окончание ан заменяется на ен (алкенов) и ин (алкинов) и цифрой указывается место (=) или (=) связи от начала цепи. Циклические углеводороды называются так же, только перед названием прибавляется приставка цикло -.
Если углеводород непредельный, то в названии алкана окончание ан заменяется на ен (алкенов) и ин (алкинов) и цифрой указывается место (=) или (=) связи от начала цепи. Циклические углеводороды называются так же, только перед названием прибавляется приставка цикло -.


 пропан пропил
пропан пропил
 изопропил СН3
изопропил СН3 СН3 – СН2 – СН2 – СН2 –
СН3 – СН2 – СН2 – СН2 – СН3 – СН – СН2 –
СН3 – СН – СН2 – СН3
СН3
 или третбутил
или третбутил СН3 – СН – СН2 – СН3
СН3 – СН – СН2 – СН3 СН3 – СН – СН2 – СН3
СН3 – СН – СН2 – СН3



 СН3
СН3
 СН3 – СН – – СН2 – СН3
СН3 – СН – – СН2 – СН3 Если одинаковых R-лов несколько, то их количество указывается приставками 2-ди, 3-три, 4-тетра. В конце пишется метан.
Если одинаковых R-лов несколько, то их количество указывается приставками 2-ди, 3-три, 4-тетра. В конце пишется метан. вторбутил
вторбутил











 Обучающее задание№8.
Обучающее задание№8. в) СН3
СН3 – С – СН2 – СН3
в) СН3
СН3 – С – СН2 – СН3

 СН3 – СН – СН – СН3
СН3 – СН – СН – СН3
 С2Н5
2) СН3
С2Н5
2) СН3





 8)
8) 9) СН3
9) СН3 Их также называют насыщенными, парафинами. углеводородами ряда метана. Опорная схема:
Их также называют насыщенными, парафинами. углеводородами ряда метана. Опорная схема:


 sp3 орбитали располагаются относительно друг друга под тетраэдрическими углами. Валентный угол равен 109028’.
sp3 орбитали располагаются относительно друг друга под тетраэдрическими углами. Валентный угол равен 109028’.
 С
С




 СН3 СН3
СН3 СН3
 С – С – С – С – С
С – С – С – С – С
 СН3 – СН2 – СН – СН – СН3
СН3 – СН2 – СН – СН – СН3 СН2 СН2 + Н – Н ¾® СН3 – СН3
СН2 СН2 + Н – Н ¾® СН3 – СН3 СН СН + 2Н – Н ¾® СН3 – СН3
СН СН + 2Н – Н ¾® СН3 – СН3 1) Реакция Вюрца. Сущность реакции заключается в действии металлического натрия на гологенопроизводные (алкилгалогениды).
1) Реакция Вюрца. Сущность реакции заключается в действии металлического натрия на гологенопроизводные (алкилгалогениды). Например:
Например:
 СН3 – СН2 J
СН3 – СН2 J
 1) Крекинг. При температуре более 4000С происходит разрыв С С связи. При этом получаются более простые насыщенные и ненасыщенные углеводороды.
1) Крекинг. При температуре более 4000С происходит разрыв С С связи. При этом получаются более простые насыщенные и ненасыщенные углеводороды. СН3 –СН2 – СН2 СН2 – СН3 ¾¾®СН3–СН2 –СН3+СН2=СН2 алкан алкен
СН3 –СН2 – СН2 СН2 – СН3 ¾¾®СН3–СН2 –СН3+СН2=СН2 алкан алкен 2) Сплавление солей одноосновных карбоновых кислот с щелочами.
2) Сплавление солей одноосновных карбоновых кислот с щелочами.
 О О
О О
 в) СН3 – СН2 – СН2 – С
в) СН3 – СН2 – СН2 – С
 Реакции замещения, разрыв С Н.
Реакции замещения, разрыв С Н. Cl Cl ¾® 2Сl · (1)
Cl Cl ¾® 2Сl · (1)


