Распад пероксида водорода в водном растворе Н2О2 = = Н2О +  О2 – пример гомогенной каталитической реакции, ускоряемый ионами CrО42–, Cr2О72–, WО42–, МоО42–, Fe2+, Fe3+ и др. Указанные ионы образуют с пероксидом водорода промежуточные соединения, которые распадаются с выделением кислорода; последним процессом определяется кинетика всей реакции. В ряде случаев удалось выделить промежуточные продукты гомогенного каталитического распада пероксида водорода, разлагаемые по мономолекулярному или бимолекулярному путям. Так, при катализе ионом CrО42– могут образоваться активные промежуточные формы CrО62– и CrО52–. Порядок реакции увеличивается с ростом температуры.
О2 – пример гомогенной каталитической реакции, ускоряемый ионами CrО42–, Cr2О72–, WО42–, МоО42–, Fe2+, Fe3+ и др. Указанные ионы образуют с пероксидом водорода промежуточные соединения, которые распадаются с выделением кислорода; последним процессом определяется кинетика всей реакции. В ряде случаев удалось выделить промежуточные продукты гомогенного каталитического распада пероксида водорода, разлагаемые по мономолекулярному или бимолекулярному путям. Так, при катализе ионом CrО42– могут образоваться активные промежуточные формы CrО62– и CrО52–. Порядок реакции увеличивается с ростом температуры.
CrО62– = CrО42– + О2 мономолекулярный распад.
2CrО52– = 2 CrО42– + О2 бимолекулярный распад.
В реакционный сосуд 1 налейте 8 мл раствора катализатора 0,25н К2СrO4 и поместите его в термостат 4 (рис.4.5). Уровень воды в бюретке 2 установите на нулевом делении или около него. Проверьте прибор на герметичность. После 10 мин. термостатирования при заданной температуре в реакционный сосуд прилейте 0,5 мл Н2О2 (20%). Раствор перемешайте встряхиванием, реакционный сосуд закройте пробкой и поставьте в термостат. Кран вверху бюретки держите открытым около 1 мин (для вытеснения воздуха), затем его закройте. Установите одинаковые уровни воды в бюретке и уравнительном сосуде 3, чтобы привести давление в приборе к атмосферному.
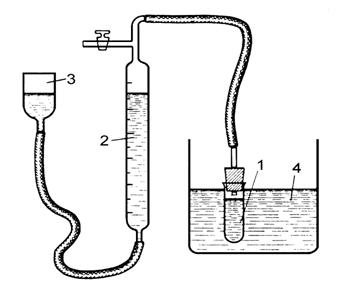
Рис. 4.5. Схема установки для изучения скорости
разложения H2O2 газометрическим методом
Запишите уровень воды в бюретке и отметьте время. Далее отмечайте время от начала реакции, за которое вытесняется 1 мл воды в бюретке, приводя давление в приборе к атмосферному при каждом измерении. Данные занесите в таблицу.
Уравнение реакции Н2О2 = Н2О + 1/2 О2
Температура опыта _________________
Катализатор _______________________
| №
изм.
| Время от начала реакции
в с. │ в мин.
| Объем выделившегося
газа, V t
| V¥ – V t
| lg(V¥ – V t)
|
Включите водяную баню. После двенадцати-четырнадцати замеров реакционный сосуд поместите в нее и держите до полного разложения Н2О2. Далее реакционный сосуд перенесите в термостат, выдержите в нем несколько минут для охлаждения до температуры термостата и при равенстве уровней воды в бюретке и уравнительном сосуде замерьте уровень воды в бюретке и запишите в таблицу.
1. По опытным данным постройте график зависимости логарифма разности объемов кислорода от времени
lg(V ¥ – Vt) = f(t),
где V ¥ – объем кислорода, выделившегося при полном разложении Н2О2 (определяется как разность уровней в бюретке в момент, принятый за начало реакции, и после кипячения Н2О2 до полного разложения).
На оси абсцисс откладывайте время в минутах. Сделайте вывод о порядке реакции.
2. Произведите расчет величины константы скорости реакции графически по

и по кинетическому уравнению реакции первого порядка, где концентрации заменяются величинами им пропорциональными, т.е. разностью объемов кислорода при t в районе 6‑го – 7-го измерений (если реакция 1 порядка)
 .
.
3. Зная константу скорости, вычислите энергию активации в Дж · моль–1 по уравнению
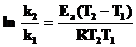 , R = 8,314 Дж · К–1 · моль–1.
, R = 8,314 Дж · К–1 · моль–1.
Значения k2 и T2 спросите у преподавателя.
4. Рассчитайте предэкспоненциальный фактор из уравнения Аррениуса:
 или
или 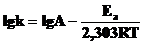 .
.
Работа должна содержать график lg(V ¥ – V t ) =f (t), подробные расчеты k, Ea, А.



 О2 – пример гомогенной каталитической реакции, ускоряемый ионами CrО42–, Cr2О72–, WО42–, МоО42–, Fe2+, Fe3+ и др. Указанные ионы образуют с пероксидом водорода промежуточные соединения, которые распадаются с выделением кислорода; последним процессом определяется кинетика всей реакции. В ряде случаев удалось выделить промежуточные продукты гомогенного каталитического распада пероксида водорода, разлагаемые по мономолекулярному или бимолекулярному путям. Так, при катализе ионом CrО42– могут образоваться активные промежуточные формы CrО62– и CrО52–. Порядок реакции увеличивается с ростом температуры.
О2 – пример гомогенной каталитической реакции, ускоряемый ионами CrО42–, Cr2О72–, WО42–, МоО42–, Fe2+, Fe3+ и др. Указанные ионы образуют с пероксидом водорода промежуточные соединения, которые распадаются с выделением кислорода; последним процессом определяется кинетика всей реакции. В ряде случаев удалось выделить промежуточные продукты гомогенного каталитического распада пероксида водорода, разлагаемые по мономолекулярному или бимолекулярному путям. Так, при катализе ионом CrО42– могут образоваться активные промежуточные формы CrО62– и CrО52–. Порядок реакции увеличивается с ростом температуры.

 .
.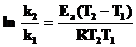 , R = 8,314 Дж · К–1 · моль–1.
, R = 8,314 Дж · К–1 · моль–1. или
или 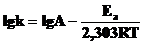 .
.


