Собственно изготовление мазей включает несколько последовательных стадий: плавление, растворение, диспергирование, при необходимости эмульгирование, упаковку, оформление.
С увеличением дисперсности лекарственных веществ возрастает их удельная поверхность, что увеличивает поверхность контакта с кожей и слизистыми оболочками организма, а значит и биологическую доступность. Поэтому основной технологической задачей при приготовлении мазей является превращение мазевых компонентов в максимально однообразную систему, имеющую достаточную степень устойчивости, с равномерным распределением по всей ее массе лекарственных веществ. Кроме того, к мазям предъявляется такие требования, как отсутствие механических включений, соответствие концентрации лекарственного вещества и массы мази выписанным в рецепте: микробиологическая чистота, т. е. в 1 г или в 1 мл суммарное содержание аэробных бактерий и грибов не более 100, энтеробактерий и некоторых других грамотрицательных бактерий не более 10, При экстемпоральном изготовлении, в случае отсутствия указания в рецепте, основу подбирают сучетом физико-химической совместимости компонентов мази. При отсутствии в рецепте точных указаний о концентрации мазей их, согласно указанию Фармакопеи, готовят с содержанием 10% лекарственного вещества, если только не имеется специальных утвержденных официальных прописей и лекарственные вещества не относятся к списку А и Б. В последнем случае, указание их концентрации обязательно. Изготовление мазей в условиях аптек складывается из подготовительной работы и основных технологических стадий. В подготовительную работу входит также выявление по нормативно-технической документации состава мазей. Выбор способа приготовления той или иной мази зависит от физико-химических свойств лекарственных веществ и применяемой мазевой основы.
Подбор основы для изготовления мази осуществляют в соответствии с прописью рецепта и (или) соответствующей нормативной документацией. Перед началом работы производят подбор вспомогательного и укупорочного материала; подбирают банки или флаконы с натягиваемыми или навинчивающимися крышками с учетом физико-химических свойств лекарственных веществ и массы мази. Рационально отпускать мази в металлических или пластмассовых тубах. Кроме того, с учетом массы мази подбирают ступку и пестик соответствующих размеров.
Взвешивание компонентов мазевой основы осуществляют в зависимости от физико-химических свойств на специальных тарирных весах.
Взвешивание лекарственных веществ осуществляют в зависимости от физико-химических свойств и количества — отвешивают на ручных или тарирных весах. Лекарственные вещества вводят в основу в растворенном или тонкодисперсном состоянии. Это способствует повышению фармакологического эффекта мази. В зависимости от физико-химических свойств веществ и характера основы, лекарственные вещества предварительно растворяют в основе или в одном из ее компонентов (получают гомогенные мази); растворяют в минимальном количестве воды (даже если мазевая основа гидрофобна; однако, если мазь дерматологическая, не растворяют в воде резорцин, цинка сульфат); измельчают сначала по правилам измельчения порошков, а затем — в присутствии вспомогательной жидкости, близкой по свойствам к основе (лучше добавление вспомогательной жидкости производить в количестве 40—60% от массы диспергируемого вещества — правило Дерягина); сухие и густые экстракты растирают со спирто-водоглицериновой смесью (13:6).
Введение лекарственных веществ в мазевые основы. При введении лекарственных веществ в мазевые основы необходимо руководствоваться определенными правилами с учетом их физико-химических свойств:
1) лекарственные вещества, легкорастворимые в мазевой основе, жирах и жирных маслах, предварительно растирают с небольшим количеством масла или растворяют при нагревании на водяной бане в части основы, а затем прибавляют остальное количество ее до требуемой массы;
2) лекарственные вещества, легкорастворимые в воде, смешивают с основой, предварительно растворив их в минимальном количестве воды;
3) лекарственные вещества, нерастворимые или труднорастворимые в основах,предварительно превращают в мельчайший порошок, растирают с половинным количеством родственной основе жидкости (с вазелиновым, жирным маслом или водой) или с частью расплавленной основы, а затем прибавляют остальное количество основы до требуемой массы;
4) лекарственные вещества, прописанные в мазях в больших количествах (более 25%), растирают в тонкий порошок и тщательно смешивают с предварительно расплавленной основой. Помимо перечисленных правил, существуют дополнительные указания, относящиеся к способам введения некоторых лекарственных веществ в мазевые основы:
1) резорцин, пирогаллол и цинка сульфат прибавляют к мазям (кроме глазных) в виде мельчайших порошков после растирания их с небольшим количеством жирного или вазелинового масла, но без растворения или растирания с водой. Введение этих веществ в растворенном в воде виде (а они растворимы в воде) значительно усиливает их всасываемость, что сопровождается выраженным токсическим воздействием на организм;
2) сухие и густые экстракты, а также опий предварительно растирают с равным количеством спиртоводоглицериновой смеси (1:3:6);
3) летучие вещества вводят в состав мазей в последнюю очередь при температуре не выше 40°С;
4) бентонитовые смеси (основы из глинистых минералов), не применяют при изготовлении мазей с лекарственными веществами, являющимися в растворе электролитами.
Кроме того, существует еще несколько правил введения лекарственных веществ:
1) при использовании сплава компонентов основы или их раствора лекарственные вещества смешивают с теплой основой;
2) при изготовлении паст лекарственные вещества смешивают с расплавленной основой, перемешивая до полного охлаждения массы;
3) при эмульгировании гидрофильных жидкостей используют ланолин безводный, однако лучше использовать его в смеси с вазелином, который понижает липкость безводного ланолина и таким образом облегчает эмульгирование;
4) при приготовлении мази на безводной основе лекарственные вещества растворяют в минимальном количестве воды, а затем эмульгируют равной массой безводного ланолина. Смешивание лекарственных веществ производят обычно в ступке.
Туда же добавляют частями основу, энергично перемешивая до образования однородной массы. При этом необходимо периодически 3—4 раза снимать массу целлулоидным скребком со стенок ступки и головки пестика.
Оформление паспорта письменного контроля (ППК)
Осуществляется после изготовления мази. При этом название и количество взятых ингредиентов мази записываются в порядке введения их в мазь, указывается также общее количество мази. На обороте ППК необходимо выполнить расчеты. Во-первых, определяют массу каждого ингредиента прописи (т. е. лекарственного вещества, основы или
50компонентов основы). Во-вторых, рассчитывают общую массу мази и процентное содержание в ней лекарственных веществ (в основном для мазей суспензионного, реже эмульсионного типа). В-третьих, рассчитывают количество вспомогательной жидкости для измельчения или растворения прописанных лекарственных веществ. При этом необходимо учитывать водопоглощающую способность основы и следить, чтобы количество дополнительно вводимых жидкостей не превышало норму допустимого отклонения в массе мази. Собственно изготовление мазей включает несколько последовательных стадий: плавление, растворение, диспергирование, при необходимости эмульгирование, упаковку, оформление. Кроме того, осуществляется контроль отдельных стадий (полноты растворения, однородности смешивания и т. д.), а также оценка готовой мази по технологическим показателям качества. В условиях аптеки вещества, входящие в состав мазей-сплавов, а также мазевые основы расплавляют на водяной бане в фарфоровых выпарительных чашках или с помощью лампы инфракрасного излучения. Растирание, растворение лекарственных веществ и их смешивание с мазевыми основами осуществляют в фарфоровых ступках с помощью пестика из того же материала. Фарфоровую чашку и ступку с пестиком следует подбирать соответствующей величины с учетом количества мази. Если не придерживаться этого принципа, то в процессе приготовления мази возникают некоторые затруднения.
При изготовлении большого количества мази в маленькой ступке трудно смешать ингредиенты и достигнуть однородности мази; приготовление же малого количества мази в большой ступке приводит к значительным потерям препарата.
Ступку с мазью для предохранения от попадания пыли и микроорганизмов из воздуха накрывают стеклянной или пластмассовой пластинкой.
При взвешивании мазевой основы и переносе ее в ступку обычно пользуются шпателями из нержавеющей стали, пластмассы, рога, фарфора.
В зависимости от химических свойств веществ, входящих в состав мази, и количества мази берут шпатель соответствующего размера, изготовленный из индифферентного по отношению к компонентам мази материала.
Например, при изготовлении мазей, содержащих йод, соли тяжелых металлов (соли ртути), салициловую кислоту, дубильные и некоторые другие вещества, взаимодействующие с металлом, нельзя пользоваться металлическим шпателем.
Для очищения ступки, пестика, перенесения мази в отпускную банку используют целлулоидную пластинку.
Возьми: Мази левомицетиновой 0,5%-10,0
Смешай, чтобы получилась мазь.
Дай. Обозначь. Закладывать за нижнее веко 4 раза в день
Паспорт
Левомицетина 0,05
Ланолина безводного 3,8 г
Вазелина 5, 7 гОбщая масса 10,00 г
В асептических условиях в стерильную ступку помещают 0,05 г левомицетина, растирают и смешивают с несколькими каплями стерильного масла вазелинового, вазелином и безводным ланолином, добавляя их частями. Мазь переносят в стерильную банку с навинчиваемой крышкой. Оформляют этикеткой «Глазная мазь». «Хранить в прохладном и защищ. от света месте.
ппк л
Chloramphenicoli 0,05/ I
Olei Vaselini 5 gt /^ Vaselini 3,8 •W Lanolini 5.7 ^
Jm = io,oj
СрошЖуътС. хр. - 10 дней в прохл. защищ. от света месте.
Вопрос 3. Flores Chamomillae ■ — цветки ромашки (Chamomillae flos — ромашки цветок)
Ромашка аптечная - Camomilla recutita Сем. сложноцветных - Compositae
Цветками в фармацевтической практике называют лекарственное сырье, представляющее
собой высушенные отдельные цветки или соцветия, а также их части. Цветки собирают
обычно в начале цветения, некоторые в фазу бутонизации.
Химический состав. Цветки ромашки аптечной содержат 0,2-0,8 % эфирного масла синего
цвета. Главный компонент его — хамазулен (около 7 %). Селекционные сорта содержат
эфирного масла до 1 %, хамазулена в масле — более 10 %. Кроме хамазулена в масле
содержатся другие сесквитерпеноиды (до 50%) — фарнезен, бизаболол, биза-бололоксиды А
и В, монотерпен мир-цен и др.
В цветках найдено значительное количество флавоноидов, производных апигенина,
лютеолина и кверцетина, обладающих противовоспалительными и антивирусными
свойствами

Рис. 29. Цветки (корзинки) ромашки аптечной и пахучей и их примеси:
Внешние признаки. Цельные и частично осыпавшиеся цветочные корзинки полушаровидной или конической формы, в поперечнике 4-8 мм, без цветоносов или с остатками их не длиннее 3 см. Обертка корзинки многорядная, из черепитчато расположенных листочков. Ложе соцветия коническое, голое, мелкоямчатое, полое. Цветки краевые — ложноязычковые, срединные — трубчатые. Цвет краевых цветков — белый, срединных — желтый, обертки -— желтовато-зеленый. Запах сильный, приятный. Вкус пряный, горьковатый, слегка слизистый.
Числовые показатели. Содержание эфирного масла не менее 0,3 %
Хранение. Хранят в сухих прохладных помещениях на стеллажах, отдельно от других видов сырья. Срок годности 1 год.
Использование. Поступает в аптеки в картонных пачках, а также в виде круглых брикетов. Цветки ромашки применяют в форме настоя или отвара, в составе желудочных и мягчительных сборов внутрь и наружно, используют для получения жидкого экстракта и препарата «Ротокан». Препараты назначают как противовоспалительное, спазмолитическое средство при спазмах кишечника, метеоризме, поносах, гастритах, колитах и других расстройствах деятельности желудочно-кишечного тракта. Наружно — для полоскания рта, для клизм, ванн. Сырье обладает антиаллергическим действием.
Хамазулен и его синтетические аналоги используют для лечения бронхиальной астмы, ревматизма, аллергических гастритов и колитов, экземы, ожогов рентгеновскими лучами.
Растение применяется в гомеопатии; входит в состав БАДов, обладающих противовоспалительным, спазмолитическим действием.
Вопрос 4. Отпуск лекарственных средств, оплата которых учитывается при определении суммы социального налогового вычета. С целью обеспечения доступности эффективных дорогостоящих ЛС всем группам населения Правительством РФ предусмотрены налоговые льготы. При налогообложении физических лиц налоговая база (доход, полученный в разных формах в налоговом периоде) может быть уменьшена на сумму так называемых социальных налоговых вычетов. К ним относится сумма, уплаченная налогоплательщиком при приобретении Л С. Постановлением Правительства РФ № 201 от 19.03.2001 утвержден Перечень медицинских услуг и дорогостоящих видов лечения в медицинских учреждениях РФ, лекарственных средств, суммы оплаты которых за счет собственных средств налогоплательщика учитываются при определении суммы социального налогового вычета. В этот перечень вошли анестетики и миорелаксанты; анальгетики, в том числе наркотические (морфин), нестероидные противовоспалительные препараты (ибупрофен); средства, применяемые для лечения аллергических реакций (кетотифен, хлоропирамин); средства, влияющие на центральную нервную систему (фенобарбитал), средства для лечения психотических расстройств (галоперидол, диазепам) и др. В перечень включены МНН ЛС, которые соответствуют Государственному реестру ЛС, утвержденномуприказом Минздрава России от 01.12.98 №01-29-15.
Совместно Минздравом России и Министерством Российской Федерации по налогам и сборам был принят приказ № 289/БГ-3-04/256 от 25.07.2001 г. о реализации данного постановления. Этим приказом, в частности, утвержден порядок выписки ЛС; назначенных лечащим врачом налогоплательщику и приобретенных им за счет собственных средств, размер стоимости которых учитывается при определении суммы социального налогового вычета.
Лекарственные средства выписываются врачом на рецептурных бланках по форме № 107/у. На одном рецептурном бланке можно выписать не более двух ЛС. В перечень, утвержденный постановлением № 201, наряду с ЛС, отпускаемыми по рецептам, включены ЛС, отпускаемые без рецепта врача на основании приказа Минздрава России от 19.07.99 № 287, и отдельные ЛС (психотропные и наркотические), которые выписываются только на специальных бланках и рецептах формы № 148/у-88. При этом в рецепте указывается одно из торговых наименований ЛС.
Лечащий врач выписывает пациенту рецепт в двух экземплярах, один из которых предъявляется в аптечную организацию для получения ЛС, другой представляется в налоговый орган РФ при подаче налоговой декларации по месту жительства налогоплательщика. На экземпляре рецепта, предназначенного для представления в налоговые органы РФ, лечащий врач в центре рецептурного бланка проставляет штамп «Для налоговых органов Российской Федерации, ИНН налогоплательщика», рецепт заверяется подписью и личной печатью врача, печатью учреждения здравоохранения (ее нет на рецепте в задании).
Экземпляр рецепта со штампом «Для налоговых органов Российской Федерации, ИНН налогоплательщика» остается на руках у налогоплательщика, оплатившего расходы по приобретению ЛС, назначенных лечащим врачом ему либо его супруге (супругу), его родителям, его детям в возрасте до 18 лет. В дальнейшем такой рецепт вместе с письменным заявлением, с товарным и кассовым чеками из аптечного учреждения, осуществившего отпуск ЛС, представляется в налоговый орган РФ по месту жительства.
Аптечным учреждениям независимо от организационно-правовой формы и. формы собственности категорически запрещается отпуск ЛС по рецептурным бланкам со штампом «Для налоговых органов Российской Федерации, ИНН налогоплательщика».
Контроль за выпиской ЛС, входящих в указанный перечень, осуществляется не реже одного раза в месяц заведующим отделением и руководителем учреждения здравоохранения.
Срок хранения рецепта в аптеке - 5 лет. срок действия рецепта - 2 мес.
Для большинства ЛС и других товаров аптечного ассортимента установлены предельные и гарантийные сроки годности. Предельные сроки годности — это максимально допустимые сроки, в течение которых товар имеет гарантированную безопасность.
В зависимости от пределов сроков годности продукция подразделяется на скоропортящуюся (от 6 ч до 96 ч), кратковременно хранящуюся (от 12 ч до 30 сут); длительно хранящуюся: с ограниченным сроком годности (в практике работыфармацевтических организаций ограниченным считается срок годности до 2 лет); без ограничения срока годности (может сохранять потребительские свойства в течение нескольких лет без их утраты).
Гарантийные сроки хранения и эксплуатации устанавливаются для ИМН. В течение этого периода изготовитель гарантирует соответствие ИМН требованиям стандартов при соблюдении условий транспортировки, хранения и эксплуатации. Другими словами, гарантируется продолжительность использования товаров в соответствии с назначением без существенной утраты потребительских свойств. Например, гарантийный срок хранения пузырей для льда составляет три с половиной года со дня изготовления. Гарантийный срок их эксплуатации составляет три года со дня продажи через розничную аптечную сеть, а в лечебных учреждениях — 18 мес со дня получения потребителем. Продлевать сроки годности не разрешается.
Особыми условиями поставки определены оставшиеся сроки годности, в соответствии с которыми ЛС должны отгружаться изготовителем с таким расчетом, чтобы к моменту их отгрузки оставалось не менее 80 % срока годности, обозначенного на этикетке, а для бактерийных препаратов, стоматологических и полимерных материалов — не менее 50 % срока годности.
При отгрузке указанной продукции со склада в розничную сеть и ЛПУ оставшийся срок годности должен быть не менее 60 %, а для бактерийных препаратов — не менее 40 % срока годности, обозначенного на этикетке.
Медицинская продукция со сроком годности более двух лет может отгружаться покупателю, если оставшийся срок годности составляет не менее 18 мес. Поставка продукции с меньшим сроком годности может производиться по согласию с покупателем, что определяется договорными условиями.
Оставшийся срок годности можно определить по номеру серии.
Серия — определенное количество однородного готового продукта, изготовленного за
При размещении на местах хранения (стеллажах, полках, шкафах) готовых лекарственных препаратов предъявляются следующие требования:
ЛС укладывают и устанавливают в оригинальной упаковке этикеткой (маркировкой) наружу;
рядом с ЛС прикрепляется стеллажная карта, в которой указывается наименование ЛС, серия, срок годности, количество. Карта отпечатывается на плотной бумаге. Она заводится на каждую вновь поступившую серию для контроля за своевременной ее реализацией.
Уничтожение лекарственных средств, пришедших в негодность
Порядок уничтожения ЛС в случаях, установленных законодательством, определен «Инструкцией о порядке уничтожения лекарственных средств, пришедших в негодность, лекарственных средств с истекшим сроком годности и лекарственных средств, являющихся подделками или незаконными копиями зарегистрированных в Российской Федерации лекарственных средств», утвержденной приказом Минздрава России от 15.12.02 № 382.
В соответствии с инструкцией изъятию из обращения и уничтожению в полном объеме Уничтожение особо ядовитых веществ. В настоящее время действуют Временные правила уничтожения сильнодействующих ядовитых веществ, пришедших в негодность, и меры личной и общественной безопасности и Инструкция по обезвреживанию и уничтожению сильнодействующих ядовитых веществ (1938). Правила уничтожения существуют для особо ядовитых веществ, таких, как мышьяковый и мышьяковистый ангидрид, сулема, фосфор (желтый), бруцин, никотин, стрихнин, синильная кислота и ее соли, хлорпикрин, сероуглерод. Необходимость и порядок уничтожения указанных веществ устанавливаются специальным приказом. Факт уничтожения оформляется актом. Уничтожение данных веществ разрешается проводить только в присутствии представителя органов санитарно-эпидемиологического надзора и органов милиции. Предъявляются строгие требования к подготовке персонала, снабжению его спецодеждой и защитными приспособлениями, мерам по обеспечению первой помощи при возможных несчастных случаях и отравлениях и пр.
Способы уничтожения и обезвреживания выбираются в каждом отдельной случае в зависимости от количества уничтожаемого вещества и местных условий, в которых это уничтожение производится.
Уничтожение наркотических средств и психотропных веществ. Производится в соответствии с Инструкцией по уничтожению наркотических средств и психотропных веществ, входящих в списки II и III Перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации, дальнейшее использование которых в медицинской практике признано нецелесообразным, утвержденной приказом Минздрава России от 31.01.2002 № 26.
Наркотические средства и психотропные вещества, дальнейшее использование которых в медицинской практике признано нецелесообразным органами, осуществляющими их изъятие или конфискацию, подлежат уничтожению в полном объеме. Уничтожение осуществляется в следующих случаях: истек срок годности;
вещество подвергалось химическому или физическому воздействию, следствием которого стала непригодность, исключающая возможность восстановления или переработки;
неиспользованные наркотические средства, принятые от родственников умерших больных;
когда трудно определить, является ли препарат наркотическим средством или психотропным веществом;
конфискованное из незаконного оборота наркотическое средство или психотропное вещество, которое не может быть использовано в медицинских, научных или иных целях.
Уничтожение этих препаратов можно проводить только в унитарных предприятиях или учреждениях, имеющих лицензию на уничтожение наркотических средств и психотропных веществ. Если юридическое лицо не имеет такой лицензии, но осуществляет Деятельность с их оборотом, то в случае необходимости уничтожения указанных Л С заключается договор с ГУП (учреждением), имеющим лицензию на право уничтожения, куда Л С передаются по приемо-сдаточному акту.подлежат ЛС:
пришедшие в негодность; с истекшим сроком годности;
являющиеся подделками или незаконными копиями зарегистрированных в РФ ЛС, обнаруженные и конфискованные, в том числе таможенными органами при ввозе в РФ.
Уничтожение ЛС производится с соблюдением обязательных требований по охране окружающей среды. Для уничтожения ЛС органом исполнительной власти субъекта Федерации создается специальная комиссия. Уничтожаются ЛС в присутствии собственника или владельца ЛС. Конфискованные таможенными органами ЛС уничтожаются только предприятиями, имеющими лицензию, на специально оборудованных площадках и полигонах.
Жидкие лекарственные формы (растворы для инъекций в ампулах, в пакетах и во флаконах, в аэрозольных баллонах, микстуры, капли и т.д.) уничтожают путем раздавливания (ампулы) с последующим разведениям содержимого ампул, пакетов и флаконов водой в соотношении 1: 100 и сливом образующегося раствора в промышленную канализацию (в аэрозольных баллонах предварительно делаются отверстия).
Остатки ампул, аэрозольных баллонов, пакетов и флаконов вывозятся обычным порядком, как производственный или бытовой мусор.
Твердые лекарственные формы (порошки, таблетки, капсулы и т.д.), содержащие водорастворимые субстанции ЛС, после дробления до порошкообразного состояния разводятся водой в соотношении 1: 100. Образовавшаяся суспензия (или раствор) сливается в промышленную канализацию.
Твердые лекарственные формы (порошки, таблетки, капсулы и т.д.), содержащие субстанции Л С, не растворимые в воде, мягкие лекарственные формы (мази, суппозитории и т.д.), трансдермальные формы ЛС, а также фармацевтические субстанции уничтожаются путем сжигания.
Огнеопасные, взрывоопасные ЛС, радиофармацевтические препараты, а также ЛРС с повышенным содержанием радионуклидов уничтожаются в особых условиях по специальной технологии, имеющейся в распоряжении организации по уничтожению в соответствии с лицензией.
При уничтожении ЛС комиссией по уничтожению ЛС составляется акт, в котором указываются: дата, место уничтожения; место работы, должность, фамилия, имя, отчество лиц, принимавших Участие в уничтожении; основание для уничтожения; сведения о наименовании (с указанием лекарственной формы, дозировки, единицы измерения, серии) и количестве уничтожаемого ЛС, а также о таре или упаковке; наименование производителя ЛС; наименование владельца или собственника ЛС: способ уничтожения. Акт по уничтожению ЛС подписывается всеми членами комиссии по уничтожению ЛС и скрепляется печатью предприятия, которое осуществило уничтожение.
Ответственность за уничтожение Л С несут субъекты обращения в соответствии с законодательством Российской Федерации. 
a-D-Глюкоза Альдегидная форма e-D-Глюкоза
D-глюкозы
Глюкоза относится к моносахаридам. Моносахариды, являясь веществами с - двойственными функциями, вступают во многие реакции, характерные для спиртов и карбонильных соединений (альдегидов).
Белый мелкокристаллический порошок без запаха, сладкого вкуса. Удельное
вращение от +52 до +53° (10%-ный водный раствор), легко растворима в воде,
Реакция на восстанавливающие сахара. Цветная реакция с 0,5%-ным раствором хлорида трифенилтетразолия в присутствии раствора гидроксида натрия при нагревании. Выпадает красный осадок трифенилформазана:

При добавлении раствора сульфата меди и подщелачивании глюкоза образует комплексное соединение фиолетово-синего цвета. Этой реакцией одновременно доказывается наличие как гидроксильных, так и альдегидной групп, восстанавливающих медь (II) до Оксида меди (I) при стоянии. (j
X
CM,
i
К-с - о
•С
V
. О I
Р-ции на альдегидную группу 1. Р-ция «серебряного зеркала» 
Показателем качества углеводов является удельное вращение растворов, характеризующее их оптическую активность. Для установления удельного вращения глюкозу предварительно сушат при 100-105 °С до постоянной массы.
Измерение угла вращения глюкозы производят с помощью поляриметра после предварительного прибавлении к испытуемому раствору двух капель раствора аммиака. При этом ускоряется процесс мутаротацгш. Он связан с установлением равновесия в образовании двух эпигиеров: 64% а-О(+)-глюкозы и 36% p-D(+)- глюкозы. Это создает усредненное значение удельного вращения раствора глюкозы, равное +52,5° (ФС допускает 51,5-53,0°).
В условиях термической стерилизации растворов глюкозы для инъекций, вне зависимост! от присутствия стабилизатора,- происходит образование продуктов деструкции дезоксигексазонов, органических кислот, формальдегида, 5-оксиметилфурфурола. 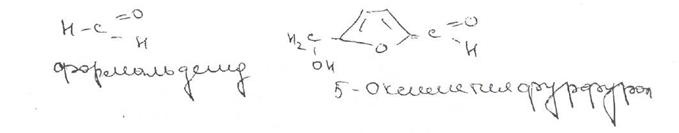
Количественное определение глюкозы можно выполнить различными методами.
Содержание глюкозы определяют иодометрическим методом, основанном на окислении альдегидной группы щелочными растворами иода до образования натриевой соли глюконовой кислоты:
СН2ОН(СНОН)4С\ -t 12 + 3NaOH—--> CH2OH(CHOH)4COONa + 2Nal + 2Н2О V
Один из титриметрических методов анализа моносахаридов основан на использовании реактива Фелинга (2-3 кратный избыток). Его добавляют к навеске точно отмеренное количество, а затем ио-дометрически устанавливают остаток неизрасходованного на окисление катиона меди (И).
Методика основана на восстановлении углеводами меди (II) до меди (I) из тартратного комплекса:

Избыток реактива Фелинга, содержащего ионы меди (П), восстанавливают иодидом в кислой среде и выделившийся иод титруют тиосульфатом натрия:
2Си2+ + 51" = 2Cul + h
Поляриметрический метод определения Сахаров основан на измерении угла вращения поляризованного света. Угол вращения а (в градусах), измеряемый на поляриметре, и удельное вращение [а]2 о связаны между собой уравнением: [а]о - 100 а /1*с. Зная удельное вращение, длину трубки I и измерив угол вращения, можно вычислить массовую долю с (%) по формуле:
С= а*100
ГЖХ-метод определения глюкозы используют после превращения её в летуча*. соединения (ацетаты сорбита или нитрил глюконовой кислоты).
Хранят лекарственные препараты углеводов в хорошо укупоренной таре при комнатной температуре.' Глюкоза в водных растворах при хранении окисляется. Следует также учитывать гигроскопичность глюкозы.
Применяют глюкозу при различных, заболеваниях сердца, печени, шоке, коллапсе вкачестве источника легко усвояемого организмом питания, улучшающего функции различных органов. Основные пути метаболизма D-глюкозы — гликолиз и аэробное окисление до углекислоты, воды и АТФ. Назначают глюкозу внутрь (по 0,5-1,0 г), внутривенно до 20-50 мл 40%-ного раствора, используют в фармацевтической практике в качестве наполнителей при приготовлении таблеток и порошков. КИСЛОТА АСКОРБИНОВАЯ (Acidum ascorbinicum).
Формы выпуска: порошок; таблетки по 0. 05 и 0. 1 г (для взрослых); таблетки по 0, 025 г (для детей); таблетки по 0, 025 г с глюкозой (в профилактических целях), 5 % и 10 % растворы в ампулах по 1 и 2 мл (в лечебных целях).
Раствор аскорбиновой кислоты для инъекций (5 %) содержит 2. 385 г натрия гидрокарбоната на каждые 5 г аскорбиновой кислоты; таким образом, при инъекции вводят натрия аскорбинат (рН 5 % раствора 6, 0 - 7, 0).
Хранение: порошок аскорбиновой кислоты - в хорошо укупоренной таре, предохраняющей от действия света, в сухом прохладном месте; таблетки и ампулы - в прохладном, защищенном от света месте.

По химическому строению кислота аскорбиновая представляет у-лактон-2,3-дегидро-Ь-гулоновой кислоты. Ввиду наличия в молекуле двойной связи возможно существование геометрических цис- и транс- изомеров кислоты аскорбиновой. Однако пока известен только один из них — цис-изомер. Два асимметрических атома углерода обусловливаю' существование четырех оптических изомеров. Все они получены синтетически, однако только /-изомер является физиологически активным.
Ascorbic acid — кислота аскорбиновая

у-лактон-23-дегидро-Ь-гулоновой кислоты
Белый кристаллический порошок без запаха, кислого вкуса. Т.пл. 190-193°С (с разложением). Удельное вращение от +22 до +24° (2%-ный водный раствор).
ГФ требует определить угол вращения (а) 2% раствора и рассчитать удельное вращение по формуле:
[а] ж0 = а* 100 1*С
где С -— концентрация раствора;
1 — длина трубки поляриметра = 1 дм.
Из-за нестойкости препарата при нагревании для определения Тпл его предварительно сушат при температуре 60 °С в течение 2 ч. Скорость подъема температуры - 5° в 1 мин (по той же причине).
Препарат поглощает свет в УФ-области спектра, что также используется при анализе подлинности.
Раствор кислоты аскорбиновой в буферном растворе (рН 7) имеет максимум поглощения при 265 нм. В кристаллической форме кислота аскорбиновая устойчива. В растворах под действием слабых окислителей различной природы она окисляется до дегидроаскорбиновои кислоты:

процесс этот — ооратимыи. кислотные свойства кислоте аскорбиновой придает наличие в молекуле двух енольных гидроксилов. В разбавленных растворах щелочей она ведет себя как одноосновная кислота. Разрыва лактонного цикла в этих условиях не происходит, а образуются нейтральные растворимые монозамещенные соли:

Эта реакция лежит в основе определения кислоты аскорбиновой методом кислотно-основного титрования.
Кислотные свойства кислоты аскорбиновой используют для испытания подлинности.
После добавления карбоната натрия в водном растворе происходит образованиеионизированной формы кислоты аскорбиновой. К полученной натриевой соли прибавляют сульфат железа (II). Появляется темно-фиолетовое окрашивание, обусловленное образованием аскорбината железа, исчезающее после добавления разведенной серной кислоты: Реактив — железа (II) сульфат, не обладающий свойствами окислителя:

Следует иметь в виду, что аскорбиновая кислота является лактоном и при действии сильных щелочей лактонное кольцо гидролизуется, а затем образуется фурфурол:

Восстановительные свойства. Окислители (AgNO;,. KMnO4. -Ь. FeCb, реактив Фелинга и др.) окисляют кислоту аскорбиновую до кислоты дикетоаскорбиновой.
При добавлении к ее раствору реактива Фелинга появляется оранжево-желтый осадок оксида меди (I).

При взаимодействии кислоты аскорбиновой с раствором нитрата серебра его катион - восстанавливается до металлического серебра (реакция образования «серебряного зеркала»): т
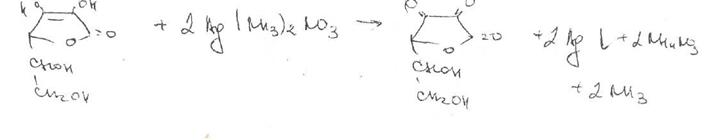
Восстановительными свойствами кислоты аскорбиновой обусловлено превращение окрашенного в синий цвет раствора 2,6-дихлорфенолиндофенола в бесцветное лейкооснование:

Восстановление сульфата меди (И) до меди (I) происходит при прибавлении к раствору кислоты аскорбиновой растворов сульфата меди и тиоцианата аммония. При этом выпадает 'белый осадок тиоцианата меди (I):

кислота аскороиновая дает положительную реакцию с хлоридом трифенилтриазилия подобно глюкозе

Количественно по ФС определяют кислоту аскорбиновую, используя в качестве титранта-окислителя 0.1 М раствор иодата калия в присутствии иодида калия: КЮз + 5KI + 6НС1 -> ЗЬ + 6КС1 + ЗИ2О

Избыток иода окрашивает крахмал в синий цвет. Окисление кислоты аскорбиновой иодом до дегидроаскорбиновой кислоты лежит в основе иодометрического определения. Титруют 0,1 М раствором иода без индикатора до образования стойкого желтого окрашивания или исполвзуют крахмал, который добавляют в конце титрования. Этот же химический процесс происходит при прямом иодхлорометрическом определении. Титруют 0,1 М раствором иодмонохлорида (индикатор крахмал). Прибавления иодида не требуется, так как он образуется при взаимодействии кислоты аскорбиновой с титрантом:
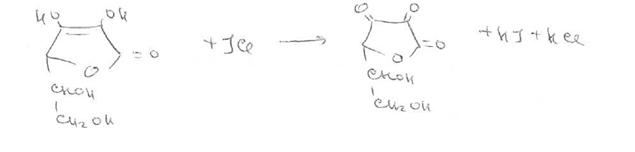
В эквивалентной точке выделяется иод, окрашивающий крахмал в синий цвет:
ICI + HI -->Ь + НС1
Так как глюкоза