Несколько слов об обратимости физических процессов
Физический (а в узком смысле термодинамический) процесс в некоторой системе тел (включающей твердые тела, жидкости, газы) является обратимым, если после того, как он был осуществлен, можно восстановить состояние, в котором система находилась до его начала. Если она не может вернуться в исходное состояние в конце процесса, то он является необратимым.
Обратимые процессы не встречаются в природе. Это идеализированная модель реальности, своеобразный инструмент ее исследования в физике. Примером такого процесса является цикл Карно. Идеальная тепловая машина - это модель реальной системы, реализующая процесс, носящий имя французского физика Сади Карно, который его впервые описал.

Что вызывает необратимость процессов?
Факторы, которые приводят к ней, включают в себя:
- тепловые потоки от источника тепла к потребителю при конечной разности температур между ними;
- неограниченное расширение газа;
- смешивание двух газов;
- трение;
- прохождение электрического тока через сопротивление;
- неупругая деформация;
- химические реакции.
Процесс необратим, если в наличии любой из этих факторов. Идеальный цикл Карно является обратимым процессом.
Внутренне и внешне обратимые процессы
Когда процесс осуществляется, факторы его необратимости могут находиться в рамках самой системы тел, а также в ее окрестности. Он называется внутренне обратимым, если система может быть восстановлена в то же самое состояние равновесия, в котором она находилась в его начале. При этом внутри нее не может быть факторов необратимости, пока длится рассматриваемый процесс.
Если факторы необратимости отсутствуют за пределами границ системы в процессе, то он называется внешне обратимым.
Процесс называется обратимым полностью, если он и внутренне, и внешне обратим.
Что такое цикл Карно?
В этом процессе, реализуемом идеальным тепловым двигателем, рабочее тело - нагретый газ - выполняет механическую работу за счет теплоты, получаемой из высокотемпературного теплового резервуара (нагревателя), а также отдает теплоту низкотемпературному тепловому резервуару (холодильнику).

·
·
·
·
·
Цикл Карно является одним из самых известных обратимых циклов. Он состоит из четырех обратимых процессов. И хотя подобные циклы недостижимы на практике, но они задают верхние пределы производительности реальных циклов. В теории показано, что данный прямой цикл осуществляет с предельно возможной эффективностью преобразование тепловой энергии (теплоты) в механическую работу.
Принципы Карно
Если процессы, которые составляют цикл Карно тепловой машины, являются обратимыми, то она носит наименование обратимой тепловой машины. В противном случае имеем ее необратимый вариант. На практике все тепловые двигатели являются таковыми, поскольку обратимых процессов не существует в природе.
Карно сформулировал принципы, являющиеся следствием второго начала термодинамики. Они выражаются следующим образом:
1. КПД необратимого теплового двигателя всегда меньше, чем у обратимого, работающего от тех же двух тепловых резервуаров.
2. КПД всех обратимых тепловых двигателей, работающих от тех же двух тепловых резервуаров, являются одинаковыми.
То есть КПД обратимой тепловой машины не зависит от используемого рабочего тела, его свойств, длительности цикла работы и типа теплового двигателя. Он является функцией только температуры резервуаров:
η = 1 - QL / QН = g (ТН, TL)
или
QH/QL = f (TH,TL),
где QL - теплота, передаваемая низкотемпературному резервуару, который имеет температуру TL; QH - теплота, передаваемая от высокотемпературного резервуара, который имеет температуру ТH; g, F - любые функции.
Тепловой двигатель Карно
Им называется такая тепловая машина, которая работает на обратимом цикле Карно. Тепловой КПД любой тепловой машины, обратимой или нет, определяется как
ηth = 1 - QL/QH,
где QL и QH являются количествами теплоты, передаваемыми в цикле низкотемпературному резервуару при температуре ТLи от высокотемпературного резервуара при температуре ТН соответственно. Для обратимых тепловых машин тепловой КПД может быть выражен через абсолютные температуры этих двух резервуаров:
ηth = 1 - TL/TH.
КПД теплового двигателя Карно является самым высоким КПД, которого может достигать тепловой двигатель, работая между высокотемпературным резервуаром при температуре ТН и низкотемпературным резервуаром при температуре ТL. Все необратимые тепловые двигатели, работающие между теми же двумя резервуарами, имеют более низкий КПД.
Обратный процесс
Рассматриваемый цикл является полностью обратимым. Его холодильный вариант может быть достигнут, если реверсировать все процессы, входящие в него. При этом работа цикла Карно используется для создания разности температур, т.е. тепловой энергии. Во время обратного цикла количество теплоты QL газ получает из низкотемпературного резервуара, а количество теплоты QH отдается им в высокотемпературный тепловой резервуар. Энергия Wnet,inтребуется, чтобы выполнить цикл. Она равна площади фигуры, ограниченной двумя изотермами и двумя адиабатами. PV-диаграммы прямого и обратного цикла Карно показаны на рисунке ниже.

Бытовой холодильник
Основная идея домашнего холодильника проста: он использует испарение хладагента для поглощения тепла от охлаждаемого пространства в холодильнике. Есть четыре основные части в любом холодильнике:
- Компрессор.
- Трубчатый радиатор вне холодильника.
- Расширительный клапан.
- Теплообменные трубы внутри холодильника.
Обратный цикл Карно приработы холодильника выполняется в следующем порядке:
- Адиабатическое сжатие. Компрессор сжимает пары хладагента, повышая их температуру и давление.
- Изотермическое сжатие. Высокотемпературный и сжатый компрессором пар хладагента рассеивает тепло в окружающую среду (высокотемпературный резервуар) при протекании через радиатор вне холодильника. Пары хладагента конденсируются (сжимаются) в жидкую фазу.
- Адиабатическое расширение. Жидкий хладагент протекает через расширительный клапан, чтобы уменьшить его давление.
- Изотермическое расширение. Холодный жидкий хладагент испаряется, когда он проходит через теплообменные трубы внутри холодильника. В процессе испарения его внутренняя энергия растет, и этот рост обеспечивается отбором тепла от внутреннего пространства холодильника (низкотемпературный резервуар), в результате чего оно охлаждается. Затем газ поступает в компрессор для сжатия снова. Обратный цикл Карно повторяется.
Обратимые и необратимые процессы. Теорема Карно
Процесс называется обратимым, если он может быть проведен в обратном направлении через те же промежуточные состояния, что и прямой процесс, причем во всех остальных телах никаких изменений произойти не должно. Если же это сделать невозможно, то процесс называется необратимым.
Обратимые процессы являются идеализацией реальных процессов. Все реальные процессы в той или иной степени являются необратимыми. Степень необратимости определяется значительностью или незначительностью изменений, которые должны произойти в окружающих систему телах, чтобы провести обратный процесс. Процесс можно считать обратимым, если есть принципиальная возможность изменить его направление на обратное путем бесконечно малого изменения внешних условий, в которых находится система.
Обратимый процесс обязательно должен быть квазистатическим. Напомним, что квазистатический – это бесконечно медленный процесс, последовательность состояний, бесконечно мало отличающихся от равновесных.
Укажем некоторые признаки принципиально необратимых процессов.
Необратимы процессы, протекающие с конечными скоростями, т.к. если скорость процесса имеет определенное, отличное от нуля значение, она должна входить в число внутренних параметров системы. Тогда состояния системы в прямом и обратном процессах не могут быть тождественными – они всегда будут отличаться знаками скоростей. Это различие исчезнет только в пределе, когда процесс идет квазистатически – бесконечно медленно.
Процессы, в которых существенную роль играют силы трения, также необратимы из-за неизбежного при этом перехода механической энергии во внутреннюю. Обратный процесс запрещен постулатом Томсона.
Необратимость процесса теплообмена при конечной разности температур тоже обусловлена вторым началом термодинамики (формулировка Клаузиуса).
Рассмотренный в § 8 цикл Карно является обратимым циклом, т.к. он не включает в себя принципиально необратимых процессов. Обратимость этого цикла будет существенно использована в доказательстве первой теоремы Карно:
машину а и используем потенциальную энергию поднятого груза, чтобы привести в действие машину в по обратному циклу (как холодильную машину). Проходя цикл Карно в обратном направлении, машина в будет забирать тепло у холодильника и отдавать тепло нагревателю. На рис. 10.1 схематически изображена работа машин а и в.
 Если для работы машины в по обратному циклу использовать всю энергию (Аа = Ав), накопленную в результате работы машины а, то количество тепла, переданное ею нагревателю Q 1 в = Ав /h в будет больше (из-за допущения, что h а >h в) количества тепла Q 1 a = Aa /h a, отобранного у нагревателя машиной а. В результате такой последовательной работы машин а и в, нагреватель получит положительное количество тепла Q = Q 1 в – Q 1 a . Такое же количество тепла Q = Q 2 в – Q 2 a , будет отобрано у холодильника. При этом никаких изменений в окружающих систему телах не произойдет. Таким образом, единственным результатом будет передача тепла от тела менее нагретого к телу более нагретому, что запрещено постулатом Клаузиуса. Поэтому предположение о том, что h а >h в неверно.
Если для работы машины в по обратному циклу использовать всю энергию (Аа = Ав), накопленную в результате работы машины а, то количество тепла, переданное ею нагревателю Q 1 в = Ав /h в будет больше (из-за допущения, что h а >h в) количества тепла Q 1 a = Aa /h a, отобранного у нагревателя машиной а. В результате такой последовательной работы машин а и в, нагреватель получит положительное количество тепла Q = Q 1 в – Q 1 a . Такое же количество тепла Q = Q 2 в – Q 2 a , будет отобрано у холодильника. При этом никаких изменений в окружающих систему телах не произойдет. Таким образом, единственным результатом будет передача тепла от тела менее нагретого к телу более нагретому, что запрещено постулатом Клаузиуса. Поэтому предположение о том, что h а >h в неверно.
Точно так же неверно предположение h в >h а. Чтобы убедиться в этом, надо заставить машину в проходить цикл Карно в прямом направлении, а машину а - в обратном. При этом направления стрелок на рис. 10.1 изменятся на противоположные. Повторяя предыдущие рассуждения, вновь придем к противоречию. Следовательно, h а = h в, и теорема Карно доказана.
Следует отметить, что если только одна из машин, рассматриваемых при доказательстве теоремы, является обратимой, то доказательство проходит лишь «наполовину». Если обратимый цикл Карно реализуется машиной в, то можно доказать ложность предположения h а >h в. Поменять машины местами теперь нельзя. Только обратимая машина в обратном цикле делает все так же, как в прямом, но с противоположным знаком. В таком случае можно сформулировать следующее положение, называемое второй теоремой Карно:
КПД любой машины, совершающей цикл между двумя тепловыми резервуарами, не может превосходить КПД машины, работающей по циклу Карно с теми же температурами нагревателя и холодильника.
Таким образом, цикл Карно имеет максимально возможный КПД при заданных температурах нагревателя и холодильника.
Цикл Карно (+ необратимый и обратимый цикл Карно)
Цикл Карно (linkisexternal) является обратимым циклическим процессом с двумя источниками теплоты, имеющими разные, но постоянные температуры.
Так как температуры источников тепла постоянные, а процессы получения и отдачи рабочим веществом тепла должны быть обратимыми, то эти процессы могут быть только изотермическими. При этом температура рабочего вещества в цикле должна, очевидно, меняться без теплообмена с окружающей средой, т.е. в адиабатных условиях. Поэтому цикл Карно состоит из двух обратимых изотермических и двух обратимых адиабатных процессов, чередующихся между собой.


Цикл Карно состоит из четырёх стадий:
1. Изотермическое расширение (на рисунке — процесс A>Б). В начале процесса рабочее тело имеет температуру TH TH, то есть температуру нагревателя. Затем тело приводится в контакт с нагревателем, который изотермически (при постоянной температуре) передаёт ему количество теплоты QH QH. При этом объём рабочего тела увеличивается.
2. Адиабатическое (изоэнтропическое) расширение (на рисунке — процесс Б>В). Рабочее тело отсоединяется от нагревателя и продолжает расширяться без теплообмена с окружающей средой. При этом его температура уменьшается до температуры холодильника.
3. Изотермическое сжатие (на рисунке — процесс В>Г). Рабочее тело, имеющее к тому времени температуру TX TX, приводится в контакт с холодильником и начинает изотермически сжиматься, отдавая холодильнику количество теплоты QX QX.
4. Адиабатическое (изоэнтропическое) сжатие (на рисунке — процесс Г>А). Рабочее тело отсоединяется от холодильника. При этом его температура увеличивается до температуры нагревателя.

КПД машины Карно

Из последнего выражения видно, что КПД тепловой машины Карно зависит только от температур нагревателя и холодильника. Кроме того, из него следует, что КПД может составлять 100 % только в том случае, если температура холодильника равна абсолютному нулю. Это невозможно, но не из-за недостижимости абсолютного нуля (этот вопрос решается только третьим началом термодинамики, учитывать которое здесь нет необходимости), а из-за того, что такой цикл или нельзя замкнуть, или он вырождается в совокупность двух совпадающих адиабат и изотерм.
Обратимый процесс может быть проведен в обратном порядке через те же состояния, что и при прямом ходе. Необратимые процессы сопровождаются изменениями окружающей среды. КПД =  В. Томсон: Невозможно осуществление цикла теплового двигателя без переноса некоторого количества теплоты от источника тепла с более высокой температурой к источнику с более низкой температурой. Для превращения тепла в работу необходим, кроме источника тепла, охладитель, т.е. температурный перепад. В периодическом процессе (цикле) только часть теплоты, за счет которой осуществляется цикл, может быть превращена в работу. В любом цикле нельзя перевести все подведенное тепло в работу.
В. Томсон: Невозможно осуществление цикла теплового двигателя без переноса некоторого количества теплоты от источника тепла с более высокой температурой к источнику с более низкой температурой. Для превращения тепла в работу необходим, кроме источника тепла, охладитель, т.е. температурный перепад. В периодическом процессе (цикле) только часть теплоты, за счет которой осуществляется цикл, может быть превращена в работу. В любом цикле нельзя перевести все подведенное тепло в работу.
Карно нашел КПД идеальной тепловой машины, она должна при работе использовать только изотермические и адиабатические процессы.
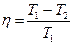 Цикл Карно́ — идеальный цикл тепловой машины.. Тепловая машина Карно, работающая по этому циклу, обладает максимальным КПД из всех машин, у которых максимальная и минимальная температуры осуществляемого цикла совпадает соответственно с максимальной и минимальной температурами цикла Карно.
Цикл Карно́ — идеальный цикл тепловой машины.. Тепловая машина Карно, работающая по этому циклу, обладает максимальным КПД из всех машин, у которых максимальная и минимальная температуры осуществляемого цикла совпадает соответственно с максимальной и минимальной температурами цикла Карно.
Одним из важных свойств цикла Карно является его обратимость: он может быть проведён как в прямом, так и в обратном направлении, при этом энтропия аддиабатически изолированной (без теплообмена с окружающей средой) системы не меняется
Круговые процессы (циклы). Цикл Карно.
Круговой процесс — процесс, при котором газ, пройдя через ряд состояний, возвращается в исходное.
Если круговой процесс на диаграмме P-V протекает по часовой стрелке, то часть тепловой энергии, полученной от нагревателя, превращается в работу. Так работает тепловая машина.
Если круговой процесс на диаграмме P-V протекает против часовой стрелки, то тепловая энергия передается от холодильника (тела с меньшей температурой) к нагревателю (телу с большей температурой) за счет работы внешней силы. Так работает холодильная машина.
|
| Коэффициент полезного действия тепловой машины равен отношению работы за цикл к полученной от нагревателя тепловой энергии  : :  . Холодильный коэффициент холодильной машины равен отношению тепловой энергии . Холодильный коэффициент холодильной машины равен отношению тепловой энергии  , отобранной от холодильника за цикл, к затраченной работе: , отобранной от холодильника за цикл, к затраченной работе: 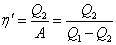 . .
|
Цикл Карно́ — идеальный термодинамический цикл. Тепловая машина Карно, работающая по этому циклу, обладает максимальным КПД из всех машин, у которых максимальная и минимальная температуры осуществляемого цикла совпадают соответственно с максимальной и минимальной температурами цикла Карно. Состоит из 2 адиабатических и 2 изотермических процессов.
Цикл Карно назван в честь французского военного инженера Сади Карно, который впервые его исследовал в 1824 году.
Одним из важных свойств цикла Карно является его обратимость: он может быть проведён как в прямом, так и в обратном направлении, при этом энтропияадиабатически изолированной (без теплообмена с окружающей средой) системы не меняется.
|
| Цикл Карно состоит из четырёх стадий: 1. Изотермическое расширение (на рисунке — процесс A→Б). Вначалепроцессарабочеетелоимееттемпературу, то есть температуру нагревателя. Затем тело приводится в контакт с нагревателем, который изотермически (при постоянной температуре) передаёт ему количество теплоты. При этом объём рабочего тела увеличивается. 2. Адиабатическое (изоэнтропическое) расширение (на рисунке — процесс Б→В). Рабочеетелоотсоединяетсяотнагревателяипродолжаетрасширятьсябезтеплообменасокружающейсредой. Приэтомеготемпературауменьшаетсядотемпературыхолодильника. 3. Изотермическое сжатие (на рисунке — процесс В→Г). Рабочеетело, имеющеектомувременитемпературу, приводитсявконтактсхолодильникоминачинаетизотермическисжиматься, отдаваяхолодильникуколичествотеплоты  . 4. Адиабатическое (изоэнтропическое) сжатие (на рисунке — процесс Г→А). Рабочеетелоотсоединяетсяотхолодильникаисжимаетсябезтеплообменасокружающейсредой. Приэтомеготемператураувеличиваетсядотемпературынагревателя. . 4. Адиабатическое (изоэнтропическое) сжатие (на рисунке — процесс Г→А). Рабочеетелоотсоединяетсяотхолодильникаисжимаетсябезтеплообменасокружающейсредой. Приэтомеготемператураувеличиваетсядотемпературынагревателя.
|
Вычисление совершаемой веществом работы, за единичный цикл Карно при постоянных не одинаковых температурах Т1 и Т2 от нагревателя и холодильника, можно вычислить с помощью расчета:
А = Q1 - Q2 = (Т1-Т2/T1) *Q1 Данная работа количественно приравнивается к площади АВСD с ограничивающими отрезками в виде изотерм и адиабат которые и создают данный цикл.
Теорема Карно (с выводом).
Из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей T1 и холодильников T2, наибольшим КПД обладают обратимые машины. При этом КПД обратимых машин, работающих при одинаковых температурах нагревателей и холодильников, равны друг другу и не зависят от природы рабочего тела, а определяются только температурами нагревателя и холодильника.
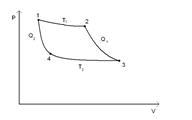
Для построения рабочего цикла использует обратимые процессы. Например, цикл Карно состоит из двух изотерм (1–2, 2-4) и двух адиабат (2-3, 4–1), в которых теплота и изменение внутренней энергии полностью превращаются в работу (рис. 19).

Рис. 19. Цикл Карно
Общее изменение энтропии в цикле: ΔS=ΔS12+ΔS23+ΔS34+ΔS41.
Так как мы рассматриваем только обратимые процессы, общее изменение энтропии ΔS=0.
Последовательные термодинамические процессы в цикле Карно:
| Процесс
| Работа
| Изменение энтропии
| Наблюдается
|
| Изотермическое расширение 1-2, T=const; V2>V1
| A12=Q1=(m/M)·RT1·ln(V2/V1)
| ΔS12=|Q1|/T1
| тело принимает теплоту
|
| Адиабатическое расширение 2-3, δQ=0; T2<T1
| A23=-(m/M)·CV(T2-T1)
| ΔS23=0
| охлаждение до T2
|
| Изотермическое сжатие 3-4, T=const; V3>V4
| A34=(m/M)·RT2·ln(V4/V3)=-Q2
| ΔS34=|Q2|/T2
| тело отдает теплоту
|
| Адиабатическое сжатие 4-1, δQ=0; T1<T2
| A41=-(m/M)·CV(T1-T2)=-A23
| ΔS41=0
| восстановление начального состояния p1, V1, T1
|
Общее изменение энтропии в равновесном цикле: ΔS=(|Q1|/T1)+0-(|Q2|/T2)+0=0⇒T2/T1=|Q2|/|Q1|,
поэтому: ηmax=1-(T2/T1) - максимальный КПД теплового двигателя.
Следствия:
1. КПД цикла Карно не зависит от рода рабочего тела.
2. КПД определяется только разницей температур нагревателя и холодильника.
3. КПД не может быть 100% даже у идеальной тепловой машины, так как при этом температура холодильника должна быть T2=0, что запрещено законами квантовой механики и третьим законом термодинамики.
4. Невозможно создать вечный двигатель второго рода, работающий в тепловом равновесии без перепада температур, т.е. при T2=T1, так как в этом случае ηmax=0.
II начало термодинамики.
Первое начало термодинамики, выражая закон сохранения и превращения энергии, не позволяет установить направление протекания термодинамических процессов. Кроме того, можно представить множество процессов, не противоречащих первому началу, в которых энергия сохраняется, а в природе они не осуществляются. Появление второго начала термодинамики связано с необходимостью дать ответ на вопрос, какие процессы в природе возможны, а какие нет. Второе начало термодинамики определяет направление протекания термодинамических процессов.
Используя понятие энтропии и неравенство Клаузиуса, второе начало термодинамики можно сформулировать как закон возрастания энтропии замкнутой системы при необратимых процессах: любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает.
Можно дать более краткую формулировку второго начала термодинамики: в процессах, происходящих в замкнутой системе, энтропия не убывает. Здесь существенно, что речь идет о замкнутых системах, так как в незамкнутых системах энтропия может вести себя любым образом (убывать, возрастать, оставаться постоянной). Кроме того, отметим еще раз, что энтропия остается постоянной в замкнутой системе только при обратимых процессах. При необратимых процессах в замкнутой системе энтропия всегда возрастает.
Формула Больцмана (2.134) позволяет объяснить постулируемое вторым началом термодинамики возрастание энтропии в замкнутой системе при необратимых процессах: возрастание энтропии означает переход системы из менее вероятных в более вероятные состояния. Таким образом, формула Больцмана позволяет дать статистическое толкование второго начала термодинамики. Оно, являясь статистическим законом, описывает закономерности хаотического движения большого числа частиц, составляющих замкнутую систему.
Укажем еще две формулировки второго начала термодинамики:
1) по Кельвину: невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу;
2) по Клаузиусу: невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
Можно довольно просто доказать эквивалентность формулировок Кельвина и Клаузиуса. Кроме того, показано, что если в замкнутой системе провести воображаемый процесс, противоречащий второму началу термодинамики в формулировке Клаузиуса, то он сопровождается уменьшением энтропии. Это же доказывает эквивалентность формулировки Клаузиуса (а следовательно, и Кельвина) и статистической формулировки, согласно которой энтропия замкнутой системы не может убывать.
В середине XIX в. возникла проблема так называемой тепловой смерти вселенной. Рассматривая Вселенную как замкнутую систему к применяя к ней второе начало термодинамики, Клаузиус свел его содержание к утверждению, что энтропия Вселенной должна достигнуть своего максимума. Это означает, что со временем все формы движения должны перейти в тепловую. Переход же теплоты от горячих тел к холодным приведет к тому, что температура всех тел во Вселенной сравняется, т. е. наступит полное тепловое равновесие и все процессы во Вселенной прекратятся – наступит тепловая смерть Вселенной. Ошибочность вывода о тепловой смерти заключается в том, что бессмысленно применять второе начало термодинамики к незамкнутым системам, например к такой безграничной в бесконечно развивающейся системе, как Вселенная.
Энтропия по Клаузиусу.
К макроскопическим параметрам термодинамической системы относятся давление, объём и температура. Однако существует ещё одна важная физическая величина, которую используют для описания состояний и процессов в термодинамических системах. Её называют энтропией.
Впервые это понятие ввёл в 1865 г. немецкий физик Рудольф Клаузиус. Энтропией он назвал функцию состояния термодинамической системы, определяющую меру необратимого рассеивания энергии.
Что же такое энтропия? Прежде чем ответить на этот вопрос, познакомимся с понятием «приведенной теплоты». Любой термодинамический процесс, проходящий в системе, состоит из какого-то количества переходов системы из одного состояния в другое. Приведенной теплотой называют отношение количества теплоты в изотермическом процессе к температуре, при которой происходит передача этой теплоты.
Q' = Q/T.
Для любого незамкнутого термодинамического процесса существует такая функция системы, изменение которой при переходе из одного состояния в другое равно сумме приведенныхтеплот. Этой функции Клаузиус дал название «энтропия» и обозначил её буквой S, а отношение общего количества теплоты ∆Q к величине абсолютной температуры Т назвал изменением энтропии.
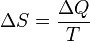
Обратим внимание на то, что формула Клаузиуса определяет не само значение энтропии, а только её изменение.
Что же представляет собой «необратимое рассевание энергии» в термодинамике?
Одна из формулировок второго закона термодинамики выглядит следующим образом: " Невозможен процесс, единственным результатом которого является превращение в работу всего количества теплоты, полученного системой ". То есть часть теплоты превращается в работу, а какая-то её часть рассеивается. Этот процесс необратим. В дальнейшем рассеиваемая энергия уже не может совершать работу. Например, в реальном тепловом двигателе рабочему телу передаётся не вся теплота. Часть её рассеивается во внешнюю среду, нагревая её.
В идеальной тепловой машине, работающей по циклу Карно, сумма всех приведенных теплот равна нулю. Это утверждение справедливо и для любого квазистатического (обратимого) цикла. И неважно, из какого количества переходов из одного состояния в другое состоит такой процесс.
Если разбить произвольный термодинамический процесс на участки бесконечно малой величины, то приведенная теплота на каждом таком участке будет равна δQ/T. Полный дифференциал энтропии dS = δQ/T.
Энтропию называют мерой способности теплоты необратимо рассеиваться. Её изменение показывает, какое количество энергии беспорядочно рассеивается в окружающую среду в виде теплоты.
В замкнутой изолированной системе, не обменивающейся теплом с окружающей средой, при обратимых процессах энтропия не изменяется. Это означает, что дифференциал dS = 0. В реальных и необратимых процессах передача тепла происходит от тёплого тела к холодному. В таких процессах энтропия всегда увеличивается (dS˃ 0). Следовательно, она указывает направление протекания термодинамического процесса.
Формула Клаузиуса, записанная в виде dS = δQ/T, справедлива лишь для квазистатических процессов. Это идеализированные процессы, являющиеся чередой состояний равновесия, следующих непрерывно друг за другом. Их ввели в термодинамику для того, чтобы упростить исследования реальных термодинамических процессов. Считается, что в любой момент времени квазистатическая система находится в состоянии термодинамического равновесия. Такой процесс называют также квазиравновесным.
Конечно, в природе таких процессов не существует. Ведь любое изменение в системе нарушает её равновесное состояние. В ней начинают происходить различные переходные процессы и процессы релаксации, стремящиеся вернуть систему в состояние равновесия. Но термодинамические процессы, протекающие достаточно медленно, вполне могут рассматриваться как квазистатические.
На практике существует множество термодинамических задач, для решения которых требуется создание сложной аппаратуры, создание давления в несколько сот тысяч атмосфер, поддержание очень высокой температуры в течение длительного времени. А квазистатические процессы позволяют рассчитать энтропию для таких реальных процессов, предсказать, как может проходить тот или иной процесс, реализовать который на практике очень сложно.
Обратимые и необратимые процессы. Тепловые машины и их КПД. Цикл Карно. Теоремы Карно.
Первое начало термодинамики. Круговые, обратимые и необратимые процессы. Тепловая машина Карно и ее кпд.
Первое начало термодинамики
Рассмотрим термодинамическую систему, для которой механическая энергия не изменяется, а изменяется лишь ее внутренняя энергия. Внутренняя энергия системы может изменяться в результате различных процессов, например совершения над системой работы или сообщения ей теплоты. Так, вдвигая поршень в цилиндр, в котором находится газ, мы сжимаем этот газ, в результате чего его температура повышается, т. е. тем самым изменяется (увеличивается) внутренняя энергия газа. С другой стороны, температуру газа и его внутреннюю энергию можно увеличить за счет сообщения ему некоторого количества теплоты — энергии, переданной системе внешними телами путем теплообмена (процесс обмена внутренними энергиями при контакте тел с разными температурами).
Таким образом, можно говорить о двух формах передачи энергии от одних тел к другим: работе и теплоте. Энергия механического движения может превращаться в энергию теплового движения, и наоборот. При этих превращениях соблюдается закон сохранения и превращения энергии; применительно к термодинамическим процессам этим законом и является первое начало термодинамики, установленное в результате обобщения многовековых опытных данных.
Допустим, что некоторая система (газ, заключенный в цилиндр под поршнем), обладая внутренней энергией U 1, получила некоторое количество теплоты Q и, перейдя в новое состояние, характеризующееся внутренней энергией U 2, совершила работу А над внешней средой, т. е. против внешних сил. Количество теплоты считается положительным, когда оно подводится к системе, а работа — положительной, когда система совершает ее против внешних сил. Опыт показывает, что в соответствии с законом сохранения энергии при любом способе перехода системы из первого состояния во второе изменение внутренней энергии D U=U 2– U 1 будет одинаковым и равным разности между количеством теплоты Q, полученным системой, и работой А, совершенной системой против внешних сил:
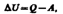
или

Уравнение (51.1) выражает первое начало термодинамики: теплота, сообщаемая системе, расходуется на изменение ее внутренней энергии и на совершение ею работы против внешних сил
Круговые, обратимые и необратимые процессы
Круговым процессом (или циклом) называется процесс, при котором система, пройдя через ряд состояний, возвращается в исходное. На диаграмме процессов цикл изображается замкнутой кривой (рис. 84). Цикл, совершаемый идеальным газом, можно разбить на процессы расширения (1 — 2) и сжатия (2 — 1) газа.

Прямой цикл используется в тепловых двигателях — периодически действующих двигателях, совершающих работу за счет полученной извне теплоты. Обратный цикл используется в холодильных машинах — периодически действующих установках, в которых за счет работы внешних сил теплота переносится к телу с более высокой температурой.
Термодинамический процесс называется обратимым, если он может происходить как в прямом, так и в обратном направлении, причем если такой процесс происходит сначала в прямом, а затем в обратном направлении и система возвращается в исходное состояние, то в окружающей среда и в этой системе не происходит никаких изменений. Всякий процесс, не удовлетворяющий этим условиям, является необратимым.
Любой равновесный процесс является обратимым. Обратимость равновесного процесса, происходящего в системе, следует из того, что се любое промежуточное состояние есть состояние термодинамического равновесия; для него «безразлично», идет процесс в прямом или обратном направлении. Реальные процессы сопровождаются диссипацией энергии (из-за трения, теплопроводности и т. д.), которая нами не обсуждается. Обратимые процессы — это идеализация реальных процессов. Их рассмотрение важно по двум причинам: 1) многие процессы в природе и технике практически обратимы; 2) обратимые процессы являются наиболее экономичными; имеют максимальный термический коэффициент полезного действия, что позволяет указать пути повышения к. п. д. реальных тепловых двигателей.
Основываясь на втором начале термодинамики, Карно вывел теорему, носящую теперь его имя: из всех периодически действующих тепловых машин, имеющих одинаковые температуры нагревателей и холодильников, наибольшим кпд обладают обратимые машины, при этом кпд обратимых машин, работающих при одинаковых температурах нагревателей и холодильников, равны друг другу и не зависят от конструкции машины.Цикл, изученный Карно, является самым экономичным и представляет собой круговой процесс, состоящий из двух изотерм и двух адиабат.рассмотрим прямой цикл Карно, в котором в качестве рабочего тела используется идеальный газ, заключенный в сосуд с подвижным поршнем. Определим его кпд. 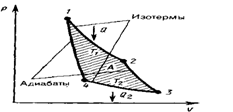
Цикл Карно схематически изображен на рис.55, где изотермическое расширение и сжатие задано соответственно кривыми 1-2 и 3-4, а адиабатические расширение и сжатие - кривыми 2-3 и 4-1.
 -кпд
-кпд
для цикла Карно кпд действительно определяется только температурой нагревателя холодильника.
Обратимые и необратимые процессы. Тепловые машины и их КПД. Цикл Карно. Теоремы Карно
•Обратимый процесс (равновесный) — термодинамический процесс, который может проходить как в прямом, так и в обратном направлении, проходя через одинаковые промежуточные состояния, причём си








 Если для работы машины в по обратному циклу использовать всю энергию (Аа = Ав), накопленную в результате работы машины а, то количество тепла, переданное ею нагревателю Q 1 в = Ав /h в будет больше (из-за допущения, что h а >h в) количества тепла Q 1 a = Aa /h a, отобранного у нагревателя машиной а. В результате такой последовательной работы машин а и в, нагреватель получит положительное количество тепла Q = Q 1 в – Q 1 a . Такое же количество тепла Q = Q 2 в – Q 2 a , будет отобрано у холодильника. При этом никаких изменений в окружающих систему телах не произойдет. Таким образом, единственным результатом будет передача тепла от тела менее нагретого к телу более нагретому, что запрещено постулатом Клаузиуса. Поэтому предположение о том, что h а >h в неверно.
Если для работы машины в по обратному циклу использовать всю энергию (Аа = Ав), накопленную в результате работы машины а, то количество тепла, переданное ею нагревателю Q 1 в = Ав /h в будет больше (из-за допущения, что h а >h в) количества тепла Q 1 a = Aa /h a, отобранного у нагревателя машиной а. В результате такой последовательной работы машин а и в, нагреватель получит положительное количество тепла Q = Q 1 в – Q 1 a . Такое же количество тепла Q = Q 2 в – Q 2 a , будет отобрано у холодильника. При этом никаких изменений в окружающих систему телах не произойдет. Таким образом, единственным результатом будет передача тепла от тела менее нагретого к телу более нагретому, что запрещено постулатом Клаузиуса. Поэтому предположение о том, что h а >h в неверно.



 В. Томсон: Невозможно осуществление цикла теплового двигателя без переноса некоторого количества теплоты от источника тепла с более высокой температурой к источнику с более низкой температурой. Для превращения тепла в работу необходим, кроме источника тепла, охладитель, т.е. температурный перепад. В периодическом процессе (цикле) только часть теплоты, за счет которой осуществляется цикл, может быть превращена в работу. В любом цикле нельзя перевести все подведенное тепло в работу.
В. Томсон: Невозможно осуществление цикла теплового двигателя без переноса некоторого количества теплоты от источника тепла с более высокой температурой к источнику с более низкой температурой. Для превращения тепла в работу необходим, кроме источника тепла, охладитель, т.е. температурный перепад. В периодическом процессе (цикле) только часть теплоты, за счет которой осуществляется цикл, может быть превращена в работу. В любом цикле нельзя перевести все подведенное тепло в работу.
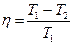 Цикл Карно́ — идеальный цикл тепловой машины.. Тепловая машина Карно, работающая по этому циклу, обладает максимальным КПД из всех машин, у которых максимальная и минимальная температуры осуществляемого цикла совпадает соответственно с максимальной и минимальной температурами цикла Карно.
Цикл Карно́ — идеальный цикл тепловой машины.. Тепловая машина Карно, работающая по этому циклу, обладает максимальным КПД из всех машин, у которых максимальная и минимальная температуры осуществляемого цикла совпадает соответственно с максимальной и минимальной температурами цикла Карно. :
:  . Холодильный коэффициент холодильной машины равен отношению тепловой энергии
. Холодильный коэффициент холодильной машины равен отношению тепловой энергии  , отобранной от холодильника за цикл, к затраченной работе:
, отобранной от холодильника за цикл, к затраченной работе: 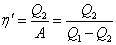 .
.
 . 4. Адиабатическое (изоэнтропическое) сжатие (на рисунке — процесс Г→А). Рабочеетелоотсоединяетсяотхолодильникаисжимаетсябезтеплообменасокружающейсредой. Приэтомеготемператураувеличиваетсядотемпературынагревателя.
. 4. Адиабатическое (изоэнтропическое) сжатие (на рисунке — процесс Г→А). Рабочеетелоотсоединяетсяотхолодильникаисжимаетсябезтеплообменасокружающейсредой. Приэтомеготемператураувеличиваетсядотемпературынагревателя.

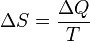
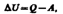



 -кпд
-кпд


