для студентов направления подготовки бакалавров
11.03.04 «Электроника и наноэлектроника», направленности
«Микроэлектроника и твердотельная электроника»
очной формы обучения

Воронеж 2017
Составители: канд. физ.-мат. наук Е.П. Николаева,
С.О. Николаева
УДК 541.1
Методические указания к выполнению практических занятий по дисциплине «Физическая химия материалов и процессов электронной техники» для студентов направления подготовки 11.03.04 «Электроника и наноэлектроника», направленности «Микроэлектроника и твердотельная электроника» очной формы обучения / ФГБОУ ВО «Воронежский государственный технический университет»; сост. Е.П. Николаева, С.О. Николаева. Воронеж, 2017. 59 с.
Методические указания включают основные методы расчета химических равновесий, определения степени завершенности и направления химической реакции, а также определения зависимости теплового эффекта химической реакции от температуры. Приведены примеры расчета и библиографический список.
Издание подготовлено в электронном виде и содержится в файле «Му пр ФХ.pdf».
Табл. 4. Ил. 11. Библиогр.: 4 назв.
Рецензент канд. техн. наук, доц. Н.Н. Кошелева
Ответственный за выпуск зав. кафедрой
д-р физ.-мат. наук, проф. С.И. Рембеза
Издается по решению редакционно-издательского совета Воронежского государственного технического университета
© ФГБОУ ВО «Воронежский государственный
технический университет», 2017
Определение зависимости теплового
Эффекта химической
Реакции от температуры
Цель работы
1. Изучить основные законы термохимии: закон Гесса, следствия закона Гесса, закон Кирхгофа.
2. Изучить методику определения теплового эффекта химической реакции.
3. Определить температурную зависимость теплового эффекта заданной химической реакции в заданном интервале температур.
Теоретическая часть
Для реакции
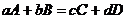 (1.1)
(1.1)
температурную зависимость теплового эффекта химической реакции 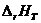 определяем по закону Кирхгофа
определяем по закону Кирхгофа
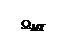
 (1.2)
(1.2)
или
 , (1.3)
, (1.3)
где 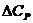 ,
, 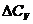 – изменения молярной теплоемкости в результате протекания процесса при P = const или V = const.
– изменения молярной теплоемкости в результате протекания процесса при P = const или V = const.
Для реакции (1.1)
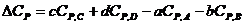 (1.4)
(1.4)
или
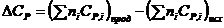 , (1.5)
, (1.5)
где 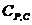 ,
, 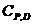 ,
, 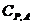 ,
,  – молярные теплоемкости реагентов при P = const;
– молярные теплоемкости реагентов при P = const;  и
и  – суммы теплоемкостей соответственно продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов ni.
– суммы теплоемкостей соответственно продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов ni.
Из (1.1) следует, что при
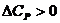
 ,
,  ; (1.6)
; (1.6)
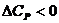
 ,
, 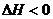 ; (1.7)
; (1.7)

 ,
, 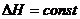 , (1.8)
, (1.8)
т.е. тепловой эффект не зависит от температуры.
При интегрировании уравнения (1.2), если известен тепловой эффект при Т 1, получим
 , (1.9)
, (1.9)
где 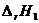 – тепловой эффект данной химической реакции при Т = Т 1 (обычно 298 К) при условии, что в заданном интервале температур нет фазовых переходов веществ, участвующих в реакции.
– тепловой эффект данной химической реакции при Т = Т 1 (обычно 298 К) при условии, что в заданном интервале температур нет фазовых переходов веществ, участвующих в реакции.
Если для реагентов
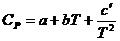 , (1.10)
, (1.10)
то
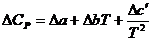 , (1.11)
, (1.11)
где
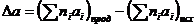 . (1.12)
. (1.12)
Например, для реакции (1.1)
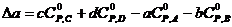 . (1.13)
. (1.13)
Аналогичным образом определяются D b, D c, D c ¢, D d.
Подставив D СР из (1.11) в (1.9), после интегрирования получим
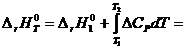
 . (1.14)
. (1.14)
Если вычислить 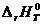 через неопределенный интеграл, получим
через неопределенный интеграл, получим
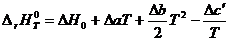 , (1.15)
, (1.15)
где D Н 0 – постоянная интегрирования, которая определяется обычно из значения теплового эффекта при стандартных условиях.
Пример расчета
Найти температурную зависимость теплового эффекта реакции
СаСО3 = СаО + СО2,
если известно, что при Т = 1173 К тепловой эффект данной реакции  = 178,074 кДж/моль. Термодинамические характеристики веществ приведены в таблице.
= 178,074 кДж/моль. Термодинамические характеристики веществ приведены в таблице.
Термодинамические характеристики веществ
| Вещество
| 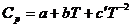 , Дж/моль×К , Дж/моль×К
| 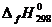 , кДж/моль , кДж/моль
|
| а
| b ×103
| c¢ ×10-5
|
| СаСО3
| 104,52
| 21,92
| –25,04
| –1206,88
|
| СаО
| 49,63
| 4,52
| –6,95
| –635,55
|
| СО2
| 44,14
| 9,04
| –8,53
| –393,51
|
Так как 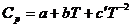 , то
, то
 .
.
Согласно уравнению Кирхгофа (1.15), определяем D а, D b и D c ¢.
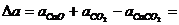
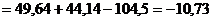 ,
,
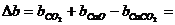
 ,
,
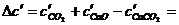
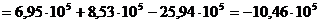 .
.
Таким образом, для данной реакции
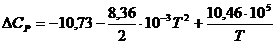 .
.
Отсюда
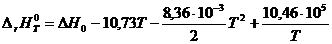 .
.
На основании определенного теплового эффекта при
Т = 1173 К находим D Н 0, подставив значения  и
и
Т = 1173 в (1.15):
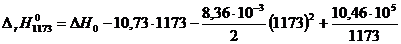 .
.
Отсюда D Н 0 = 191141,4.
Тогда уравнение (1.15) для рассматриваемой реакции имеет вид:
 .
.
На основании этого уравнения можно рассчитать тепловой эффект реакции при любой температуре.
Для определения теплового эффекта, например, при 1300 К подставим значение температуры в полученное уравнение:
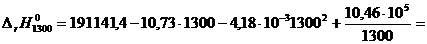
= 163869 [Дж/моль].
Для определения расхода теплоты, например, на разложение 1 кг СаСО3 при 1300 К нужно определить число молей п в 1 кг CaCO3, тогда
 ,
,
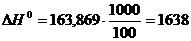 [кДж/кг].
[кДж/кг].
Если значение теплового эффекта не задано в условии, то для определения D Н 0 нужно найти тепловой эффект реакции при Т = 298 К, используя справочные значения стандартных теплот образования компонентов реакции 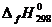 .
.
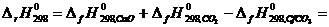
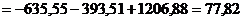 [кДж/моль].
[кДж/моль].
На основании определенного теплового эффекта 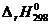 находим D Н 0:
находим D Н 0:
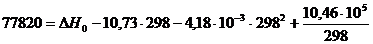 ,
,
D Н 0 = 191149,4.
Задание
1. Изучить основные законы термохимии: закон Гесса, следствия закона Гесса, закон Кирхгофа.
2. Изучить методику определения теплового эффекта химической реакции.
3. Определить температурную зависимость теплового эффекта заданной химической реакции в заданном интервале температур.
Примеры задач
1. Пользуясь данными справочника, найдите изменение энтальпии при нагревании 64 г газообразного метилового спирта от 300 дл 700 К.
2. Рассчитайте тепловой эффект реакции СО + Н2О = СО2 + Н2 при постоянном давлении и температуре 1000 К, если значение его при 298 К равно-41,17 кДж/моль. Теплоемкость взять в справочнике.
3. Определите работу, совершаемую одним молем одноатомного газа в идеальном состоянии при адиабатическом расширении, если температура газа понизилась на 50 °С.
4. Как зависит от температуры внутренняя энергия индивидуального вещества? Дайте математическое выражение этой зависимости и объясните его.
5. Пользуясь справочными данными, укажите возрастает, уменьшается или остается без изменения тепловой эффект реакции при изменении температуры от 298 до 1000 К.
6. Пользуясь справочными данными, рассчитайте тепловой эффект (ΔН) реакции, протекающей при 798 К и постоянном давлении 1 атм: 2Cl2 + 2H2O(г) = 4HCl(г) +O2.
7. Пользуясь справочными данными по стандартным энтальпиям образования индивидуальных веществ, рассчитайте изменение энтальпии при конденсации 1 моля CS2 при 298 К.
8. На основании справочных данных найдите уравнение зависимости теплового эффекта ΔН (Дж/моль) от температуры для реакции СО + 2Н2 (г) = СО2 + Н2.
9. На основании справочных данных определите тепловой эффект ΔН (Дж/моль) реакции
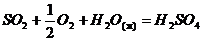 :
:
а) при температуре 298 К и постоянном давлении;
б) при температуре 298 К и постоянном объеме.
10. Используя справочные данные, определите тепловой эффект реакции MnO + H2 (г) = Mn + H2O (г) при 800 К.
11. Пользуясь справочными данными, составьте уравнение ΔС = f (T) для реакции СН4 = С + 2Н2.
12. Стандартная теплота образования кристаллического In2O3 равна -926,76 кЖд/моль. Напишите уравнение реакции, к которой относится этот тепловой эффект.
13. Найдите тепловой эффект (ΔН) реакции
СН4 + Cl2 = CH3Cl + HCl:
СН4 + О2 = СО2 + 2Н2О(ж), ΔН = -892,0 кДж;
CH3Cl + O2 = CO2 + 2Н2О(ж) + HCl, ΔН = -637,0 кДж;
Н2 + О2 = Н2О(ж), ΔН = -236,0 кДж;
Н2 + Cl2 = HCl, ΔН = -92,5 кДж.
14. Зависимость теплоемкости алюминия от температуры выражается уравнением Ср = 20,67 + 12,39·10-3 ТДж/моль. Алюминий плавится при температуре 685,5 °С, его удельная теплота плавления равна 386,23 Дж/г. Вычислите, какое количество тепла потребуется на то, чтобы получить 500 г расплавленного алюминия при температуре плавления, усли начальная температура его 25 °С.




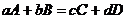 (1.1)
(1.1)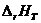 определяем по закону Кирхгофа
определяем по закону Кирхгофа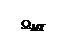
 (1.2)
(1.2) , (1.3)
, (1.3)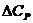 ,
, 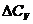 – изменения молярной теплоемкости в результате протекания процесса при P = const или V = const.
– изменения молярной теплоемкости в результате протекания процесса при P = const или V = const.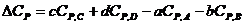 (1.4)
(1.4)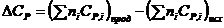 , (1.5)
, (1.5)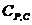 ,
, 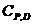 ,
, 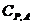 ,
,  – молярные теплоемкости реагентов при P = const;
– молярные теплоемкости реагентов при P = const;  и
и  – суммы теплоемкостей соответственно продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов ni.
– суммы теплоемкостей соответственно продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов ni.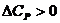
 ,
,  ; (1.6)
; (1.6)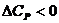
 ,
, 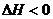 ; (1.7)
; (1.7)
 ,
, 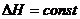 , (1.8)
, (1.8) , (1.9)
, (1.9)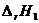 – тепловой эффект данной химической реакции при Т = Т 1 (обычно 298 К) при условии, что в заданном интервале температур нет фазовых переходов веществ, участвующих в реакции.
– тепловой эффект данной химической реакции при Т = Т 1 (обычно 298 К) при условии, что в заданном интервале температур нет фазовых переходов веществ, участвующих в реакции.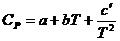 , (1.10)
, (1.10)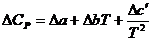 , (1.11)
, (1.11)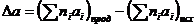 . (1.12)
. (1.12)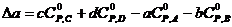 . (1.13)
. (1.13)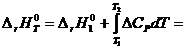
 . (1.14)
. (1.14)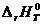 через неопределенный интеграл, получим
через неопределенный интеграл, получим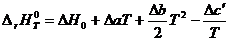 , (1.15)
, (1.15) = 178,074 кДж/моль. Термодинамические характеристики веществ приведены в таблице.
= 178,074 кДж/моль. Термодинамические характеристики веществ приведены в таблице.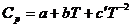 , Дж/моль×К
, Дж/моль×К
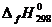 , кДж/моль
, кДж/моль
 .
.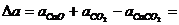
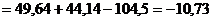 ,
,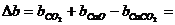
 ,
,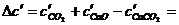
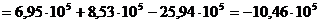 .
.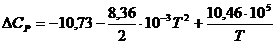 .
.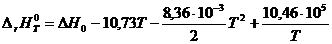 .
. и
и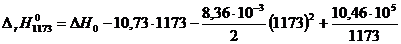 .
. .
.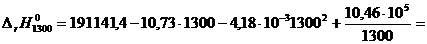
 ,
,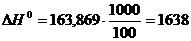 [кДж/кг].
[кДж/кг].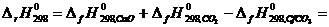
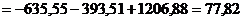 [кДж/моль].
[кДж/моль].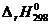 находим D Н 0:
находим D Н 0: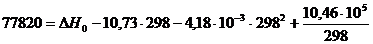 ,
,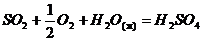 :
:


