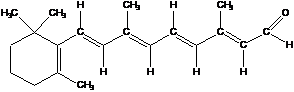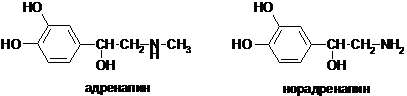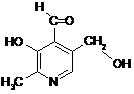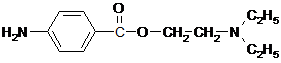Екатеринбург
УДК 546:376.14
Биоорганическая химия. Учебно-методическое пособие /Под ред. д.т.н. Белоконовой Н.А.- Екатеринбург: УГМУ, 2015. – 132 с.
JSBN 978-5-89895-731-5
Настоящее пособие содержит материалы по биоорганической химии. Это фундаментальный раздел, входящий в учебную программу дисциплины «Химия» для студентов I курса лечебно-профилактического, медико-профилактического, педиатрического и стоматологического факультетов. В учебном пособии, в отличие от предыдущих изданий собран обширный объем заданий и упражнений для аудиторной и самостоятельной работы. Методический уровень изложения материала курса биоорганической химии соответствует современным требованиям ФГОС-3 и компетентностного подхода.
Учебное пособие входит в единый комплекс материалов методического сопровождения дисциплины «Химия». Каждый раздел пособия включает необходимую учебную информацию по соответствующей теме биоорганической химии и состоит из вводной части, перечня вопросов данного раздела, тестов для самопроверки усвоения материала (с указанием правильного ответа в конце каждого раздела), задач и упражнений для аудиторной работы, а также для самостоятельного рассмотрения при подготовке к практическому занятию. В приложении представлен большой объем наглядного и справочного материала, способствующего лучшему усвоению учебной дисциплины.
Составители: С.Г. Перевалов, Л.А. Каминская, Е.Ю. Ермишина, Н.С. Клубникина, Н.А. Наронова, Н.М. Дорофеева, Р.П. Лелекова, Н.Н. Катаева Н.Н., И.В. Гаврилов.
Ответственный редактор Белоконова Н.А., д.т.н.
Рецензент Тхай В.Д., д.х.н.
JSBN 978-5-89895-731-5
© Авторы, 2015
© УГМУ, 2015
Содержание
| ТЕМА I
| Электронное строение атома углерода, виды гибридизации орбиталей (sp3, sp2). Образование химических связей в органических соединениях (σ и π связи). Классификация, номенклатура органических соединений
|
|
| ТЕМА II
| Сопряженные системы. Виды сопряжения. Ароматичность. Правило Хюккеля
|
|
| ТЕМА III
| Взаимное влияние атомов в молекулах биоорганических соединений. Электронные эффекты заместителей. Кислотные и основные свойства органических молекул
|
|
| Тема IV
| Моно- и дикарбоновые кислоты
|
|
| ТЕМА V
| Гидрокси- и оксокислоты
|
|
| Тема VI
| Высшие карбоновые кислоты. Липиды. Фосфолипиды
|
|
| Тема VII
| Аминокислоты
|
|
| ТЕМА VIII
| Пептиды и белки. Строение и биологическая роль
|
|
| ТЕМА IX
| Углеводы. Классификация. Моносахариды
|
|
| ТЕМА X
| Углеводы. Дисахариды. Олигосахариды. Полисахариды
|
|
| ТЕМА XI
| Нуклеиновые кислоты. Нуклеотиды
|
|
| ТЕМА XII
| Механизмы реакций в биоорганической химии. Реакции биологического окисления
|
|
| ТЕМА XIII
| Изомерия биоорганических соединений
|
|
|
литературА
|
|
|
ПРИЛОЖЕНИЯ
|
|
ТЕМА I. Электронное строение атома углерода, виды гибридизации орбиталей (sp3, sp2). Образование химических связей в органических соединениях (сигма- и πи- связи). Классификация, номенклатура органических соединений
Биоорганическая химия изучает строение и химические свойства органических веществ, участвующих в процессах жизнедеятельности, в непосредственной связи с их биологическими функциями. В настоящее время известно более 50 млн органических соединений. Такое громадное количество соединений требует строгой классификации и единых международных номенклатурных правил. Этому вопросу уделяется особое внимание в связи с использованием компьютерных технологий для создания разнообразных баз данных.
По теме занятия студентдолжен
знать следующий материал:
- электронное строение атомовбиогенных э лементов C, H, N, O, S;
- понятия: гибридизация атомных орбиталей и ее типы, σ- и π-связь, функциональная группа;
- правила записи структурных формул органических соединений;
- номенклатурные названия важнейших классов органических соединений, функциональных групп;
- правила составления названий органических соединений по их структурным формулам в соответствии с номенклатурой
(ИЮПАК);
уметь записывать по названию структурную формулу органического соединения, а по формуле – название; определять принадлежность органических соединений к номенклатурным классам по их старшим функциональным группам (по названиям и структурным формулам);
владеть знаниями классификации, номенклатуры и систематизации органических соединений.
Вопросы для подготовки
1. Предмет и задачи биоорганической химии. Роль биоорганической химии в подготовке врача.
2. Электронное строение атома углерода, виды гибридизации орбиталей (sp3, sp2). Образование химических связей в органических соединениях (σ- и π-связи).
3. Классификация органических соединений по строению углеродного скелета, по природе функциональных групп.
4. Номенклатура органических соединений.
Задачи и упражнения
1. Дайте определение σ-связи и π-связи. Определите число σ- и π-связей в молекуле метана, этена, этанола, этаналя, муравьиной кислоты.
2. Составьте диаграммы распределения электронов атомов углерода в sp3, sp2 гибридных состояниях (метан, этен), атома азота в основном состоянии и зарисуйте пространственную конфигурацию орбиталей.
3. Дайте определения первичному, вторичному, третичному и четвертичному атомам углерода. Выберите соединения, в молекулах которых все атомы углерода вторичные: этилен, пропанол-2, циклопентан, изобутан, бензол, этан.
4. Напишите структурную формулу углеводорода, который содержит шесть первичных атомов углерода, но не содержит – вторичных и третичных, назовите его по современной номенклатуре.
5. Сформулируйте определение понятия «функциональная группа».
6. Классифицируйте следующие органические соединения по типу углеродного скелета и наличию кратных связей (см. приложение к теме 1 схема 1.1.): пентан, этанол, диэтиловый эфир, этен, пента-1,4-диен, бута-1,3-диен, хлорэтен, циклопентан, циклогексан, ретиналь, бензол, фенол, анилин, нафталин, пиридин, никотиновая (пиридин-3-карбоновая) кислота, пиримидин, пиррол, фуран, пурин.
7. Классифицируйте следующие органические соединения по природе функциональных групп (см. приложение к теме 1: таблица 1.1):пропанол-1, 2-метилбутанол-2, 3-метил-пентанол-2, глицерин, фенол, диэтиловый эфир, метилизопропиловый эфир, этиловый эфир пропионовой кислоты, метилпальмитат, этилбензоат, метиламин, этиламин, метилэтиламин, триэтиламин, этантиол, формальдегид (метаналь), ацетальдегид (этаналь), ацетон (пропанон), уксусная кислота (этановая), янтарная кислота (бутандиовая), фумаровая кислота (транс -бутендиовая), молочная кислота (2-гидроксипропановая), яблочная кислота (2-гидроксибутандиовая), пировиноградная кислота (2-оксопропановая), щавелевоуксусная кислота (2-оксо-бутандиовая).
8. Какие основные принципы формирования названий органических соединений положены в основу современной систематической номенклатуры ИЮПАК (IUPAC)? Расшифруйте аббревиатуру ИЮПАК.
9. Расположите функциональные группы в порядке увеличения старшинства:
1) гидроксильная, аминогруппа, карбоксильная, тиольная,
2) хлор-, сульфогруппа, гидроксильная, карбонильная.
10. Назовите приведенные соединения в соответствии с правилами современной номенклатуры ИЮПАК:
1) аспарагиновая кислота НООС-СН2-СН(NН2)-СООН
2) глицерин НО-СН2-СН(ОН)-СН2–ОН
3) янтарная кислота НООС-СН2-СН2-СООН
4) глицериновый альдегид НО-СН2-СН(ОН)-СНО
5) цистеин НS-СН2-СН(NН2)-СООН
| 6) фенилаланин
| 
|
11. Напишите структурные формулы биоорганических соединений, укажите их принадлежность к определенному классу:
1) 2-оксопропановая кислота (пировиноградная кислота)
2) 2- аминоэтантиол (меркамин)
3) 3-оксобутановая кислота (ацетоуксусная кислота)
4) 2-аминоэтанол (коламин, этаноламин)
5) 2,3,4,5-тетрагидрокcипентаналь (рибоза)
6) 2-амино-3-фенилпропановая кислота (фенилаланин)
7) 2-оксопентандиовая кислота (α-кетоглутаровая кислота)
8) 3-гидрокcи-3-метилпентандиовая кислота (ключевое соединение в синтезе холестерина в организме человека)
9) 2,3-дигидроксипропаналь (глицериновый альдегид)
10) 2-амино-3-гидроксипропановая кислота (серин)
11) 2-аминопентандиовая кислота (глутаминовая кислота)
12) 2-амино-3-(4-гидроксифенил)пропановая кислота (тирозин)
13) 4-(2-аминоэтил)имидазол (гистамин)
14) 2-амино-3-метилпентановая кислота (изолейцин)
15) 1-(3,4-дигидроксифенил)-2-метиламиноэтанол (адреналин)
16) цис-9-октадекаеновая кислота (олеиновая кислота)
17) 2-амино-4-метилтиобутановая кислота (метионин)
18) 2-гидроксипропан-1,2,3-трикарбоновая кислота (лимонная кислота)
19) 2-амино-1-(3,4-дигидроксифенил)этанол (норадреналин)
20) все цис 9,12,15-октадекатриеновая кислота (линоленовая)
21) 2-амино-3-меркаптопропановая кислота (цистеин)
22) 3-(2-аминоэтил)-5-гидроксииндол (серотонин)
23) 6-аминопурин (аденин)
24) 5-метил-2,4-диоксопиримидин (тимин)
25) 2,6-диаминогексановая кислота (лизин)
Тесты
1. Выберите верно составленный ряд старшинства групп:
а) СНО > ОН > СН3 б) СН3 > ОН > СНО
в) ОН > СНО > СН3 г). СНО > СН3 > ОН
д) ОН > СН3 > СНО
2. Выберите верно составленный ряд старшинства групп:
а) С1 > NН2 > SH б) NН2 > SH > С1
в) С1 > SH > NН2 г) SH > NН2 > С1
д) SH > С1 > NН2
3. В соответствии с номенклатурой ИЮПАК выберите верное название вещества:
 а) 2-амино-1-карбоксипропан
б) 2-амино-3-карбоксипропан
в) 2-аминобутановая кислота
г) 3-аминобутановая кислота
д) 3-амино-3-метилпропановая кислота
а) 2-амино-1-карбоксипропан
б) 2-амино-3-карбоксипропан
в) 2-аминобутановая кислота
г) 3-аминобутановая кислота
д) 3-амино-3-метилпропановая кислота
|
4. В соответствии с номенклатурой ИЮПАК выберите верное название вещества:
 а) 2-амино-3-гидроксибутаналь
б) 2-гидрокси-3-аминобутаналь
в) 1-оксо-2-аминобутанол-3
г) 1-амино-1-оксобутанол-3
д) 3-амино-4-оксобутанол-2
а) 2-амино-3-гидроксибутаналь
б) 2-гидрокси-3-аминобутаналь
в) 1-оксо-2-аминобутанол-3
г) 1-амино-1-оксобутанол-3
д) 3-амино-4-оксобутанол-2
|
Ответы к теме I
1а; 2г; 3г; 4а; 5б; 6г; 7б; 8в; 9а; 10а; 11а.
Задачи и упражнения
1. Запишите структурные формулы ациклических (линейных) сопряженных соединений, для которых характерно π-π-сопряжение: бутадиен, изопрен, кислоты пировиноградная, щавелевоуксусная, 2-бутеновая.
2. Запишите структурные формулы ациклических (линейных) сопряженных соединений, для которых характерно р -π-сопряжение: хлорэтен, дивиниламин, дивиниловый эфир, этенол. Объясните участие атомов азота, кислорода, галогена в образовании сопряженной системы.
3. Выберите соединения с сопряженными системами и укажите тип сопряжения:
а) СН3-СН=СН-СН=СН2 б) СН2=СН-СН2-СН2-СН=СН2
в) Н2С=СН-ОН г) СН3-NH-СН=СН2
д) Н3С-СН=СН-СООН е) Н2С=СН-СН2-СООН
ж) СН2=СН—СН=СН2 з) СН2=СН—СН2—СН=СН2
и) СН2=СН—NH—СН=СН2 к) СН2=СН—O—СН=СН2
4. Сравните структурные формулы витамина А в двух его формах: ретинола и ретиналя, определите длину цепи сопряжения. Сделайте вывод о том, какое из двух соединений является термодинамически более устойчивым.

Витамин А (ретинол)
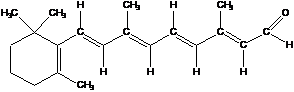
Витамин А (ретиналь)
5. Используя правило Хюккеля докажите, что бензол, нафталин, антрацен и фенантрен являются ароматическими соединениями. Укажите тип сопряжения в молекулах.
6. Объясните строение гетероциклических азотсодержащих соединений: пиридина, пиримидина, пиррола. Какой тип сопряжения для них характерен? Ароматичны ли эти соединения? Укажите отличительные особенности в строении и химическом поведении пиридинового атома азота и пиррольного атома азота?
7. Гибридизация электронных орбиталей атома азота при образовании пяти- и шестичленных гетероароматических соединений.
8. Докажите, используя правило Хюккеля, что тиофен, пиррол, фуран являются ароматическими соединениями. Укажите тип сопряжения в этих соединениях.
9. Расположите каждые три соединения в порядке увеличения ароматических свойств:
а) тиофен, бензол, фуран
б) бензол, пиридин, пиримидин
в) фуран, тиофен, пиррол
г) пиридин, пиррол, бензол
10. Распределите вышеприведенные соединения из задания 9 на две группы:
а) π-недостаточные б) π-избыточные
11. Запишите структурные формулы биологически активных соединений: имидазол, пурин, индол. Приведите нумерацию атомов; определите, какие атомы азота имеют, а какие не имеют заметные основные свойства. Объясните возникшие различия в участии атома азота при образовании пяти- и шестичленных гетероароматических систем.
Тесты
Ответы к теме II
1б; 2а; 3а; 4б; 5.2; 6г; 7б; 8а; 9а; 10.4; 11в; 12г; 13.3; 14в
Задачи и упражнения
1. Изобразите направление индуктивных эффектов в молекулах следующих кислот: этановая, пропановая, бутановая, 2-гидроксипропановая (молочная), 3-гидроксипропановая.
2. Сравните индуктивные эффектов двух групп: амино -NH2 и положительно заряженной триметиламмонийной - +N(CH3)3 на примере 2-аминоэтанола (коламина) и холина
(НО-СН2–СН2–N+(СН3)3), который в организме образует нейромедиатор ацетилхолин.
3. Составьте диаграммы распределения электронной плотности(покажите мезомерные и индуктивные эффекты и укажите их знак) в ациклических сопряженных системах: хлорэтен (сравнить с хлорэтаном); пропеновая, 2-бутеновая, 2-оксопропановая кислоты (сравнить с 2-гидроксипропановой); этенол (сравнить с этанолом).
4. Изобразите направление мезомерных эффектов в гетероароматических соединениях: пиридин, пиридиниевый катион, никотиновая кислота, пиримидин.
5. В анилине или в этиламине аминогруппа проявляет +М эффект?
6. Изобразите направление мезомерных эффектов в молекулах: пропена, пропеновой кислоты, хлористого винила, 3-хлорпропена и объясните соблюдение и несоблюдение правила Марковникова в реакциях гидрогалогенирования этих соединений.
7. Изобразите направление мезомерных эффектов в молекулах: бензойной кислоты, толуола, фенола, анилина и объясните правило ориентации в реакциях замещения атомов водорода ароматического кольца на галогены.
8. Сравните кислотные свойства биоорганических соединений, расположите их в последовательности изменения кислотных свойств:
а) фенол, пропанол, этанол – уменьшения;
б) этанол, холин, аминоэтанол – увеличения;
в) пропановая, пировиноградная, молочная кислоты – увеличения;
г) этандиовая, пропановая, пропандиовая (малоновая) кислоты – уменьшения;
д) пропановая, уксусная, малоновая кислоты – уменьшения;
е) фенол, вода, этанол – увеличения;
ж) 4-нитробензойная, 4-метилбензойная, бензойная кислоты – уменьшения.
9. Сравните основные свойства биоорганических соединений, расположите их в последовательности изменения:
а) аммиак, диэтиламин, этиламин- увеличения;
б) анилин, этиламин, аммиак – уменьшения;
в) пиридин, аммиак, диэтиламин – уменьшения;
г) анилин, 4-нитроанилин, 4-метиланилин – увеличения;
д) диметиловый эфир, диметиламин, диметилсульфид – уменьшения.
10. Сравните основные свойства атома азота в молекулах гормонов адреналина и норадреналина.
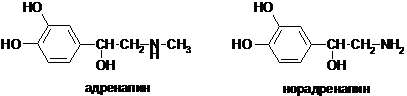
11. Сравните кислотные свойства гидроксигрупп в молекуле пиридоксаля – одной из активных форм витамина В6.
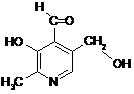
12. Запишите реакцию образования хлороводородной соли новокаина (учтите, что присоединение протона происходит к более основному атому азота). Новокаин является распространенным обезболивающим препаратом (анестетиком).
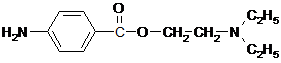
Тесты
1. Выберите заместители, проявляющие положительный индуктивный эффект по отношению к радикалу:
1. R-CH3 2. R-ОС2Н5 3. R-C2H5 4. R‑SH
5. R-NH2 6. R‑С1
а) 1, 2, 3, 5 б) 2, 3, 4, 6 в) 1, 3, 6 г) 2, 3,5 д) 1, 3
2. Выберите заместители, проявляющие отрицательный индуктивный эффект по отношению к радикалу:
1. R-COOH 2. R-С2H5 3. R-OPO3H2 4. R-CH3 5. R-NO2
а) 1, 3, 4 б) 1, 2, 4 в) 2, 3, 5 г) 1, 3, 5 д) 1, 2, 4, 5
3. Выберите заместители, проявляющие положительный мезомерный эффект по отношению к радикалу:
1. С6Н5-СООН 2. С6Н5-Сl 3. С6Н5-SO3H
4. С6Н5-ОСН3 5. С6Н5-NН2
а) 4, 5 б) 3, 4, 5 в) 2, 4, 5 г) 1, 3, 4 д) 1, 2, 3, 5
4. Выберите заместители, проявляющие отрицательный мезомерный эффект по отношению к фенильному радикалу (С6Н5-):
1. С6Н5-Сl 2. С6Н5-SO3H 3. С6Н5-СООН
4. С6Н5-СН3 5. С6Н5-NH2
а) 1, 2 б) 2, 4, 5 в) 1, 4, 5 г) 2, 3, 5 д) 2, 3
5. Мезомерный эффект – это:
а) перераспределение электронной плотности в сопряженных системах, обусловленное смещением электронной плотности p-связей;
б) перераспределение электронной плотности по системе s-связей;
в) смещение электронной плотности в системе, содержащей только атомы углерода в sp3 -гибридном состоянии;
г) перераспределение электронной плотности только в ароматических системах.
6. Индуктивный эффект передается:
а) только в сопряженной системе б) по системе p-связей
в) по системе s- связей г) по системе s-связей и p-связей
7. Какие соединения проявляют основные свойства:
а) пиррол, пиридин
б) пиридин, пиримидин
в) пиррол, пиримидин, имидазол
г) пиррол, пиридин, пиримидин
д) пиррол, пиридин, имидазол
8. Какие соединения проявляют кислотные свойства:
а) пиррол, пиридин б) пиридин, пиримидин
в) пиррол, индол г) пиррол, пиридин, пиримидин
д) пиридин, имидазол
Ответы к теме III
1д; 2г; 3в; 4д; 5а; 6в; 7б; 8в; 9б; 10в; 11в; 12г; 13б; 14б; 15в; 16а; 17г; 18г; 19а; 20д; 21в; 22.4; 23г.
Задачи и упражнения
1. Укажите структурные особенности молекул карбоновых кислот, позволяющие им образовывать водородные связи. Объясните, почему Ткип. карбоновых кислот выше, чем у соответствующих спиртов.
2. Покажите электронные эффекты в молекулах карбоновых кислот, с точки зрения протолитической теории объясните различие силы кислот:
- пропановая и малоновая; - акриловая и кротоновая.
2. Сравните кислотные свойства карбоновых кислот:
1) а) янтарная, б) малоновая, в) щавелевая;
2) а) муравьиная, б) пропановая, в) уксусная;
3) а) хлоруксусная, б) трихлоруксусная, в) уксусная;
4) а) кротоновая, б) пропионовая, в) масляная;
5) а) щавелевая, б) уксусная, в) акриловая.
3. Запишите уравнения химических реакций, укажите условия, назовите продукты:
1) уксусная кислота + этанол;
2) этерификации пропионовой и щавелевой кислот метанолом;
3) образования хлорангидрида валериановой кислоты;
4) образования амида пропановой кислоты;
5) образования натриевой соли муравьиной кислоты;
6) образования ангидридов глутаровой и малеиновой кислот;
7) декарбоксилирования щавелевой и малоновой кислот;
8) образования ацетил-КоА из уксусной кислоты;
9) образования малонил-КоА
10) образования сложного тиоэфира – ацетилхолина;
11) янтарная кислота + ФАД ↔? + ФАДН2
4. Запишите качественные реакции:
1) обнаружения уксусной кислоты;
2) обнаружения муравьиной кислоты;
3) обнаружения акриловой кислоты;
4) обнаружения щавелевой кислоты.
Тесты
1. Монокарбоновыми кислотами являются:
а) уксусная, муравьиная, масляная;
б) щавелевая, малоновая, янтарная;
в) уксусная, масляная, щавелевая;
г) щавелевая, янтарная, муравьиная;
д) муравьиная, масляная, малоновая.
2. Непредельными кислотами являются:
а) бутановая, кротоновая, малеиновая;
б) акриловая, бутановая, янтарная;
в) акриловая, кротоновая, фумаровая;
г) щавелевая, янтарная, муравьиная;
д) муравьиная, масляная, малоновая.
3. Выберите макроэргическое соединение in vivo:
а) уксусная кислота б) муравьиная кислота
в) янтарная кислота г) ацетил-КоА
д) фумаровая кислота
4. Дикарбоновыми кислотами являются:
а) уксусная, муравьиная, масляная;
б) щавелевая, малоновая, янтарная;
в) уксусная, масляная, щавелевая;
г) щавелевая, янтарная, муравьиная;
д) муравьиная, масляная, малоновая.
5. При гидрировании (восстановлении) непредельной кислоты в биохимической реакции получили янтарную кислоту. Какая кислота участвовала в реакции:
а) фумаровая б) малеиновая в) яблочная
г) щавелевоуксусная д) лимонная
6. Выберите дикарбоновую ненасыщенную кислоту, которая является важнейшим клеточным метаболитом:
а) уксусная б) янтарная в) малеиновая
г) глутаровая д) фумаровая
7. Выберите дикарбоновую насыщенную кислоту, которая является метаболитом цикла Кребса, лекарственным препаратом:
а) уксусная б) янтарная в) малеиновая
г) глутаровая д) фумаровая
8. Сравните кислотные свойства карбоновых кислот:
1) муравьиная 2) масляная 3) уксусная
а) 1 > 2 > 3 б) 1 > 3 > 2 в.) 2 > 3 > 1
г) 2 > 1 > 3 д) 3 > 2 > 1
9. Сравните кислотные свойства карбоновых кислот:
1) янтарная 2) малоновая 3) щавелевая
а) 1 > 2 > 3 б) 1 > 3 > 2 в) 2 > 3 > 1
г) 2 > 1> 3 д) 3 > 2 > 1
10. Сравните кислотные свойства карбоновых кислот:
1) масляная 2) щавелевая 3) янтарная
а) 1 > 2 > 3 б) 1 > 3 > 2 в) 2 > 3 > 1
г) 2 > 1 > 3 д) 3 > 2 > 1
Ответы к теме IV
1а; 2в; 3г; 4б; 5а; 6д; 7б; 8б; 9д; 10в.
Задачи и упражнения
1. Сравните кислотные свойства карбоновых кислот и объясните различия:
- янтарная и яблочная; - уксусная и гликолевая;
- молочная и пропановая; - молочная и пировиноградная.
2. Сравните кислотные свойства карбоновых кислот:
а) 1) уксусная, 2) пировиноградная, 3) молочная;
б) 1) яблочная, 2) янтарная, 3) щавелевоуксусная;
в) 1) молочная, 2) β-гидроксимасляная, 3) пропановая;
г) 1) яблочная, 2) щавелевоуксусная, 3) бутановая.
3. Напишите уравнения особых химических реакций гидроксикислот:
3.1. реакция элиминирования (внутримолекулярная дегидратация)
а) 3-гидроксибутановая ↔ кротоновая + НОН
б) яблочная ↔ фумаровая + НОН
3.2. реакции окисления, образование кетокислот
а) молочная + НАД+ ↔ пировиноградная + НАДН + Н+
б) яблочная + НАД+ ↔ щавелевоуксусная + НАДН + Н+
в) изолимонная +НАД+ ↔ α -кетоглутаровая + НАДН + Н+
4. Запишите уравнения особых химических реакций оксокислот:
- стереоспецифическая реакция восстановления in vivo, образование D- или L- гидроксикарбоновых кислот.
4.1. реакции восстановления, образования гидроксикислот:
а) пировиноградная + НАДН + Н+ ↔ молочная + НАД+
б) щавелевоуксусная + НАДН + Н+ ↔ яблочная + НАД+
4.2. реакция декарбоксилирования α- и β – оксокислот
а) пировиноградная → уксусный альдегид + СО2
б) ацетоуксусная → ацетон + СО2
4.3. Реакция окисления пировиноградной кислоты in vivo с образованием ацетил КоА
ПВК + НАД+ + коэнзим А → ацетил-КоА + НАДН + Н+ + СО2
4.4 Кето-енольная таутомерия оксокислот: пировиноградной, ацетоуксусной, щавелевоуксусной. Строение и биологическая роль фосфорного эфира пировиноградной кислоты – макроэргического соединения.
5. Составьте уравнения реакций, соответствующих превращениям in vivo, которые изучаются в курсе биохимии:
а) молочная кислота ↔ пировиноградная → уксусный альдегид;
б) янтарная кислота ↔фумаровая ↔ яблочная ↔ щавелевоуксусная;
в) щавелевоуксусная ↔яблочная ↔фумаровая ↔ янтарная;
г) бут-2-еновая кислота (кротоновая) ↔β-гидроксимасляная ↔ацетоуксусная → ацетон;
д) лимонная → цис -аконитовая → изолимонная.
6. Запишите уравнения химических реакций:
1) термическое разложение пировиноградной кислоты;
2) гидратация фумаровой кислоты и образование L- и D–яблочных кислот;
3) термическое разложение 3-оксобутановой кислоты.
7. Запишите качественные реакции:
1. обнаружение фенола в растворе (применение соли хлорида железа (III));
2. обнаружение молочной кислоты (с участием фенолята железа).
8. Запишите структурные формулы кислот в последовательности реакций цикла Кребса. Назовите все полученные соединения в соответствии с номенклатурой ИЮПАК:
щавелевоуксусная кислота + ацетил-КоА (1) → лимонная кислота (2) → изолимонная кислота (3) → α-кетоглутаровая кислота (4) → янтарная кислота (5) → фумаровая кислота (6) → яблочная кислота (7) → щавелевоуксусная кислота (8).
Тесты
1. В состав «кетоновых тел» входят соединения:
1. уксусная кислота 2. ацетон
3. яблочная кислота 4. 2-гидроксипропановая
5. β-гидроксимасляная 6. β-оксомасляная
а) 1, 2, 3 б) 2, 3, 4 в) 4,5, 6
г) 2, 5, 6 д) 2, 3, 6
2. К гидроксикарбоновым кислотам относятся кислоты:
а) молочная, пировиноградная; б) молочная, яблочная;
в) пировиноградная, малоновая; г) янтарная, молочная;
д) щавелевоуксусная, яблочная.
3. К оксокарбоновым кислотам относятся кислоты:
а) пировиноградная, щавелевоуксусная;
б) яблочная, щавелевоуксусная;
в) янтарная, лимонная;
г) молочная, малоновая;
д) лимонная, пировиноградная.
4. Дикарбоновыми кислотами являются:
а) лимонная, янтарная, щавелевая;
б) щавелевоуксусная, янтарная, яблочная;
в) лимонная, яблочная, щавелевая;
г) щавелевая, янтарная, молочная;
д) молочная, янтарная, бутановая.
5. Выберите гидрокситрикарбоновую кислоту:
а) янтарная б) фумаровая в) лимонная
г) пировиноградная д) молочная
6. Какую кислоту получают при дегидратации яблочной кислоты:
а) малоновую б) фумаровую в) янтарную
г) пировиноградную д) молочную
7. Какие две кислоты превращаются друг в друга в окислительно-восстановительной реакции:
а) молочная и малоновая
б) пировиноградная и щавелевоуксусная
в) молочная и пировинограданая
г) яблочная и янтарная
д) фумаровая и яблочная
8. Сравните кислотные свойства карбоновых кислот:
1) уксусная 2) пировиноградная 3) молочная
а) 1 >2 > 3 б) 1 > 3 > 2 в) 2 > 3 > 1
г) 2 > 1 >3 д) 3 >1 >2 e) 3 > 2 > 1
9. Какое вещество образуется при окислении пировиноградной кислоты in vivo:
а) молочная кислота б) малоновая кислота
в) ацетоуксусная кислота г) ацетил-КоА
д) уксусный альдегид
10. Сравните кислотные свойства карбоновых кислот:
1) яблочная 2) янтарная 3) щавелевоуксусная
а) 1 >2 > 3 б) 1 > 3> 2 в) 2 > 3 > 1
г) 2 > 1 > 3 д) 3 >1 > 2
Ответы к теме V
1г; 2б; 3а; 4б; 5в; 6б; 7в; 8в; 9г; 10д.
Липиды. Фосфолипиды
Липиды – большая группа природных биоорганических веществ и их синтетических аналогов, которая объединяет химические соединения не по общему признаку состава, строения, а по признаку сходства физико-химических свойств.
Липиды совместимы друг с другом, растворимы в неполярных органических растворителях (диэтиловый эфир), не растворимы в воде. Такие липиды обладают липофильными (гидрофобными) свойствами. Некоторые липиды в воде образуют разные виды коллоидных раcтворов. Это амфифильные липиды.
Большое разнообразие различных химических соединений в одной группе делает любую их классификацию несовершенной.
Многие представители липидов – сложные эфиры, содержат высшие карбоновые кислоты. Многие липиды in vivo совместно участвуют в биохимических реакциях и имеют общие пути биосинтеза.
По теме занятия студент должен:
знать следующий материал:
- классификацию и номенклатуру представителей липидов;
- строение заменимых и незаменимых природных высших карбоновых кислот, триглицеридов, фосфолипидов, холестерина и его эфиров, связь между пространственным строением и физико-химическими и биологическими свойствами этих липидов, их важнейшие химические свойства (гидролиз, образование триглицеридов и фосфолипидов in vivo из глицерина и ацил-КоА);
- биологическое значение важнейших классов липидов (см. приложение VIII);
уметь записывать структурные формулы заменимых и незаменимых высших жирных кислот в цис- и транс- изомерных формах, триглицеридов, фосфолипидов (кефалина, лецитина), холестерина и его эфиров, применять номенклатуру для их обозначения; составить уравнения реакций, подтверждающих важнейшие химические свойства представителей липидов; проводить качественные реакции обнаружения представителей липидов (холестерин);
владеть знаниями биологического значения важнейших классов липидов, их использования в медицине.
Вопросы для подготовки
1. Высшие карбоновые кислоты (высшие жирные кислоты, ВЖК). Классификация, номенклатура, особенности химического строения, физические свойства. Высшие насыщенные кислоты: пальмитиновая, стеариновая. Высшие цис-ненасыщен-ные кислоты, содержащие одну и несколько несопряженных двойных связей:
- моноеновые: пальмитолеиновая, олеиновая, транс-ненасыщенная кислота элаидиновая;
- полиеновые: линолевая, линоленовая, арахидоновая, Незаменимые и заменимые ВЖК. Витамин F. Биологическая роль.
2. Химические свойства высших карбоновых кислот:
а) образование солей, отличие в растворимости Na, K-солей от Ca и Mg-солей, физико-химические свойства растворимых солей (поверхностно-активные вещества (ПАВ), мыла);
б) образование сложных эфиров;
в) реакция гидрирования непредельных кислот;
г) условия изомеризации природных цис-кислот в транс-кислоты, токсические свойства транс-ненасыщенных кислот.
3. Классификация липидов:
а) по химическому строению (наиболее распространенная) –простые липиды; сложные липиды; стероиды; терпены, каротиноиды (каротин, ликопин), жирорастворимые витамины (А, D, Е, К); прочие (высшие жирные кислоты – насыщенные и ненасыщенные);
б) классификация по способности к щелочному гидролизу (омыляемые и неомыляемые).
4. Простые липиды:
а) воски: химический состав, номенклатура, строение, распространение в природе, биологическое значение;
б) триглицериды (ТГ): строение, номенклатура, распространение в природе, биологическое значение, физические свойства, химический состав, связь между химическим составом и физическими свойствами. Реакции гидролиза в кислой и щелочной среде (омыление).
5. Сложные липиды:
а) L-фосфатидовые кислоты - промежуточные вещества в синтезе ТГ и ФЛ-строение, биологическое значение;
б) фосфолипиды (ФЛ): глицерофосфолипиды: фосфатидилхолин (лецитин), фосфатилилэтаноламин (кефалин), фосфатидилсерин, фосфатидилинозитолдифосфат. Структурные формулы, химический состав, физико-химические свойства, биологическое значение;
в) сфингомиелины и гликолипиды: цереброзиды и ганглиозиды. Состав и биологическая роль.
6. Строение холестерина, нумерация атомов молекулы, расположение гидроксигруппы, двойной связи, название циклической системы (циклопентанпергидрофенантреновая). Биологическое значение холестерина. Эфиры холестерина. Реакция этерификации холестерина высшими карбоновыми кислотами.
7. Строение клеточных мембран.
8. Липотропные медицинские препараты. Линетол и полиненасыщенные ВЖК.
Задачи и упражнения
1. Для высшей природной карбоновой кислоты стали составлять обозначение: 18:2: … Допишите, указав расположение всех кратных связей.
2. Для природной высшей карбоновой кислоты записали обозначение: 18:3:9,12,15. Назовите эту кислоту.
3. В составе крема содержится природная кислота, названная «омега-3». Какое химическое название ей соответствует?
4. Для лечебных целей используется набор незаменимых природных высших жирных кислот – витамин F. Назовите эти кислоты.
5. При анализе липидного состава ткани обнаружили высокое содержание природной кислоты, о которой известно: «С-18, ω-3». Составьте пространственную формулу этой кислоты, опишите ее физико-химические свойства и объясните происхождение обозначения «ω-3».
6. Карбоновая кислота арахидоновая. Какое обозначение соответствует этой кислоте?
7. С какой целью используется в химии липидов понятие «йодное число»? Что оно определяет?
8. Составьте структурные формулы ацетил-КоА, пальмитоил-КоА, олеил-КоА. Какова биологическая роль этих веществ в организме?
9. Составьте структурные формулы триглицеридов и запишите для них уравнения реакций гидролиза в кислой и щелочной среде. Как называются полученные вещества?
а) тристеарин
б) L-1-пальмитоил-2-олеоил-3-стеарин
в) L-1-олеоил-2-пальмитоил-3-стеарин
г) L-1-стеароил-2-линолео-3-олеин
д) L-1-линолео-2-линоленоил-3-пальмитин
10. Составьте формулу фосфатидовой кислоты, содержащей пальмитиновую и линоленовую кислоты.
11. Составьте формулы L-фосфатидов:
а) лецитина, содержащего стеариновую и линолевую кислоты;
б) кефалина, содержащего пальмитиновую и линолевую кислоты.
12. При гидролизе лецитина в щелочной среде среди продуктов гидролиза обнаружили соли арахидоновой и стеариновой кислот. Запишите структурную форму лецитина и реакцию гидролиза.
13. При гидролизе фосфолипида получили олеиновую и пальмитиновую кислоты, спирт коламин и фосфорную кислоту. Запишите название и формулу фосфолипида в ионизированной форме.
14. Запишите структурную формулу холестерина и реакцию этерификации холестерина олеиновой кислотой.
Тесты
1. Выберите верные утверждения. Природные высшие жирные кислоты в липидах человеческого организма могут быть по составу и строению:
1. насыщенными, содержат четное число атомов углерода;
2. насыщенными, содержат нечетное число атомов углерода;
3. ненасыщенными, имеют транс-строение двойных связей, содержат четное число атомов углерода;
4. ненасыщенными, имеют цис-строение двойных связей, содержат четное число атомов углерода;
5. ненасыщенными, имеют цис-строение двойных связей, содержат нечетное число атомов углерода.
а) 1, 4 б) 2, 4 в) 1, 3 г) 1, 5 д) 2, 3, 5
2. К незаменимым высшим полиеновым кислотам относятся:
а) линолевая, арахидоновая, олеиновая;
б) линолевая, линоленовая, олеиновая;
в) линолевая, линоленовая, арахидоновая;
г) линолевая, пальмитиновая, линоленовая;
д) линолевая, линоленовая, стеариновая.
Ответы к теме VI
1а; 2в; 3 г; 4б; 5г; 6в; 7д;8б; 9а; 10а; 11г; 12в; 13г; 14а; 15в.
Тема VII. Аминокислоты
Аминокислоты – органические соединения, содержащие в молекулах не менее одной карбоксильной (СООН) и не менее одной аминогруппы (NH2), очень разнообразные по происхождению, строению и физико-химическ




 а) 2-амино-1-карбоксипропан
б) 2-амино-3-карбоксипропан
в) 2-аминобутановая кислота
г) 3-аминобутановая кислота
д) 3-амино-3-метилпропановая кислота
а) 2-амино-1-карбоксипропан
б) 2-амино-3-карбоксипропан
в) 2-аминобутановая кислота
г) 3-аминобутановая кислота
д) 3-амино-3-метилпропановая кислота
 а) 2-амино-3-гидроксибутаналь
б) 2-гидрокси-3-аминобутаналь
в) 1-оксо-2-аминобутанол-3
г) 1-амино-1-оксобутанол-3
д) 3-амино-4-оксобутанол-2
а) 2-амино-3-гидроксибутаналь
б) 2-гидрокси-3-аминобутаналь
в) 1-оксо-2-аминобутанол-3
г) 1-амино-1-оксобутанол-3
д) 3-амино-4-оксобутанол-2