Сильные электролиты в растворе полностью диссоциируют на ионы. Для других электролитов диссоциация – процесс обратимый. Константа равновесия этого обратимого процесса называется константой диссоциации.
KА D K+ + А–
|
|  , ,
| (7.14)
|
где K д – константа диссоциации.
Константа диссоциации постоянна при определенной температуре и в отличие от степени диссоциации не зависит от концентрации. Значения констант диссоциации слабых электролитов приведены в таблице приложения 6.
Рассмотрим зависимость между степенью диссоциации и концентрацией электролита на примере слабого электролита - уксусной кислоты:
СН3СООН D СН3СОО – + Н +.
Принимая исходную концентрацию кислоты равной С, а степень диссоциации α, получаем, что концентрация части кислоты, которая диссоциирует на ионы, будет равна α С. Так как при диссоциации одной молекулы кислоты образуется по одному иону Н + и СН3СОО –, то их концентрации тоже будут равны по α С. Концентрация кислоты, оставшейся в недиссоциированном состоянии, будет равна (С – α С) = С (1 – α). Подставив значения равновесных концентраций ионов и кислоты в уравнение константы равновесия, получим:
|
| 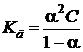 . .
| (7.15)
|
Если степень диссоциации α << 1, то уравнение упрощается:
откуда:
|
|  . .
| (7.17)
|
Уравнения (7.15-7.17) называются законом разбавления Оствальда.
Слабые электролиты подчиняются закону разбавления Оствальда, согласно которому с увеличением концентрации степень диссоциации уменьшается, а константа диссоциации остается неизменной.
Теория сильных электролитов
Константа диссоциации сильных электролитов изменяется с изменением концентрации. С увеличением концентрации сильных электролитов уменьшается величина электропроводности, осмотическое давление и др. Изменение свойств растворов сильных электролитов при высоких концентрациях объясняется с позиций теории сильных электролитов П. Дебая–Э. Хюккел, которая учитывает взаимодействие ионов в растворе. Согласноэтой теории, молекулы сильных электролитов в растворах любой концентрации практически полностью диссоциированы на ионы. Наблюдаемое же понижение электропроводности при повышении концентрации сильных электролитов, объясняется влиянием электростатического взаимодействия ионов. В результате электростатического взаимодействия каждый ион окружен определенным числом ионов противоположного знака (ионной атмосферой). Ионная атмосфера препятствует свободному движению ионов в электрическом поле. В разбавленных растворах сильных электролитов силы электростатического взаимодействия практически отсутствуют из-за большого расстояния между ионами, это выглядит как полная диссоциация.
Для количественной характеристики свойств сильных электролитов вводится понятие активности ионов (а). Активность выражает эффективную концентрацию диссоциированной части электролита в растворе, учитывающей взаимное притяжение разноименных ионов. Она является вспомогательной, расчетной величиной:
где f – коэффициент активности; С – аналитическая концентрация иона (моль/1000 г растворителя).
Величина коэффициента активности зависит от концентрации всех ионов в растворе. Значение f приводится в справочниках. В концентрированных растворах f< 1, с разбавлением раствора f→ 1, при этом а →С.



 ,
,
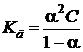 .
.
 .
.

