

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Биохимия спиртового брожения: Основу технологии получения пива составляет спиртовое брожение, - при котором сахар превращается...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Биохимия спиртового брожения: Основу технологии получения пива составляет спиртовое брожение, - при котором сахар превращается...
Топ:
Теоретическая значимость работы: Описание теоретической значимости (ценности) результатов исследования должно присутствовать во введении...
Отражение на счетах бухгалтерского учета процесса приобретения: Процесс заготовления представляет систему экономических событий, включающих приобретение организацией у поставщиков сырья...
Процедура выполнения команд. Рабочий цикл процессора: Функционирование процессора в основном состоит из повторяющихся рабочих циклов, каждый из которых соответствует...
Интересное:
Принципы управления денежными потоками: одним из методов контроля за состоянием денежной наличности является...
Искусственное повышение поверхности территории: Варианты искусственного повышения поверхности территории необходимо выбирать на основе анализа следующих характеристик защищаемой территории...
Подходы к решению темы фильма: Существует три основных типа исторического фильма, имеющих между собой много общего...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
При температуре кипения
Цель работы: определение теплоты фазового перехода первого рода на примере испарения воды.
Теоретическая часть
Переход вещества из одной фазы в другую при изменении внешних условий: температуры, давления, магнитного и электрического полей и т.д. называется фазовым переходом. Значение температуры, давления или какой-либо другой физической величины, при которой происходит фазовый переход, называется точкой перехода.
Различают фазовые переходы двух родов. При фазовом переходе 1-го рода скачком меняются такие термодинамические характеристики вещества, как плотность, концентрация компонентов, а в единице массы вещества выделяется или поглощается вполне определенное количество теплоты, называемое теплотой фазового перехода. Примерами фазовых переходов 1-го рода являются испарение и конденсация, плавление и затвердевание, некоторые структурные переходы в твердых телах, например, образование мартенсита[3] в сплаве железо-углерод (сталь).
При фазовом переходе 2-го рода некоторая физическая величина, равная нулю с одной стороны от точки перехода, постепенно растет (от нуля) при удалении от точки перехода в другую сторону, при этом плотность изменяется непрерывно, теплота не выделяется и не поглощается. К примерам фазовых переходов 2-го рода относятся переход парамагнетик - ферромагнетик или переход металла в сверхпроводящее состояние при температуре ниже критической.
В жидкостях при любой температуре имеется некоторое количество молекул, энергия которых оказывается достаточной для того, чтобы преодолеть притяжение к другим молекулам, покинуть поверхность жидкости и перейти в газообразную фазу. Переход жидкости в газообразное состояние называется испарением. При испарении жидкость покидают наиболее быстрые молекулы, вследствие чего средняя энергия оставшихся молекул уменьшается, и жидкость охлаждается. Чтобы поддерживать температуру испаряющегося тела неизменной, к нему нужно подводить тепло. Количество теплоты, которое необходимо подвести к единице жидкости для превращения ее в пар при постоянной температуре, называется удельной теплотой перехода жидкости в пар. Обычно ее обозначают  и измеряют в Дж/кг.
и измеряют в Дж/кг.
|
|
Теплота, подводимая к жидкости при изотермическом испарении, идет на работу  по преодолению сил молекулярного взаимодействия и на работу
по преодолению сил молекулярного взаимодействия и на работу  , связанную с увеличением объема вещества при переходе его из жидкого состояния в газообразное.
, связанную с увеличением объема вещества при переходе его из жидкого состояния в газообразное.
Работа  при испарении единицы массы будет численно равна разности внутренних энергий пара и жидкости. Так как средние кинетические энергии молекул пара и жидкости одинаковы при постоянной температуре, разность удельных внутренних энергий будет равна разности потенциальных энергий единицы массы пара и жидкости. Согласно теории Ван-дер-Ваальса[4] межмолекулярное взаимодействие приводит к появлению добавочного внутреннего давления, которое равно:
при испарении единицы массы будет численно равна разности внутренних энергий пара и жидкости. Так как средние кинетические энергии молекул пара и жидкости одинаковы при постоянной температуре, разность удельных внутренних энергий будет равна разности потенциальных энергий единицы массы пара и жидкости. Согласно теории Ван-дер-Ваальса[4] межмолекулярное взаимодействие приводит к появлению добавочного внутреннего давления, которое равно:
 , (1)
, (1)
где  - постоянная Ван-дер-Ваальса для единицы массы жидкости,
- постоянная Ван-дер-Ваальса для единицы массы жидкости,  - удельный объем. Тогда работа против сил межмолекулярного взаимодействия при испарении единицы массы жидкости будет равна:
- удельный объем. Тогда работа против сил межмолекулярного взаимодействия при испарении единицы массы жидкости будет равна:
 , (2)
, (2)
где  - удельный объем жидкости,
- удельный объем жидкости, 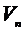 - удельный объем пара. Работу
- удельный объем пара. Работу  , совершаемую против внешнего давления, при испарении единицы массы жидкости найдем по формуле:
, совершаемую против внешнего давления, при испарении единицы массы жидкости найдем по формуле:
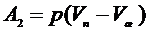 , (3)
, (3)
где p - внешнее давление.
Удельная теплота перехода жидкости в пар равна сумме этих работ:
 . (4)
. (4)
Удельная теплота перехода жидкости в пар зависит от природы жидкости, а для данной жидкости является функцией температуры. С увеличением температуры удельная теплота перехода жидкости в пар убывает. В критическом состоянии различие между жидкостью и ее насыщенным паром исчезает, и удельная теплота перехода обращается а нуль, т.к.  .
.
|
|
Экспериментальная часть
|
|
|

История развития хранилищ для нефти: Первые склады нефти появились в XVII веке. Они представляли собой землянные ямы-амбара глубиной 4…5 м...

Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций...

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!