

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Эмиссия газов от очистных сооружений канализации: В последние годы внимание мирового сообщества сосредоточено на экологических проблемах...
Топ:
Установка замедленного коксования: Чем выше температура и ниже давление, тем место разрыва углеродной цепи всё больше смещается к её концу и значительно возрастает...
Генеалогическое древо Султанов Османской империи: Османские правители, вначале, будучи еще бейлербеями Анатолии, женились на дочерях византийских императоров...
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного...
Интересное:
Подходы к решению темы фильма: Существует три основных типа исторического фильма, имеющих между собой много общего...
Средства для ингаляционного наркоза: Наркоз наступает в результате вдыхания (ингаляции) средств, которое осуществляют или с помощью маски...
Как мы говорим и как мы слушаем: общение можно сравнить с огромным зонтиком, под которым скрыто все...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Вопрос Основные положения теории химического строения А.М. Бутлерова
1. Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. Последовательность межатомных связей в молекуле называется ее химическим строением и отражается одной структурной формулой (формулой строения).
2. Химическое строение можно устанавливать химическими методами. (В настоящее время используются также современные физические методы).
3. Свойства веществ зависят от их химического строения.
4. По свойствам данного вещества можно определить строение его молекулы, а по строению молекулы - предвидеть свойства.
5. Атомы и группы атомов в молекуле оказывают взаимное влияние друг на друга.
Теория Бутлерова явилась научным фундаментом органической химии и способствовала быстрому ее развитию. Опираясь на положения теории, А.М. Бутлеров дал объяснение явлению изомерии, предсказал существование различных изомеров и впервые получил некоторые из них.
Развитию теории строения способствовали работы Кекуле, Кольбе, Купера иВант-Гоффа. Однако их теоретические положения не носили общего характера и служили, главным образом, целям объяснения экспериментального материала.
Вопрос. Предельные углеводороды
Предельные углеводороды - это углеводороды, в молекулах которых имеются только простые (одинарные) связи ( -связи). Предельнымиуглеводородамиявляютсяалканыициклоалканы. Атомыуглеродавпредельныхуглеводородахнаходятсявсостоянииsp3-гибридизации.
-связи). Предельнымиуглеводородамиявляютсяалканыициклоалканы. Атомыуглеродавпредельныхуглеводородахнаходятсявсостоянииsp3-гибридизации.
Алканы - предельные углеводороды, состав которых выражается общей формулой C n H 2n+2. Алканы являются насыщенными углеводородами.
Физические свойства алканов При комнатной температуре С1-C4 - газы, C5-C15 - жидкости, C16 и следующие - твердые вещества; нерастворимы в воде; плотность меньше 1 г/см3; жидкие - с запахом бензина.
С увеличением числа атомов углерода в молекуле возрастает температура кипения.
|
|
Химические свойства алканов Малоактивны в обычных условиях, не реагируют с растворами кислот и щелочей, не обесцвечивают раствор KMnO4 и бромную воду.
-Горение (окисление с разрывом связей C—C и C—H): CH4 + 2O2 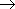 CO2 + 2H2O + Q
CO2 + 2H2O + Q
-Замещение(сразрывомсвязейC—H):
а) галогенирование (только с хлором и с бромом):
1-я стадия: CH4 + Cl2 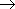 CH3Cl + HCl (при нагревании или на свету).
CH3Cl + HCl (при нагревании или на свету).
При достаточном количестве галогена происходит дальнейшее замещение атомов водорода:
CH4 + HONO2 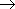
| CH3NO2 нитрометан | + H2O (при нагревании) |
б) нитрование (реакция Коновалова):
Получение алканов
Лабораторные способы:
-Гидролиз карбида алюминия (получение метана): Al4C3 + 12H2O 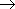 4Al(OH)3 + 3CH4
4Al(OH)3 + 3CH4 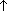
-Реакция обмена: CH3COONa + NaOH 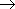 Na2CO3 + CH4
Na2CO3 + CH4 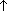 (при нагревании)
(при нагревании)
-Реакция Вюрца: 2CH3Cl + 2Na 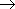 CH3—CH3 + 2NaCl
CH3—CH3 + 2NaCl
Промышленные способы:
-Выделение из природных источников (природного газа, нефти, каменного угля, горючих сланцев).
-Газификация твердого топлива: C + 2H2 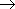 CH4 (при нагревании под давлением в присутствии Ni-катализатора)
CH4 (при нагревании под давлением в присутствии Ni-катализатора)
Циклоалканы - предельные углеводороды, состав которых выражается формулой C n H2 n . В состав молекул циклоалканов входят замкнутые углеродные цепи (циклы).
Химические свойства
За исключением циклопропана и циклобутана циклоалканы, как и алканы, малоактивны в обычных условиях.
Общие свойства циклоалканов (на примере циклогексана):
-горение (окисление с разрывом связей C—C и C—H):
C6H12 + 9O2 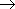 6CO2 + 6H2O + Q
6CO2 + 6H2O + Q
-замещение (галогенирование, нитрование):
C6H12 + Cl2 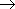 C6H11Cl + HCl (при нагревании или на свету)
C6H11Cl + HCl (при нагревании или на свету)
-присоединение (гидрирование):
C6H12 + H2 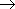 C6H14 (при нагревании под давлением в присутствии Ni-катализатора)
C6H14 (при нагревании под давлением в присутствии Ni-катализатора)
-разложение (дегидрирование, крекинг, пиролиз):
C6H12 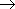 C6H6 + 3H2 (при нагревании с катализатором).
C6H6 + 3H2 (при нагревании с катализатором).
Особые свойства циклопропана и циклобутана (склонность к реакциям присоединения):
|
|
-галогенирование:
 + Br2
+ Br2 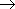 BrCH2—CH2—CH2Br
BrCH2—CH2—CH2Br
-гидрогалогенирование:
 + HBr
+ HBr 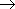 CH3—CH2—CH2Br
CH3—CH2—CH2Br
Способы получения.
Галогенпроизводные получают прямым галогенированием углеводородов реакцией замещения, присоединением галогенов и галогенводородов к алкенам и алкинам, из спирта – реакцией с галогенводородами и галогенидами фосфора и серы.
Фторирование.
Фтор с алканами реагирует очень энергично, даже со взрывом, так как в реакции выделяется много теплоты, поэтому необходимы специальные условия: разбавление фтора азотом, специальная конструкция реакторов с медными сетками для эффективного отвода теплоты реакции. В качестве переносчиков фтора используют фториды металлов (СоF2.AgF, MnF2). Под действием фтора образуются CoF3, AgF2, MnF4, которые фторируют алканы. Реакция протекает по свободнорадикальному механизму:
СН4 → CH3F + CoF3
Таким методом можно получить хлор-, фтор- и бромуглеводороды. Прямое иодированиеалканов неизвестно. Методы являются промышленными. Бромирование.
Прямоебромирование для простейших алканов (метан, этан) малохарактерно. В принципе бромирование возможно при нагревании и интенсивном облучении УФ-светом. Для гексана, гептана и других алканов возможно бромирование при кипячении и освещении:
Реакции замещения.
Применение
Важной особенностью аминокислот является их способность к поликонденсации, приводящей к образованию полиамидов, в том числе пептидов, белков, нейлона, капрона, энанта.
Аминокислоты входят в состав спортивного питания и комбикорма. Аминокислоты применяются в пищевой промышленности в качестве вкусовых добавок, например, натриевая соль глутаминовой кислоты[4].
14. Моносахариды: классификация, номенклатура, физические и химические св-ва,практическое применение.
Моносахариды (от греческого monos: единственный, sacchar: сахар), — органические соединения, одна из основных групп углеводов; самая простая форма сахара; являются обычно бесцветными, растворимыми в воде, прозрачными твердыми веществами. Некоторые моносахариды обладают сладким вкусом. Моносахариды — стандартные блоки, из которых синтезируются дисахариды (такие, как сахароза, мальтоза, лактоза), олигосахариды и полисахариды (такие, как целлюлоза и крахмал), содержат гидроксильные группы и альдегидную(альдозы) или кетогруппу (кетозы). Каждый углеродный атом, с которым соединена гидроксильная группа (за исключением первого и последнего), является хиральным, что дает начало многим изомерным формам. Например, галактоза и глюкоза — альдогексозы, но имеют различные химические и физические свойства. Моносахариды представляют собой производные многоатомных спиртов, содержащие карбонильную группу — альдегидную или кетонную[1].
|
|
Виды моносахаридов
Моносахариды подразделяют на триозы, тетрозы, пентозы, гексозы и т. д. (3, 4, 5, 6 и т. д. атомов углерода в цепи); природные моносахариды с углеродной цепью, содержащей более 9 атомов углерода, не обнаружены. Моносахариды, содержащие 5-членный цикл, называются фуранозами, 6-членный — пиранозами.
Для моносахаридов, содержащих n асимметричных атомов углерода, возможно существование 2n стереоизомеров
Классификация моносахаридов
Не все следующие монозы найдены в природе, некоторые были синтезированы:альдоза,кетоза.
Химические свойства
Моносахариды вступают в химические реакции, свойственные карбонильной и гидроксильной группам. Характерная особенность моносахаридов — способность существовать в открытой (ациклической) и циклической формах и давать производные каждой из форм. Большинство моноз циклизуются в водном растворе с образованием гемиацеталей илигемикеталей (в зависимости от того, являются ли они альдозами или кетозами) между спиртом и карбонильной группой того же самого сахара. Глюкоза, например, легко образуетполуацетали, соединяя свои своим С1 и О5, чтобы сформировать 6-членное кольцо, названное пиранозид. Та же самая реакция может иметь место между С1 и О4, чтобы сформировать 5-членное фуранозид.
Применение
Некоторые свободные моносахариды и их производные (например, глюкоза, фруктоза и её дифосфат и др.) используются в пищевой промышленности и медицине.
ПОЛУЧЕНИЕ ТИОЛОВ
Тиоэфиры получают взаимодействием галогеналкилов с неорганическими сульфидами (рис. 6А). Когда нужно получить тиоэфиры с различающимися органическими группами, проводят взаимодействие галогеналкилов с тиолятами щелочных металлов (рис. 6Б), либо присоединением тиолов к олефинам (рис. 6В). О В некоторых простых эфирах, имеющих циклическое строение, можно заменить атом О атомом S, при этом образуется циклический тиоэфир, например, тиофен, который относят к гетероциклическим соединениям
|
|

Применение сераорганических соединений.
При автоокислении многих органических соединений возникают свободные радикалы (соединения, содержащие неспаренный электрон у атома углерода), которые далее ведут цепной процесс окисления. Тиолы и тиоэфиры используют как эффективные ловушки свободных радикалов, при этом они окисляются подобно тому, как показано на рис. 1Б и 2В. Это свойство позволяет использовать ихв качестве стабилизаторов, защищающих моторные топлива и масла от окисления. Для стабилизации каучуков используют трудно испаряющиеся соединения, например, додекантиол С12Н23SH.
Свойство тиолов «гасить» свободные радикалы нашло применение в создании радиопротекторов – веществ, защищающих от радиоактивного излучения. Для этих целей используют различные аминотиолы и их производные, например, H2N(CH2)n S H.
Радиопротекторы вводят в организм до облучения перед радиотерапевтическим лечением в медицине при долговременных космических полетах для защиты от солнечных вспышек. В результате заметно снижается доза полученной радиации.
На основе сераорганических соединений, содержащих дисульфидные группировки – S – S –, созданы полимеры – полисульфидные каучуки (промышленное название – тиоколы), которые получают поликонденсацией дигалогенпроизводных алифатических соединений Cl–R–Cl [R = (CH2)2, (CH2)3] и дисульфида натрия Na2S2, в результате образуются полисульфиды [–R–S–S–]n. Такие каучуки при добавлении окислителей (например, бихроматов) образуют сшитые резиноподобные материалы – вулканизаты, которые по прочности уступают обычным каучукам, но превосходят их по бензо- и маслостойкости, а также по атмосферостойкости, они не теряют механических свойств при действии влаги, смене температур и воздействии солнечной радиации. Это позволяет применять их при изготовлении бензо- и маслопроводов как внутренние покрытия резервуаров для хранения топлива, для герметизации швов между бетонными панелями при строительстве домов и к
СТРОЕНИЕ
Белки — это природные полипептиды с высокими значениями молекулярной массы (от 10 000 до десятков миллионов). Они входят в состав всех живых организмов и выполняют разнообразные биологические функции.
Можно выделить четыре уровня в строении полипептидной цепи. Первичная структура белка - это конкретная последовательность аминокислот в полипептидной цепи.
Вторичная структура - это конформация полипептидной цепи, т.е. способ скручивания цепи в пространстве за счет водородных связей между группами NH и СО. Существует два основных способа укладки цепи — α-спираль и β-структура.В α-спирали на одном витке укладывается четыре аминокислотных остатка. В β-структуре (складчатом слое) полипептидная цепь растянута, ее участки располагаются параллельно друг другу и удерживаются водородными связями
|
|
Третичная структура белка — это трехмерная конфигурация закрученной α-спирали или β-структуры в пространстве. Третичная структура образуется за счет дисульфидных мостиков -S-S- между цистеиновыми остатками, находящимися в разных местах полипептидной цепи. В образовании третичной структуры участвуют также ионные взаимодействия противоположно заряженных групп NН3+ и СОО- и гидрофобные взаимодействия, т.е. стремление молекулы белка свернуться так, чтобы гидрофобные углеводородные остатки оказались внутри структуры. Третичная структура — высшая форма пространственной организации белков. Однако, некоторые белки (например, гемоглобин) имеют четвертичную структуру, которая образуется за счет взаимодействия между разными полипептидными цепями.
Четвертичная структура белка — тип взаимодействия между несколькими полипептидными цепями. Четвертичная структура белков. Например, гемоглобин представляет из себя комплекс из четырех макромолекул белка.
ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА, ЗНАЧЕНИЕ
Физические свойства белков весьма разнообразны и определяются их строением. По физическим свойствам белки делят на два класса: глобулярные белки растворяются в воде или образуют коллоидные растворы, фибриллярные белки в воде нерастворимы.
Химические свойства. 1. Разрушение вторичной и третичной структуры белка с сохранением первичной структуры называется денатурацией. Она происходит при нагревании, изменении кислотности среды, действии излучения. Пример денатурации - свертывание яичных белков при варке яиц. Денатурация бывает обратимой и необратимой. Необратимая денатурация может быть вызвана образованием нерастворимых веществ при действии на белки солей тяжелых металлов — свинца или ртути.
2. Гидролиз белков — это необратимое разрушение первичной структуры в кислом или щелочном растворе с образованием аминокислот. Анализируя продукты гидролиза, можно установить количественный состав белков.
3. Для белков известны несколько качественных реакций. Все соединения, содержащие пептидную связь, дают фиолетовое окрашивание при действии на них солей меди (II) в щелочном растворе. Эта реакция называется биуретовой. Белки, содержащие остатки ароматических аминокислот (фенилаланина, тирозина) дают желтое окрашивание при действии концентрированной азотной кислоты (ксантопротеиновая реакция).
Биологическое значение белков чрезвычайно велико. Упомянем только важнейшие функции белков в живых организмах.
1. Абсолютно все химические реакции в организме протекают в присутствии катализаторов — ферментов. Даже такая простая реакция как гидратация углекислого газа катализируется ферментом карбоангидразой. Все известные ферменты представляют собой белковые молекулы. Белки — это очень мощные и, самое главное, селективные катализаторы. Они ускоряют реакции в миллионы раз, причем для каждой реакции существует свой единственный фермент.
2. Некоторые белки выполняют транспортные функции и переносят молекулы или ионы в места синтеза или накопления. Например, содержащийся в крови белок гемоглобин переносит кислород к тканям, а белок миоглобин запасает кислород в мышцах.
3. Белки — это строительный материал клеток. Из них построены опорные, мышечные, покровные ткани.
4. Белки играют важную роль в иммунной системе организма.Существуют специфические белки (антитела), которые способны распознавать и связывать чужеродные объекты - вирусы, бактерии, чужие клетки.
5. Белки-рецепторы воспринимают и передают сигналы, поступающие от соседних клеток или из окружающей среды. Например, действие света на сетчатку глаза воспринимается фоторецептором родопсином. Рецепторы, активизируемые низкомолекулярными веществами типа ацетилхолина, передают нервные импульсы в местах соединения нервных клеток.
Из приведенного перечня функций белков ясно, что белки жизненно необходимы любому организму и являются, следовательно, важнейшей составной частью продуктов питания. В процессе пищеварения белки гидролизуются до аминокислот, которые служат исходным сырьем для синтеза белков, необходимых данному организму. Существуют аминокислоты, которые организм не в состоянии синтезировать сам и приобретает их только с пищей. Эти аминокислоты называются незаменимыми. Для человека незаменимы триптофан, лейцин, изолейцин, валин, треонин, лизин, метионин и фенилаланин.
16.Дисахариды – это углеводы, которые при нагревании с водой в присутствии минеральных кислот или под влиянием ферментов подвергаются гидролизу, расщепляясь на две молекулы моносахаридов.
Классификация. Дисахариды состоят из двух остатков моносахаридов, соединенных между собой О-гликозидной связью. Если один полуацетальный гидроксил остается свободным, а дисахариды проявляют альдегидные свойства, то такие дисахариды называются восстанавливающими. Если же связь между двумя остатками моносахаридов осуществляется посредством обоих полуацетальных гидроксилов, то для таких дисахаридов альдегидные свойства не характерны и они называются невосстанавливающими.
Гидролиз дисахаридов протекает достаточно легко в связи с тем, что связь между моносахаридными звеньями ацетальная.
17. АЛЬДЕГИДЫ И КЕТОНЫ – органические соединения содержащие фрагмент >C=O (углерод, связанный двойной связью с кислородом, его называют карбонильным).
Химические свойства альдегидов и кетонов определяются особенностями карбонильной группы >C=O, обладающей полярностью – электронная плотность между атомами С и О распределена неравномерно, сдвинута к более электроотрицательному атому О. В результате карбонильная группа приобретает повышенную реакционную способность, что проявляется в разнообразных реакциях присоединения по двойной связи. Во всех случаях кетоны менее реакционноспособны, чем альдегиды, в частности, из-за пространственных затруднений, создаваемых двумя органическими группами R, наиболее легко участвует в реакциях формальдегид Н2С=О.
Применение альдегидов и кетонов. Формальдегид Н2С=О (его водный раствор называют формалином) используют как дубитель кожи и консервант биологических препаратов.
Ацетон (СН3)2С=О – широко применяемый экстрагент и растворитель лаков и эмалей.
Алифатический альдегид СН3(СН2)7С(Н)=О (тривиальное название – пеларгоновый альдегид) содержится в эфирных маслах цитрусовых растений, обладает запахом апельсина, его используют как пищевой ароматизатор.
18.МОЮЩИЕ СРЕДСТВА
(детергенты) - вещества, усиливающие моющее действие воды. Первыми детергентами были мыла, полученные из встречающихся в природе веществ. Но сейчас под детергентами обычно понимают синтетические вещества, по моющему действию сходные с мылом. Синтетические моющие средства используются в быту, в промышленности их применяют для отбеливания текстиля, при крашении и аппретировании тканей, на стадиях очистки и травления металлов, для стерилизации оборудования в пищевой промышленности, а также в производстве косметики. Наиболее распространенные синтетические моющие средства - сульфонаты натрия. Существуют их многочисленные разновидности, несколько различающиеся по свойствам. Для специальных целей используются и другие соединения. Использование мыла всегда осложняется, если вода жесткая. При стирке в ней приходится расходовать много мыла, чтобы достичь ощущения "мылкости". Это объясняется присутствием в воде солей типа гидрокарбоната кальция, которые реагируют с мылом, образуя нерастворимые соединения. Лишь после того как растворенные соли удалены реакцией с мылом, прибавление дополнительных количеств мыла приводит к проявлению его моющих свойств. Если после стирки мылом прополоскать ткань в жесткой воде, на ней осаждается нерастворимое и трудно удалимое "кальциевое мыло", которое портит ее вид.
19.ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ – один из самых многочисленных классов органических соединений (см. ОРГАНИЧЕСКАЯ ХИМИЯ), они содержат в составе углеводородного цикла они содержат один или несколько гетероатомов: O, N, S
Классификация гетероциклических соединений. В зависимости от природы гетероатома различают кислород-, азот- и серосодержащие соединения. Существуют и соединения, в составе которых есть одновременно несколько одинаковых (рис. 2, диоксан) или различных гетероатомов (рис. 2, тиазол, оксазин). Кроме того, их делят на насыщенные соединения (рис. 1, пиперидин) и ненасыщенные, т.е. содержащие кратные связи (рис. 1, фуран, пиридин, тиофен). В зависимости от числа циклических фрагментов в молекуле различают моноядерные – моноциклические соединения (рис. 1) и полиядерные – содержащие несколько циклов, причем циклы могут быть конденсированные (содержать два общих атома, рис. 2, индол), либо соединенные простой связью (рис. 2, бипиридил). В особую группу выделяют макроциклические соединения, так называемые краун-эфиры (crown англ. – корона), содержащие свыше четырех гетероатомов и более десяти звеньев в структуре цикла (звеном называют фрагмент из двух химически связанных атомов
Химические свойства гетероциклических соединений. Трех- и четырехчленные гетероциклы представляют собой напряженные системы, для них характерны реакции с раскрытием цикла. Этиленоксид (при 150° С и давлении 2 мПа) гидролизуется, образуя этиленгликоль (рис. 4А). Реакция О-содержащих напряженных циклов со спиртами приводит к соединениям с ОН-группой и простой эфирной связью (целлозольвы, рис. 4Б), а при действии на них галогенводородов образуются соединения, содержащие Hal и ОН-группу (галогенгидрины, рис. 4В). N-содержащие напряженные циклы, взаимодействуя с галогеноводородами образуют галогеналкиламины
Нитросоединения
Нитросоединения — органические соединения, содержащие одну или несколько нитрогрупп —NO2. Под нитросоединениями обычно подразумевают C-нитросоединения, в которых нитрогруппа связана с атомом углерода. O-нитросоединения и N-нитросоединения выделяют в отдельные классы — нитроэфиры (органические нитраты) и нитрамины[1].
В зависимости от радикала R, различают алифатические (предельные и непредельные), ациклические, ароматические и гетероциклические нитросоединения. По характеру углеродного атома, с которым связана нитрогруппа, нитросоединения подразделяются на первичные, вторичные и третичные.
Нитрогруппа имеет строение, промежуточное между двумя предельными резонансными структурами:

Физические свойства. Простейшие нитроалканы-бесцв. жидкости. Физ. св-ва нек-рых алифатических нитросоединений приведены в таблице. Ароматические нитросоединения-бесцв. или светло-желтые высококипящие жидкости или низкоплавкие твердые в-ва, обладающие характерным запахом, плохо раств. в воде, как правило, перегоняются с паром.
Химические свойства
По химическому поведению нитросоединения обнаруживают определенное сходство с азотной кислотой. Это сходство проявляется при окислительно-восстановительных реакциях.
· Восстановление нитросоединений (Реакция Зинина):

· Реакции конденсации
· Таутомерия нитросоединений.
Применение. Поли-нитросоединения, особенно ароматические, применяют в качестве взрывчатых веществ и в меньшей степени как компонентыракетных топлив. Алифатические нитросоединения используют как р-рители в лакокрасочной пром-сти и в произ-ве полимеров, в частности эфиров целлюлозы; для очистки минер. масел; депарафинизации нефти и др.
Ряд нитросоединений находят применение в качестве биологически активных в-в. Так, эфиры фосфорной к-ты, содержащие нитроарильный фрагмент,-инсектициды; производные 2-нитро-1,3-пропандиола и 2-нитростирола - фунгициды; производные 2,4-динитрофенола - гербициды; a-нитрофураны -важнейшие антибактериальные препараты, на их основе созданы лекарства, обладающие широким спектром действия (фуразолидин и др.). Нек-рые ароматические нитросоединения-душистые в-ва.
Нитросоединения- полупродукты в произ-ве синтетич. красителей, полимеров, моющих препаратов и ингибиторов коррозии; смачивающих, эмульгирующих, диспергирующих и флотац. агентов; пластификаторов и модификаторов полимеров, пигментов и пр. Они находят широкое применение в орг. синтезе и в качестве модельных соед. в теоретич. орг. химии.
26.Органические соединения фосфора

Фосфорорган и ческие соедин е ния, обширный класс органических соединений, содержащих в своём составе фосфор. Различают Ф. с., в молекулах которых фосфор непосредственно связан с углеродом, и Ф. с., в которых фосфор связан с органической частью молекулы через гетероатом – кислород, азот, серу (это главным образом эфиры и др. производные кислот фосфора). Ф. с. второго типа широко распространены в природе преимущественно в виде эфиров фосфорной, пирофосфорной и трифосфорной кислот (см.Фосфорные кислоты); к ним относятся нуклеиновые кислоты, многие важные коферменты, аденозинтрифосфат (см. Аденозинфосфорные кислоты) – переносчик энергии в живых организмах, некоторые витамины. В 60-е гг. 20 в. в природе были найдены Ф. с., содержащие связь фосфор – углерод, например (b-аминоэтилфосфоновая кислота (цилиатин).
Применение. Ф. с. используются в технике, сельском хозяйстве, медицине, а также в научных исследованиях. Больших масштабов достигло производство фосфорорганических пестицидов(инсектицидов, акарицидов, дефолиантов и др.). Однако, отличаясь высокой эффективностью, пестициды в большинстве своём токсичны для людей и животных, поэтому их применение требует мер предосторожности; вместе с тем они не накапливаются во внешней среде и тем выгодно отличаются от пестицидов др. типов. В медицине Ф. с. используются главным образом в офтальмологии; большое значение имеют также биологически важные фосфаты, например аденозинтрифосфат, кокарбоксилаза, ряд витаминов. Как комплексообразователи Ф. с. употребляют в экстракционном обогащении руд (в производстве урана и др. металлов). Многие Ф. с. применяют в качестве присадок к смазочным маслам, повышающих их эксплуатационные свойства (см. Присадки), компонентов пластмасс и волокон, придающих негорючесть (т. н. антипиренов), растворителей, гидравлических жидкостей и др. Получила развитие также область фосфорорганических комплексонов, используемых для разделения, например, металлов и для др. целей.
Получение. В синтезе Ф. с. большое значение имеют методы образования связи С–Р. К ним относятся: Арбузова реакция: (PO)3P + R’X (R’PO (OR)2 + RX; реакция Михаэлиса – Беккера: (RO)2PONa + R’X (R’PO (OR)2 + NaX; синтезы с металлоорганическими соединениями, например: PСl3 + SRMgX (R3P + 3MgXCl; фосфорилирование по типу реакции Фриделя – Крафтса: С6H6 + PСl3  С6H5PСl2 + HСl; присоединение пятихлористого фосфора к олефинам: С6H5СH = СH2 + 2PCl5 (C6H5CHCl – СH2PСl4×PCl5; алкилирование элементарного фосфора, например: 3RCl + 2P
С6H5PСl2 + HСl; присоединение пятихлористого фосфора к олефинам: С6H5СH = СH2 + 2PCl5 (C6H5CHCl – СH2PСl4×PCl5; алкилирование элементарного фосфора, например: 3RCl + 2P  RPCl2 + R2PCl
RPCl2 + R2PCl
24 вопрос.Фенол
ФЕНОЛЫ – класс органических соединений. Содержат одну или несколько группировок С–ОН, при этом атом углерода входит в состав ароматического (например, бензольного) кольца.
Химические свойства фенола
Фенол представляет собой кристаллическое вещество белого цвета, с характерным резким сладковато-приторным запахом, которое легко окисляется при взаимодействии с воздухом, приобретая сначала розоватый, а спустя некоторое время насыщенный бурый цвет. Особенностью фенола является прекрасная растворимость не только в воде, но и в спирте, щелочной среде, бензоле и ацетоне. Кроме этого, фенол обладает очень низкой температурой плавления и легко переходит в жидкое состояние при температуре +42°C, а также имеет слабые кислотные свойства. Поэтому при взаимодействии со щелочами фенол образует соли, именуемые фенолятами.
Способы получения фенола
В чистом виде в природе фенол не встречается, он является искусственным продуктом органической химии. В настоящее время существует три основных способа получения фенола в промышленных объемах. --Основная доля его производства приходится на так называемый кумпольный метод, который подразумевает окисление воздухом ароматического органического соединения изопропилбензола. --Для производства также используется метилбензол (толуол), в результате окисления которого образуется данное химическое вещество и бензойная кислота. Кроме этого, в некоторых видах промышленности, таких, как производство металлургического кокса, фенол выделяется из каменноугольной смолы. Однако этот способ получения является нерентабельным из-за повышенной энергоемкости. Среди последних достижений химической промышленности – получение фенола путем взаимодействия бензола и уксусной кислоты, а также окислительное хлорирование бензола.
Область применения фенола \Первоначально фенол использовался для производства различного рода красителей, благодаря своему свойству изменять цвет в процессе окисления с бледно-розового до бурого оттенка. Это химическое вещество вошло в состав многих видов синтетических красок. Кроме этого, свойство фенола уничтожать бактерии и микроорганизмы, было взято на вооружение в кожевенном производстве при дублении шкур животных. Позже фенол успешно использовался в медицине как одно из средств обеззараживания и дезинфекции хирургических инструментов и помещений, а в качестве 1,4-процентного водного раствора - как болеутоляющее и антисептик для внутреннего и наружного применения. В настоящее время основное предназначение фенола – химическая промышленность, где это вещество применяется для изготовления пластмассы, фенолформальдегидных смол, таких искусственных волокон, как капрон и нейлон, а также различных антиоксидантов. Кроме этого, фенол применяется для производства пластификаторов, присадок для масел, является одним из компонентов, входящих в состав препаратов по защите растений.
Вопрос
1я группа
Эти соединения обычно представляют собой бесцветные порошкообразные, иногда микрокристаллические вещества, чрезвычайно легко окисляющиеся, на воздухе самовоспламеняющиеся, бурно, иногда со взрывом, реагирующие с водой.
Как показал П. П. Шорыгин, натрийалкилы являются промежуточными продуктами в реакции Вюрца (см. также реакцию Вюрца—Фиттига):
Натрийалкилы реагируют даже с простыми эфирами:
Аналогичны натрийорганическим соединениям по свойствам и поведению литийорганические соединения, которые в последние годы употребляются вместо магнийорганических соединений там, где надо применить более энергично действующий реагент. Изорганических соединений других металлов первой группы получены соединения калия, цезия, рубидия и даже крайне непрочное соединение одновалентной меди C2H5Cu.
Этиллитий C2H5Li образует прозрачные, растворимые в бензоле шестиугольные таблички с т. пл. 95° С.
2я Группа
Для металлов второй группы возможны как симметрические полные металлоорганические соединения, так и смешанные. Последние обычно представляют собой неперегоняющиеся вещества, способные (например, в случае магния) давать кристаллические соединения с эфирами. В этой группе наиболее важны смешанные магнийорганические соединения, применяемые для различных реакций в виде эфирных растворов, а также цинкорганические соединения.
5. Непредельные углеводороды — углеводороды с открытой цепью, в молекулах которых между атомами углерода имеются двойные или тройные связи. Непредельные углеводороды способны к реакциям присоединения по двойным и тройным связям в открытой цепи. Они, например, присоединяют бром, легко окисляются растворомперманганата калия. Для многих непредельных углеводородов характерны реакции полимеризации. К непредельным углеводородам принадлежит несколько гомологических рядов: этилена (алкены), ацетилена (алкины), диены.
Алкенами называются углеводороды с двойной связью. Гомо-
логический ряд алкенов начинается этиленом (по номенклатуре
ИЮПАК— этеном):
CH2 CH2 C2H4 этилен (этен)
CH2 CH CH3 или C3H6 пропилен (пропен)
CH2 CH CH2 CH3 или C4H8 бутен-1
CH2 CH CH2 CH2 CH3 или C5H10 пентен-1
и т. д.
В молекулах алкенов только одна двойная связь. В этом слу-
чае атомов водорода ровно вдвое больше, чем атомов углерода,
поэтому общая формула гомологического ряда алкенов CnH2n. Если
двойных связей две, три или больше, такие соединения выделяют
в отдельные классы диенов, триенов и т. д. (в общем случае —
полиенов). Химические свойства полиенов обычно отличаются от
свойств алкенов, поскольку двойные связи способны влиять друг
на друга — в этом мы убедимся уже в следующем параграфе.
Изомерия алкенов более разнообразна по сравнению с алканами,
и причина тому — наличие двойной связи. К изомерии углеродного
скелета добавляется изомерия положения кратной связи.
алкены-1 образуют гомологический ряд, в ко-
тором наблюдается закономерное изменение физических свойств по
мере увеличения длины цепи. Гомологической разностью является
фрагмент СН2.
способы
введения двойной связи в остовы углеводородов.
1. Термический крекинг алканов. Этот способ используется
в промышленности. Газообразныеалканы, разбавленные водяным
паром, пропускают через нагретые трубки при температуре около
800◦С. Время пребывания реагентов в реакторе-трубке должно быть
очень небольшим, иначе образующиеся продукты вступят в даль-
нейшие реакции. Крекинг протекает по радикальному механизму.
При крекинге происходят реакции разрыва связей СС и дегид-
Рирования
2. Взаимодействие галогеналканов со спиртовымраство-
ром щелочи или дегидрогалогенирование. «Гидрогалогены»— это
переиначенное название галогенводородов НХ, где Х — F, Cl, Br, I.
Следовательно, дегидрогалогенирвание — это отщепление атома га-
логена и атома Н из соединений типа R Х (галогеналканов) под
действием спиртового (но не водного!) раствора щелочи.
Физические свойства
Этен (этилен) СН2 = СН2, - бесцветный газ со слабым запахом;
ЭТИЛЕН (этен) СН2 = СН2, мол. м. 28,05; бесцв. газ со слабым запахом; т. пл. -169,15 °С, т. кип. -103,71 °С;  0,566; tкрит 9,2 °С, ркрит 5,042 МПа;
0,566; tкрит 9,2 °С, ркрит 5,042 МПа;  (жидкости) 0,161 мПа х с;
(жидкости) 0,161 мПа х с;  (жидкости) 16,4 мН/м; давление пара (кПа): 4110 (0 °С), 2200 (-25 °С), 151 (-100 °С); Ср 62,16 Дж/(моль х К) (-193 °С);
(жидкости) 16,4 мН/м; давление пара (кПа): 4110 (0 °С), 2200 (-25 °С), 151 (-100 °С); Ср 62,16 Дж/(моль х К) (-193 °С);  -140
-140
|
|
|

Наброски и зарисовки растений, плодов, цветов: Освоить конструктивное построение структуры дерева через зарисовки отдельных деревьев, группы деревьев...

Своеобразие русской архитектуры: Основной материал – дерево – быстрота постройки, но недолговечность и необходимость деления...

Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ - конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой...

История создания датчика движения: Первый прибор для обнаружения движения был изобретен немецким физиком Генрихом Герцем...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!