

Адаптации растений и животных к жизни в горах: Большое значение для жизни организмов в горах имеют степень расчленения, крутизна и экспозиционные различия склонов...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...

Адаптации растений и животных к жизни в горах: Большое значение для жизни организмов в горах имеют степень расчленения, крутизна и экспозиционные различия склонов...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...
Топ:
Комплексной системы оценки состояния охраны труда на производственном объекте (КСОТ-П): Цели и задачи Комплексной системы оценки состояния охраны труда и определению факторов рисков по охране труда...
Определение места расположения распределительного центра: Фирма реализует продукцию на рынках сбыта и имеет постоянных поставщиков в разных регионах. Увеличение объема продаж...
Интересное:
Уполаживание и террасирование склонов: Если глубина оврага более 5 м необходимо устройство берм. Варианты использования оврагов для градостроительных целей...
Лечение прогрессирующих форм рака: Одним из наиболее важных достижений экспериментальной химиотерапии опухолей, начатой в 60-х и реализованной в 70-х годах, является...
Инженерная защита территорий, зданий и сооружений от опасных геологических процессов: Изучение оползневых явлений, оценка устойчивости склонов и проектирование противооползневых сооружений — актуальнейшие задачи, стоящие перед отечественными...
Дисциплины:
|
из
5.00
|
Заказать работу |
Вопросы для подготовки к занятию
1. Обратимые и необратимые реакции. Условия необратимости реакций.
2. Константа равновесия.
3. Факторы, влияющие на смещение равновесия. Принцип Ле Шателье.
4. Изучение влияния различных факторов на смещение химического равновесия
Состояние системы, при котором скорости прямой и обратной реакции равны, называют химическим равновесием. Состояние равновесия характеризуют константой равновесия (Кр).
Гомогенная система:
2SO2 (г) + O2 (г)  2SO3(г)
2SO3(г) 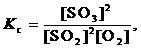
где [ ] – равновесные концентрации веществ.
Гетерогенная система:
Fe2O3 (т) + 3H2 (г)  3 Fe (т) + 3H2O (г)
3 Fe (т) + 3H2O (г) 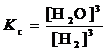 .
.
В выражение константы равновесия гетерогенной реакции, как и в выражение закона действия масс, входят только концентрации веществ, находящихся в жидкой или газообразной фазе, так как концентрации твёрдых веществ остаются, как правило, постоянными.
Принцип Ле Шателье. На состояние равновесия системы влияют давление, концентрация реагирующих веществ и температура. Система может находиться в состоянии равновесия бесконечно долго. Если изменить условия его существования, равновесие будет нарушено. Со временем установится новое состояние равновесия, но с другими равновесными концентрациями. Переход из одного равновесного состояния в другое называют смещением равновесия. Качественно определить направление смещения равновесия позволяет принцип Ле Шателье (1884): если находящаяся в истинном равновесии система подвергается внешнему воздействию, равновесие смещается в направлении, которое способствует ослаблению этого воздействия.
 Пример 1. Для реакции N2 (г) + 3H2 (г)
Пример 1. Для реакции N2 (г) + 3H2 (г)  2NH3 (г) при изменении параметров равновесие смещается: 1) с увеличением
2NH3 (г) при изменении параметров равновесие смещается: 1) с увеличением 
 2) с увеличением Р
2) с увеличением Р
Пример 2. В системе А(г) + 2В(г)  D(г) равновесные концентрации, моль/л: [A] = 0,06; [B] = 0,12; [D] = 0,216. Найти константу равновесия реакции и исходные концентрации веществ А и В.
D(г) равновесные концентрации, моль/л: [A] = 0,06; [B] = 0,12; [D] = 0,216. Найти константу равновесия реакции и исходные концентрации веществ А и В.
Решение. Константа равновесия данной реакции выражается уравнением

Обозначим исходные концентрации веществ С 0, концентрации прореагировавших веществ – С прор; С 0 = С прор + [ ].
Согласно уравнению реакции
С А прор = [D], С А0 = С А прор + [А] = 0,216 + 0,06 = 0,276 моль/л.
С В прор =2 [D], С В0 = С В прор + [В] =2× 0,216 + 0,12 = 0,552 моль/л
Упражнения
1. При синтезе аммиака в равновесии находится 1 моль водорода, 2 моль азота и 8 моль NH3. Во сколько раз исходное количество N2 больше равновесного?
2. В замкнутом сосуде протекает обратимый процесс диссоциации
PCl5 (г)  PCl3 (г) + Cl2 (г). Начальная концентрация PCl5равна 2,4 моль/л. Равновесие установилось после того, как 33,3% PCl5 продиссоциировало. Вычислить равновесные концентрации всех веществ и Кс.
PCl3 (г) + Cl2 (г). Начальная концентрация PCl5равна 2,4 моль/л. Равновесие установилось после того, как 33,3% PCl5 продиссоциировало. Вычислить равновесные концентрации всех веществ и Кс.
3. В сосуде емкостью 1 л при 410 оС смешали 1 моль H2 и 1 моль I2.Вычислить, при каких концентрациях устанавливается химическое равновесие, если константа равновесия равна 48.
4. В сосуде объемом 0,5 л находятся 0,5 моль H2 и 0,5 моль N2. При некоторой температуре к моменту установления равновесия образовалось
0,02 моль NH3. Вычислить константу химического равновесия.
5. В обратимой реакции CO (г) + Cl2 (г)  COCl2 (г) установились следующие равновесные концентрации веществ, моль/л: [CO] = 0,1; [Cl2] = 0,4; [COCl2] = 4. Вычислить К равн и исходные концентрации Cl2 и CO.
COCl2 (г) установились следующие равновесные концентрации веществ, моль/л: [CO] = 0,1; [Cl2] = 0,4; [COCl2] = 4. Вычислить К равн и исходные концентрации Cl2 и CO.
6. Определить объемный состав смеси в момент равновесия для системы
Cграфит + O2 (г)  CO2 (г), если при 1300 оС К с = 0,289.
CO2 (г), если при 1300 оС К с = 0,289.
7. Равновесие в системе CO(г) + H2O(г)  H2(г) + CO2(г) установилось при следующих концентрациях веществ, моль/л: [CO] = 0,04; [H2O] = 0,08; [CO2] = 0,08. Вычислить К c и начальные концентрации CO и H2O.
H2(г) + CO2(г) установилось при следующих концентрациях веществ, моль/л: [CO] = 0,04; [H2O] = 0,08; [CO2] = 0,08. Вычислить К c и начальные концентрации CO и H2O.
8. Константа равновесия системы 2N2 (г) + O2 (г)  2N2O (г) равна 1,21. Равновесные концентрации, моль/л: [N2] = 0,72; [N2O] = 0,84. Рассчитать исходную и равновесную концентрации кислорода.
2N2O (г) равна 1,21. Равновесные концентрации, моль/л: [N2] = 0,72; [N2O] = 0,84. Рассчитать исходную и равновесную концентрации кислорода.
9. Равновесие в системе CO (г) + H2O (г)  H2 (г) + CO2 (г) установилось при сле-дующих концентрациях веществ, моль/л: [CO] = 1; [H2O] = 4; [H2] = [CO2] = 2. Вычислить равновесные концентрации, которые установились после повышения концентрации CO в три раза. В каком направлении сместится равновесие?
H2 (г) + CO2 (г) установилось при сле-дующих концентрациях веществ, моль/л: [CO] = 1; [H2O] = 4; [H2] = [CO2] = 2. Вычислить равновесные концентрации, которые установились после повышения концентрации CO в три раза. В каком направлении сместится равновесие?
10. Рассчитать константу равновесия реакции CO(г) + Cl2 (г)  COCl2 (г), если исходные концентрации CO и Cl2 составляли 4 моль/л, а равновесная концентрация COCl2 равна 2 моль/л.
COCl2 (г), если исходные концентрации CO и Cl2 составляли 4 моль/л, а равновесная концентрация COCl2 равна 2 моль/л.
11. Равновесие в системе 2CO (г) + O2 (г)  2CO2 (г) установилось при следующих концентрациях веществ, моль/л: [CO] = 1,2; [O2] = 0,1; [CO2] = 4. Вычислить исходную концентрацию CO.
2CO2 (г) установилось при следующих концентрациях веществ, моль/л: [CO] = 1,2; [O2] = 0,1; [CO2] = 4. Вычислить исходную концентрацию CO.
12. Определить направление смещения равновесия при увеличении давления в системе 2CO (г)  2CO2 (г) + С(г). Ответ пояснить.
2CO2 (г) + С(г). Ответ пояснить.
13. Константа равновесия процесса CO (г) + Cl2 (г)  COCl2 (г) при определенных условиях равна 4. Равновесные концентрации веществ составляют, моль/л: [Cl2] = 0,5; [COCl2] = 2. Определить равновесную концентрацию CO.
COCl2 (г) при определенных условиях равна 4. Равновесные концентрации веществ составляют, моль/л: [Cl2] = 0,5; [COCl2] = 2. Определить равновесную концентрацию CO.
14. При каких условиях в равновесной системе N2(г) + 3H2(г)  2NH3(г), DH0298 = – 92,4 кДж можно максимально увеличить выход NH3?
2NH3(г), DH0298 = – 92,4 кДж можно максимально увеличить выход NH3?
15. Исходные концентрации оксида азота (II) и хлора в гомогенной системе 2NO(г) + Cl2(г)  2NOCl (г) составляют соответственно 0,5 и 0,2 моль/л. Вычислить К с , если к моменту наступления равновесия прореагировало 20% оксида азота (II).
2NOCl (г) составляют соответственно 0,5 и 0,2 моль/л. Вычислить К с , если к моменту наступления равновесия прореагировало 20% оксида азота (II).
16. Две реакции протекали с такой скоростью, что за единицу времени в первой реакции образовалось 3 г сероводорода, а во второй 10 г йодоводорода. Какая из реакций протекала с большей средней скоростью? Ответ пояснить.
17. В сосуде объемом 2 л смешали газ А (4,5 моль) и газ В (3 моль). Газы А и В реагируют в соответствии с уравнением А + В = С. Через 20 с в системе образовалось 2 моль газа С. Определить среднюю скорость реакции. Сколько моль газов А и В осталось в системе?
18. Равновесие гомогеннойсистемы 4HCl(г) + O2(г)  2H2O (г) + 2Cl2(г) установилось при следующих концентрациях реагирующих веществ, моль/л: [H2O] = 0,14; [Сl2] = 0,14; [HCl] = 0,20; [O2] = 0,32. Вычислите исходные концентрации хлористого водорода и кислорода.
2H2O (г) + 2Cl2(г) установилось при следующих концентрациях реагирующих веществ, моль/л: [H2O] = 0,14; [Сl2] = 0,14; [HCl] = 0,20; [O2] = 0,32. Вычислите исходные концентрации хлористого водорода и кислорода.
19. Вычислите константу равновесия для системы CO(г) + H2O(г)  СO2(г) + H2 (г), если равновесные концентрации веществ, моль/л: [CO] = 0,004; [H2O] = 0,084; [CO2] = 0,016; [H2] = 0,016.
СO2(г) + H2 (г), если равновесные концентрации веществ, моль/л: [CO] = 0,004; [H2O] = 0,084; [CO2] = 0,016; [H2] = 0,016.
20. Константа равновесия гомогенной системы CO(г) + H2O(г)  СO2(г) + H2(г) при некоторой температуре равна 1. Вычислите равновесные концентрации реаги-рующих веществ, если исходные концентрации, моль/л: С CO = 0,10; С H2O= 0,40.
СO2(г) + H2(г) при некоторой температуре равна 1. Вычислите равновесные концентрации реаги-рующих веществ, если исходные концентрации, моль/л: С CO = 0,10; С H2O= 0,40.
ЛАБОРАТОРНАЯ РАБОТА

История развития хранилищ для нефти: Первые склады нефти появились в XVII веке. Они представляли собой землянные ямы-амбара глубиной 4…5 м...

Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим...

Автоматическое растормаживание колес: Тормозные устройства колес предназначены для уменьшения длины пробега и улучшения маневрирования ВС при...

История создания датчика движения: Первый прибор для обнаружения движения был изобретен немецким физиком Генрихом Герцем...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!