

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни...

Кормораздатчик мобильный электрифицированный: схема и процесс работы устройства...
Топ:
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов...
Оснащения врачебно-сестринской бригады.
Характеристика АТП и сварочно-жестяницкого участка: Транспорт в настоящее время является одной из важнейших отраслей народного...
Интересное:
Влияние предпринимательской среды на эффективное функционирование предприятия: Предпринимательская среда – это совокупность внешних и внутренних факторов, оказывающих влияние на функционирование фирмы...
Наиболее распространенные виды рака: Раковая опухоль — это самостоятельное новообразование, которое может возникнуть и от повышенного давления...
Что нужно делать при лейкемии: Прежде всего, необходимо выяснить, не страдаете ли вы каким-либо душевным недугом...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
Волгодонский инженерно-технический институт
ФАКУЛЬТЕТ ____________________
КАФЕДРА ____________________
СПЕЦИАЛЬНОСТЬ ____________________
ОТЧЁТ
По лабораторным работам по общей химии
Студента________________________________________________
(группа, курс) (фамилия, имя, отчество)
Принял преподаватель______________________________________
(фамилия, имя, отчество)
______________________________________
(дата) (подпись)
Волгодонск 2015 г.
ЛАБОРАТОРНАЯ РАБОТА №1
ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ЭКВИВАЛЕНТА (ЭКВИВАЛЕНТНОЙ МАССЫ) МЕТАЛЛА ПО ОБЪЁМУ ВЫТЕСНЕННОГО ВОДОРОДА
Ц е л ь р а б о т ы: Ознакомиться с методикой определения и расчёта молярной массы эквивалента металлов.
О б о р у д о в а н и е и м а т е р и а л ы: штатив, две бюретки на 50 см3, пробирка с газоотводной трубкой, термометр, барометр, аналитические весы и разновесы; навеска металла около 0,01 г; 2,5 М раствор НС1.
Методика выполнения работы
По объёму вытесненного водорода можно определить молярные массы эквивалентов активных металлов (магния, алюминия, цинка и т.д.), способных вытеснять водород из разбавленных кислот.
Прибор для определения молярной массы эквивалента металлов изображён на рис. 1.1. и состоит из:

|
1) двух бюреток на 50 см3, соединённых резиновой трубкой;
2) реакционной пробирки;
3) газоотводной трубки;
4) штатива.
Налить в пробирку 4-5 см3 2,5 М раствора хлористоводородной кислоты, 5 капель раствора Со(NO3)2 – катализатора. Навеску металла количественно перенести в пробирку c кислотой, которую плотно присоединить к прибору. Тотчас начинается выделение водорода и вода вытесняется из правой бюретки в левую. Пока идёт реакция, записать показания барометра и термометра; по табл. 1 определить давление насыщенных паров воды.Когда весь металл растворится, прекратится понижение уровня воды в бюретке. Окончательный точный отсчёт показаний бюретки производится после охлаждения пробирки до комнатной температуры (через 3-5мин.).
|
|
Результаты измерений записывают по форме:
Масса металла, m=..., г
Показания бюретки до проведения реакции V1=..., см3
Показания бюретки после реакции V2=..., см3
Объём выделившегося водорода VH2 =V2 – V1=..., см3
Температура окружающей среды t=..., ° С; Т=273 +t=..., К
Атмосферное давление Р=..., Па
Давление насыщенных паров воды  =..., Па
=..., Па
Парциальное давление водорода  =
=  -
- 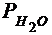 =..., Па
=..., Па
Объём выделившегося водорода приводят к нормальным условиям на основании уравнения состояния идеального газа, объединяющего законы Бойля-Мариотта и Гей-Люссака:

где P0 - нормальное давление, равное 101325 Па; Vo - объём газа при нормальных условиях, см3; То - 273 К;  - парциальное давление сухого водорода;
- парциальное давление сухого водорода;  - объём газа в условиях опыта; Т - температура опыта по абсолютной шкале температур.
- объём газа в условиях опыта; Т - температура опыта по абсолютной шкале температур.
Таким образом, объём водорода, приведённый к нормальным условиям, определяется по уравнению:
 ;
;
По закону эквивалентов в случае, когда одно из реагирующих веществ находится в твёрдом состоянии, а второе - в газообразном, молярная масса эквивалента металла определяется по формуле:

где m - масса металла; МЭоп - молярная масса эквивалента металла; Vo -объём газа, приведённый к нормальным условиям; Vэ - молярный объём эквивалента газа.Молярный объём эквивалента водорода, составляющий  объёма его моля, занимает при нормальных условиях 11200 см3/моль.
объёма его моля, занимает при нормальных условиях 11200 см3/моль.
Таблица 1.
Давление насыщенного водяного пара в равновесии с водой

Затем студенты вычисляют теоретическую величину молярной массы эквивалента металла и находят относительную ошибку определения:

В конце работы записываются выводы.
Общий вывод по работе:
| Работу выполнил Студент группы | Работу принял Преподаватель | Дата | ||
|
|
Контрольные вопросы.
1. Что называется молярной массой эквивалента элемента? В каких единицах измеряется молярная масса эквивалента?
2.. Сформулируйте закон эквивалентов. Выразите его математически.
3. Какие факторы оказывают влияние на точность определения молярной массы эквивалента металла при взаимодействии его с кислотой?
Лабораторная работа №2
Выполнение работы.
Лабораторная работа №3
Химическое равновесие
Цель работы: ознакомиться с понятием скорости химических реакций; факторами, влияющими на её величину, а также влиянием изменения внешних факторов на состояние химического равновесия.
Оборудование и материалы: растворы иодата калия, сульфата натрия, серной кислоты, тиосульфата натрия, хлорида железа (III), роданида калия, сульфата меди, крахмала, карбонат кальция (мрамор); штатив с пробирками (8шт.); секундомер; термометр; нагревательный прибор.
Выполнение работы
Лабораторная работа №4
Гидролиз солей
Цель работы: изучить условия протекания процесса гидролиза солей и влияние факторов,обусловливающих смещение ионного равновесия при гидролизе.
Оборудование и материалы:иономер, штатив с пробирками, растворы солей, кислот, щелочей, индикаторы, кристаллические соли, спиртовая горелка, пипетка.
Выполнение работы.
Опыт №1. Смещение ионного равновесия в растворах вследствие гидролиза
В разные пробирки внести небольшое количество следующих соединений: НСl; NaOH; NаСl;
Nа2СО3; ZnСl2; Pb(СН3СОО)2. Во все пробирки прилить одинаковое количество воды. Осторожным встряхиванием добиться полного растворения каждой соли. Полосками универсальной индикаторной бумажки измерить рН каждого раствора. Для сравнения такой бумажкой измерим рН дистиллированной воды. Данные опыта свести в таблицу
Составить сокращенные ионные уравнения гидролиза солей и объяснить изменение окраски индикаторной бумаги в растворах солей в сравнении с окраской ее в дистиллированной воде.
|
Общий вывод
| Работу выполнил Студент группы | Работу принял Преподаватель | Дата |
Лабораторная работа №5
Выполнение работы.
Методика выполнения
Опыт №1. Получение и свойства предельных углеводородов на примере метана.
Поместить в пробирку тщательно измельчённую смесь, состоящую из ацетата натрия и гидроксида натрия в массовом соотношении 1:2. Пробирку закрыть пробкой с отводной трубкой и нагреть. Происходит образование метана и карбоната натрия. Пропустив полученный метан через водные растворы KMnO4, сделать выводы относительно свойств предельных углеводородов. Написать уравнение реакции получения метана.
Опыт №2. Окисление спиртов.
В пробирку налить 2 см3 разбавленного раствора К2Сг2O7, 1 см3 2 М
H2 SO4 и 1 см этанола. Смесь осторожно нагреть. Как изменяется цвет раствора? Обратить внимание на характерный запах ацетальдегида (запах прелых яблок). Реакция протекает по уравнению:
ЗСН3СН2OН+К2Сг2О7+4Н2SO4=ЗСН3СНО+К2SO4+Сг2(SO4)3+7Н2O
Опыт №3. Реакция на альдегиды (реакция серебряного зеркала).
В чистую пробирку налить 2 см3 аммиачного раствора оксида серебра [Ag(NH3)2OH и прибавить 3-4 капли раствора формальдегида. Пробирку подогреть на кипящей водяной бане. При этом её стенки покрываются блестящим налётом металлического серебра.
Реакция идёт по уравнению:
HCHO+2[Ag(NH3)2]OH=HCOOH+2Ag  +H2O+4NH3
+H2O+4NH3
| Работу выполнил студент группы | Работу принял преподаватель | Дата |
Контрольные вопросы
1. Чем обусловлены значительные различия в свойствах предельных и непредельных углеводородов?
2. По какому признаку и на какие классы делятся органические соединения?
4. Какие функциональные группы и сколько должны содержать органические вещества, чтобы их можно было использовать для получения полимеров?
Волгодонский инженерно-технический институт
ФАКУЛЬТЕТ ____________________
КАФЕДРА ____________________
СПЕЦИАЛЬНОСТЬ ____________________
ОТЧЁТ
|
|
|

Особенности сооружения опор в сложных условиях: Сооружение ВЛ в районах с суровыми климатическими и тяжелыми геологическими условиями...

Двойное оплодотворение у цветковых растений: Оплодотворение - это процесс слияния мужской и женской половых клеток с образованием зиготы...

Таксономические единицы (категории) растений: Каждая система классификации состоит из определённых соподчиненных друг другу...

Типы сооружений для обработки осадков: Септиками называются сооружения, в которых одновременно происходят осветление сточной жидкости...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!