

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...

Семя – орган полового размножения и расселения растений: наружи у семян имеется плотный покров – кожура...

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого...
Топ:
Процедура выполнения команд. Рабочий цикл процессора: Функционирование процессора в основном состоит из повторяющихся рабочих циклов, каждый из которых соответствует...
Теоретическая значимость работы: Описание теоретической значимости (ценности) результатов исследования должно присутствовать во введении...
Интересное:
Аура как энергетическое поле: многослойную ауру человека можно представить себе подобным...
Лечение прогрессирующих форм рака: Одним из наиболее важных достижений экспериментальной химиотерапии опухолей, начатой в 60-х и реализованной в 70-х годах, является...
Средства для ингаляционного наркоза: Наркоз наступает в результате вдыхания (ингаляции) средств, которое осуществляют или с помощью маски...
Дисциплины:
|
из
5.00
|
Заказать работу |
|
|
|
|
При тяжелом алкалозе (pH > 7,55) с угрожающими жизни нарушениями, если введение хлорида натрия или калия по той или иной причине не осуществимо (например, перегрузка объемом, почечная недостаточность), показано внутривенное введение HCl. Соляная кислота также показана при необходимости быстро купировать метаболический алкалоз – при возникновении аритмий, печёночной энцефалопатии, кардиотоксического эффекта дигоксина.
Для определения необходимого количества HCl нужно рассчитать дефицит водорода в организме (в мэкв).
H+ДЕФИЦИТ = 0,5×mКГ×(HCO3-ИСТИННЫЙ – HCO3-ЖЕЛАЕМЫЙ)
где 0,5 – это объем распределения водорода, который больше, чем у хлоридов, так как некоторое количество H+ проникает внутрь клеток.
Традиционно используется раствор 0,1N HCl для внутривенных инфузий, который содержит 100 мэкв/л H+. Примерно такое количество водорода содержит желудочный сок. Объем 0,1 N HCl, необходимый для коррекции дефицита H+, устанавливается путем деления рассчитанного дефицита H+ на его концентрацию в растворе.
V = H+ДЕФИЦИТ/100.
Желаемый уровень HCO3- должен быть немного выше нормального, так как конечная цель инфузии HCl это не коррекция метаболического алкалоза, а уменьшение его тяжести.
Вследствие выраженного коррозийного действия HCl необходимо вводить только в центральные вены. Внесосудистое введение соляной кислоты вызывает тяжелый некроз тканей, а в концентрации выше 0,1 N разъедается внутрисосудистый катетер. Поэтому скорость введения HCl не должна превышать 0,2 мэкв/кг/час или 15-20 мэкв/час.
Для лечения алкалоза может применяться хлорид аммония внутрь. В печени аммиак превращается в мочевину, высвобождая HCl, который немедленно реагирует с буферами и сдвигает концентрацию H+ в сторону ацидоза. Хлорид аммония можно применять и внутривенно, что довольно опасно, так как NH4+ является высокотоксичным соединением и противопоказан при печеночной энецафалопатии. Вместо хлорида аммония также можно применять лизина моногидрохлорид.
|
|
Пример.
Анализ КЩС, проведенный больному весом 80 кг выявил наличие метаболического ацидоза, уровень pH составил 7,55, количество HCO3- - 40 мэкв/л.
Если желаемый уровень HCO3- равен 35 мэкв/л, то дефицит H+ = 0,5 × 70 × (40 – 35) = 175 мэкв.
Объем 0,1 N HCl составит 175/100 = 1,75 литра, а максимальна скорость введения 0,2 × 70 = 14 мэкв/час, то есть 140 мл 0,1 N HCl в час или 2,3 мл/мин.
Прочие варианты лечения.
Как вариант коррекции метаболического алкалоза применяется гемодиализ и перитонеальный диализ. Диализ применяется в случаях острой почечной недостаточности, сопровождающейся объёмной перегрузкой и резистентностью к ацетазоламиду. При метаболическом алкалозе применяется диализат со сниженным количеством бикарбоната (менее 18 ммоль/л). Можно также использовать диализат, не содержащий бикарбонат или ацетат (buffer-free dialysate), тогда во время диализа или после него бикарбонат добавляется по необходимости.
Перитонеальный диализ при лечении метаболического алкалоза проводится изотоническими растворами хлорида натрия.
Правила взятия пробы
Капиллярная кровь
Перед забором пробы крови для анализа КЩС необходимо четко представить себе цель исследования. Если планируется оценить функцию лёгких, а точнее легочной газообмен, требуется брать пробу артериальной крови. PaO2, PaCO2 в артериальной крови будут отражать реальный газообмен в легких при условии отсутствия внутрисердечного шунта. Если необходимо оценить степень ацидемии при повышенном поступлении или образовании кислот, зачастую достаточно пробы смешанной венозной крови.
Капиллярная кровь по газовому составу не имеет четкого отношения ни к артериальной, ни к венозной крови. В зависимости от состояния гемодинамики газовый состав капиллярной крови будет варьировать.
|
|
Информативность капиллярной крови для больного в состоянии гемодинамической нестабильности очень низкая. В случае нестабильной гемодинамики или охлаждения пациента развивается периферический вазоспазм и артериовенозное шунтирование, в результате чего время прохождения крови через конечные капилляры удлиняется, растет степень экстракции кислорода, увеличивается образование CO2, включается анаэробный гликолиз. Гиперкапния, гипоксемия и умеренный метаболический ацидоз в таком случае говорят о нарушении периферической микроциркуляции в данном участке тела и ни в коем случае не отражают системный газообмен.
Для выявления расстройств периферической микроциркуляции при выполнении капиллярной пробы крови определяется симптом «бледного пятна» (capillary refill time): производится давление на ноготь до изгнания крови из капилляров – появления бледного окрашивания. Затем давление прекращается и оценивается скорость наполнения капилляров. В норме естественный цвет должен вернуться не позже, чем через 2 секунды. Удлинение скорости наполнения более 2 секунд указывает на нарушение периферической микроциркуляции.
Для адекватного анализа капиллярной крови иногда достаточно согреть конечность, где планируется произвести пробу. Так, капиллярная кровь, взятая у больного без нарушений гемодинамики и вентиляции, но с холодными руками, практически полностью соответствует нормам венозной крови, при согревании руки в последующем результат анализа максимально приближается к нормальным показателям артериальной крови, что обусловлено повышением кровенаполнения конечности и увеличением скорости тканевого кровотока. Можно смоделировать соответствующую клиническую ситуацию, создав гиперкинетический тип кровообращения, приблизив тем самым состав капиллярной крови к артериальной, либо снизить системное артериальное давление до критических величин, замедлив в итоге тканевую перфузию. В последнем случае проба капиллярной (тканевой) крови будет сходна с венозной кровью. Однако такие опыты будут выглядеть весьма негуманно по отношению к больному, да и не каждый больной в силах без последствий перенести столь выраженные сдвиги в гемодинамике. В целом такие методы позволяют весьма относительно оценивать КЩС и газовый состав крови, так как в любом случае, результат анализа капиллярной крови не будет соответствовать каким-либо общепринятым нормам. Даже если максимально приблизить качество капиллярной крови к венозной, результат не будет отражать истинное положение гомеостаза, так как ситуация, вызвавшая такой сдвиг в тканевой перфузии, уже является дополнительным патологическим агентом и не отражает реальную ситуацию при не нарушенной перфузии. Практическую пользу можно извлечь при повторном заборе крови у одного и того же больного при стабильной гемодинамике и одинаковых условиях технического исполнения. В таком случае можно оценить состояние данного пациента в динамике.
|
|
Как правило, капиллярную кровь чаще используют в педиатрической практике – для анализа КЩС и газового состава у новорождённых.
Артериальная кровь.
При прохождении через лёгкие венозная кровь отдает наработанный углекислый газ и присоединяет кислород. Углекислый газ является четким критерием способности лёгких к элиминации, а уровень кислорода в артериальной крови – критерием диффузионной способности легких и состояния вентиляционно-перфузионных отношений. Являясь биологическим фильтром, лёгкие нейтрализуют многие продукты метаболизма, что отражается в кислотно-щелочном состоянии артериальной крови.
Поэтому артериальная кровь является наиболее подходящей для анализа КЩС и газового состава.
Венозная кровь.
Венозная кровь содержит повышенное количество СО2, выделяемого тканями при метаболизме и уменьшенное количество О2, отражающее утилизацию кислорода.
Диагностическая ценность пробы венозной крови заключается в оценке системного метаболизма. Уменьшение PvO2 свидетельствует об увеличении экстракции кислорода тканями, увеличение – о шунтировании артериальной крови мимо периферических сосудов.
При взятии крови из периферических вен будет отражаться метаболизм отдельных участков тела. Такие исследования не представляют особой ценности, так как кому и зачем нужно знать, например, метаболизм правой руки? Однако при отсутствии других альтернатив, при стабильной гемодинамике и отсутствии расстройств периферической микроциркуляции, допускается забор периферической венозной крови. Для цельного представления о тканевом метаболизме необходимо производить забор смешанной венозной крови из легочной артерии. При взятии пробы из правых отделов сердца результат может быть не совсем точным, так как полного смешивания двух потоков крови (из верхней и нижней полых вен) может не произойти. Разумеется, в большинстве клиник страны катетеризировать легочную артерию не предоставляется возможным, поэтому следует ограничиться забором крови из правого предсердия или из верхней полой вены через центральный катетер.
|
|
Практическую пользу несет сравнение газов артериальной и венозной крови, позволяющее рассчитать артериовенозную разницу по кислороду. Зная количество доставленного O2 и количество O2 в венозной крови, можно вычислить потребление кислорода. Естественно, без показателей системной гемодинамики (сердечный выброс и сердечный индекс) придется довольствоваться всего лишь коэффициентом экстракции кислорода.
Виды артериального доступа.
Наиболее часто для взятия проб артериальной крови используются бедренная и лучевая артерии. При необходимости можно пунктировать плечевую артерию и артерию тыла стопы.
Пункция лучевой артерии.
Преимущества: простота доступа, низкий риск развития гематомы (0,58%).
Недостатки: при плохо развитом коллатеральном кровотоке тромбоз лучевой артерии может привести к ишемическому некрозу пальцев, также возможны механические повреждения нервов иглой или из-за сдавления гематомой, спазм артерии, клинически значимый у лиц с болезнью Рейно.
Противопоказания: выраженный локальный атеросклероз, отрицательная проба Аллена.
Техника пункции:
· проверка эффективности коллатерального кровотока – проба Аллена. Лучевая и локтевая артерии анастомозируют через поверхностную и глубокую ладонные дуги, при недостаточно развитом коллатеральном кровотоке в бассейне локтевой артерии тромбоз или спазм лучевой артерии может привести к некрозу пальцев кисти.
Для проведения пробы Аллена больного просят несколько раз сжать и разжать кулак до побледнения кисти, оставляя кулак сжатым, затем пережимается локтевая и лучевая артерии (рис. 28). Кисть разжимается, после чего давление на локтевую артерию прекращается. Естественный цвет кожи должен вернуться не позже, чем через 5 секунд.
Наиболее удалённым от локтевой артерии является большой палец, на качество кровообращения в котором необходимо ориентироваться в первую очередь. Если восстановление первоначального цвета занимает от 5 до 10 секунд, это трактуется как нарушение кровотока по локтевой артерии.
|
|

Рис. 28. Проба Аллена. Чен Г., Сола Х. Е., Лиллемо К. Д. Руководство по технике врачебных манипуляций.
Если же время кровенаполнения составляет более 10 секунд, от пункции лучевой артерии лучше отказаться. Конечно, проба Аллена является не слишком достоверным способом определения адекватности коллатерального кровообращения и применяется в основном перед катетеризацией артерии. Как показала практика, при частой пункции лучевой артерии, особенно у больных в стрессовом состоянии с гиперкоагуляционными расстройствами, нередко возникают нарушения кровотока в кисти, проявляющиеся в виде отечности и побледнения пальцев. Пациенты, получающие вазопрессоры, также повергаются повышенному риску ишемии при многократной пункции лучевой артерии. На наш взгляд, проба Аллена должна проводиться перед любыми манипуляциями на лучевой артерии, так как приблизительно у 3 - 5% людей arcus palmaris superficialis и arcus palmaris profundus оказываются незамкнутыми.
У больных в бессознательном состоянии выполнить классическую пробу Аллена не предоставляется возможным. У таких больных проба проводится без предварительного сжатия кисти, для чего достаточно пережать артерии на поднятой руке.
Визуальная оценка является вариабельным критерием, поэтому автор предлагает проводить модифицированную пробу Аллена с использованием пульсоксиметрии.
На большой палец исследуемой руки крепится датчик пульсоксиметра, далее пережимаются локтевая и лучевая артерии до исчезновения пульсовой волны на мониторе. После прекращения давления на локтевую артерию пульсовая волна должна появиться не позже, чем через 3 секунды. Ориентирование на SpO2 не является точным в связи с определённой задержкой между изменением насыщения артериальной крови кислородом и отображением этого изменения на мониторе. Можно уменьшить время расчета SpO2, однако это увеличит погрешность измерения.
· обработка места пункции антисептиком;
· пальпируется пульс на лучевой артерии у дистального конца лучевой кости. Для облегчения пальпации кисть слегка переразгибают, слишком сильное разгибание кисти может затруднить пальпацию. Местную инфильтрационную анестезию не проводят, так как раствор анестетика может сместить артерию и затруднить её пальпацию;
· иглой 22 калибра, используя 2-миллилитровый шприц, промытый гепарином, пунктируется артерия под углом 30 - 45º к поверхности кожи по направлению к пульсации (рис. 29);
· присутствующий в шприце воздух немедленно удаляется, игла закрывается колпачком или вводится в специальную резиновую заглушку или пробку;
· шприц с полученным образцом несколько раз перекатывается между ладонями для смешивания гепарина и крови;

Рис. 29. Пункция лучевой артерии.
· после удаления шприца место пункции плотно прижимают в течение 5 минут или более, в зависимости от кровоточивости;
· необходимо зафиксировать время взятия пробы, температуру тела и позицию пациента, FiO2 и параметры ИВЛ.
Пункция бедренной артерии.
Преимущества: простота доступа.
Недостатки: высокий риск кровотечений, тромбоза, окклюзии артерии из-за наличия атеросклеротических бляшек, ишемии конечности, инфекционных осложнений.
Противопоказания: наличие подвздошного или бедренного сосудистого трансплантата (протеза), локальное заболевание сосудов (аневризма, атеросклероз, тромбоз), применение тромболитиков или высоких доз антикоагулянтов.
Техника пункции:
· область пункции обрабатывается антисептиком;
· определяются анатомические ориентиры: лобковый симфиз и передняя верхняя ость подвздошной кости. Бедренная артерия определяется по пульсации в средней точке по линии, соединяющей лобковый симфиз и переднюю верхнюю ость подвздошной кости (см. рис. 27);
· определяется пульсация на 1-2 см. дистальнее начальной точки;
· иглой 22 калибра, используя 2-миллилитровый шприц, промытый гепарином, пунктируется артерия под углом 45º к поверхности кожи по направлению к пульсации. При использовании игл большего диаметра необходимость создавать разрежение в шприце отсутствует, так как шприц наполняется самотеком под действием кровяного давления в артерии. При использовании игл небольшого калибра допускается поддержание небольшого разрежения в шприце.
Особенности:
· если пункция артерии не удалась, делается попытка на 1 см проксимальнее предыдущей точки;
· при возникновении гематомы или кровотечения необходимо прижать рукой место пункции на 15-20 минут.
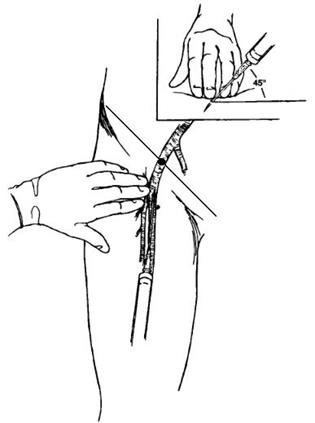
Рис. 27. Пункция бедренной артерии. Чен Г., Сола Х. Е., Лиллемо К. Д. Руководство по технике врачебных манипуляций.
Некоторые особенности.
Воздух.
Крайне важно содержать пробу крови в анаэробных условиях. PO2 в воздухе приблизительно равно 150 мм рт. ст., в то время как PaO2 составляет 80 -110 мм рт. ст. Если в шприце с пробой содержится пузырек воздуха, будет происходить диффузия кислорода из пузырька в кровь, что приведет к увеличению PaO2. При дыхании обогащенной кислородом смеси PaO2 может быть выше, чем PO2 воздуха, достигая 620 мм рт. ст. при дыхании 100 кислородом. В таком случае при наличии пузырька воздуха PaO2 будет снижаться. С углекислым газом наблюдается обратная картина – PCO2 в воздухе приближается к нулю, а PaCO2 артериальной крови равно 35 – 45 мм рт. ст. При большом объеме пузырька воздуха PaCO2 падает, однако, снижение PaCO2 более заметно в случаях, когда оно изначально очень высоко.
Для предотвращения диффузионных изменений шприц сразу же после пункции закрывают колпачком или надевают на иглу специальную резиновую заглушку или пробку. Такие мероприятия, однако, не исключают диффузию кислорода через стенки пластмассового шприца. Чем больше площадь поверхности шприца и выше напряжение кислорода в крови, тем больше диффузия кислорода в атмосферу. Наименьшая диффузионная утечка кислорода наблюдается при использовании миллилитровых или стеклянных шприцов.
Время.
От быстроты выполнения анализа зависит его точность. При длительном «простое» пробы наблюдается рост PaCO2, что приводит к снижению pH, а также падение PaO2. Напряжение кислорода в крови падает вследствие активного поглощения клетками крови, преимущественно лейкоцитами, тромбоцитами и ретикулоцитами. Чем больше выражен лейкоцитоз или тромбоцитоз, тем быстрее поглощается кислород, приводя к развитию псевдогипоксемии. Это имеет практическое значение при количестве лейкоцитов более 40×109 или тромбоцитов не менее 1000×109. Эритроциты здесь не играют существенной роли, так как при увеличении гематокрита снижается объем свободной плазмы и точность анализа падает. Метаболическая активность лейкоцитов приводит также к увеличению PaCO2 – псевдоацидозу. Когда кислород заканчивается, включается анаэробный гликолиз, что вызывает накопление лактата в пробе крови. Вследствие продолжающегося метаболизма уровень глюкозы в крови падает. Смешанный ацидоз (гиперкапнический и лактат-ацидоз) уменьшает количество анионных сайтов на молекулах альбумина, что повышает уровень свободного кальция. Если выполнить анализ в течение 1 минуты невозможно, необходимо охладить пробу, поместив её в лед или замедлить метаболизм в клетках крови, добавив цианидов для разобщения окислительных процессов. Даже хранящаяся на льду проба меняется со временем – в течение часа PaCO2 повышается на 3 – 10 мм рт. ст., вызывая небольшое снижение pH. Напряжение кислорода в охлаждённой пробе обычно стабильно в течение 1 часа.
Гепарин.
Жидкий гепарин является слабой кислотой, поэтому чрезмерное количество гепарина в шприце для взятия пробы приводит к ацидозу вследствие разведения бикарбоната и его нейтрализации, хотя гепарин буферизируется преимущественно гемоглобином. Разведение крови также приводит к занижению значений глюкозы, лактата, некоторых электролитов. Гепарин является натриевой солью и может искусственно завышать истинную концентрацию натрия в крови. Кальций и калий связываются с негативно заряженным гепарином, что приводит к ложному занижению их количества. Газовый состав раствора гепарина приближается к таковому у атмосферного воздуха – PO2 около 150 мм рт. ст., а PCO2 менее чем 0,3 мм рт. ст., что сказывается на газовом составе крови в полученном образце. Степень изменений пробы зависит от количества гепарина и концентрации гемоглобина (гематокрита). Клинически значимые изменения состава пробы проявляются при большом количестве гепарина и в целом значение их невелико. При количестве гепарина 0,1 мл на 1-2 мл крови ошибка составляет не более 5%. Если использовать меньшее количество гепарина, возрастает риск образования сгустков в шприце. Использование обработанных сухим гепарином шприцов позволяет избежать дилюционных ошибок, однако увеличивает риск образования кровяных сгустков.
Клетки крови.
У больных лейкозом проба крови достаточно быстро теряет свою информативность, по причине развивающейся гипоксии, гиперкапнии, гипогликемии, гиперкапнического и лактат-ацидоза (см. выше).
Лактат.
Для точного определения лактата измерение должно быть выполнено в максимально короткое время – до 5 минут с помещением пробы в лед. При задержке достоверность пробы уменьшается. Лактат-ацидоз, связанный с периферической гипоперфузией и гипоксией можно диагностировать и при помощи пробы смешанной венозной крови. Если у больного присутствует эндотоксин-обусловленное острое повреждение легких, тогда необходимо получить образец артериальной крови (см. «лактат-ацидоз»).
Положение тела пациента.
При положении на спине PaO2 обычно несколько ниже, чем сидя.
Температура.
Измерение температуры тела пациента существенно не влияет на оценку газового состава крови и КЩС. Существующие нормы показателей КЩС и ABG рассчитаны при стандартной температуре 37ºС. На данный момент неизвестны «нормальные» параметры КЩС при повышенной или пониженной температуре тела.
Однако следует ожидать определённых изменений при нагревании или охлаждении пробы крови. При нагревании крови происходит смещение кривой диссоциации гемоглобина вправо и уменьшение растворимости газов в плазме. В результате PaO2 и PaCO2 увеличиваются, а pH снижается. При нагревании крови на каждый градус выше 37ºС PaO2 увеличивается на 7,2% от исходного, а PaCO2 – на 4,4%. При охлаждении - наоборот, кривая диссоциации оксигемоглобина смещается влево, а растворимость газов в крови увеличивается, что приводит к снижению PaO2 и PaCO2 и к увеличению pH. Охлаждение крови на каждый градус ниже 37ºС приводит к снижению PaO2 на 7,2%. Большинство аппаратов для измерения КЩС и ABG автоматически производят коррекцию на настоящую температуру тела пациента. Коррекция на температуру тела пациента имеет практическое значение при t > 39ºC.
Таблица 16. Температурная коррекция pH крови, PaCO2 и PaO2 (Дж. Марини, 2002)
| Температура тела, ºС. | pH | PaCO2 | PaO2 |
| 41,5 40,5 39,5 38,5 35,5 34,5 33,5 | -0,09 -0,07 -0,06 -0,05 -0,04 -0,04 -0,03 -0,02 -0,01 Нет 0,01 0,02 0,03 0,04 0,04 0,05 0,06 0,07 0,09 0,10 6,12 0,13 0,15 0,19 | +22 +17 +16 +14 +12 +10 +8 +6, +4 Нет -4 -6 -8 -10 -12 -14 -16 -19 -22 -26 -29 -32 -36 -43 | +35 +27 +25 +22 +19 +16 +13 +10 +7 Нет -7 -10 -13 -16 -19 -22 -25 -30 -35 -39 -43 -47 -53 -60 |
Технические погрешности.
Возможно смешивание артериальной крови и венозной, которое приводит к несоответствии результатов (получении гипоксемии и гиперкапнии без существенных изменений pH) и неправильной их трактовке.
Длительные попытки пункции артерии вызывают стрессорный ответ пациента на болевые импульсы, приводя к гипервентиляции. Возможна и обусловленная болью задержка дыхания, которая вызывает гипоксемию и гиперкапнию.
При активном заборе крови через иглу малого диаметра, интенсивном охлаждении и замерзании части крови может развиваться гемолиз. Гемолиз влияет на концентрацию калия и ионизированного кальция, дополнительно определяемых некоторыми типами аппаратов.
Для точного измерения ABG необходимо, чтобы состояние пациента было стабильно определённое время до пункции артерии. После поворотов больного, применения прон-позиции, изменения режимов ИВЛ, проведения болюсной инфузионной терапии пробы не следует брать в течение 15 – 20 минут.
При изменении концентрации кислорода во вдыхаемой смеси необходимо выждать не менее 10 минут, чтобы обеспечить стабильное PaO2.
Когда врач не может принести пользы, пусть он не вредит.
Гиппократ
Послесловие
Существует три типа подхода к медицине – доказательный, рациональный, и традиционный. Доказательный медицина в настоящее время пользуется популярностью среди молодых врачей, когда особенно модно становиться публично заявить результаты эффективности лечения при определённых заболеваниях перед менее продвинутыми коллегами, особенно если они расходятся с общепринятыми (скорее, общеожидаемыми) результатами. Например, эффективность панацеи №1 глюкокортикоидных гормонов или ингибиторов протеаз либо неотъемлемого спутника терапии панкреатитов сандостатина уже давно не воспринимается цивилизованным миром всерьёз согласно всё той же доказательной медицине. Вообще, доказательная медицина в отечественной медицине является своеобразным аппендиксом: все знают, что она где-то есть, но мало кто знает, зачем она, собственно, нужна. Особенно уникальные врачи заявляют про доказательную медицину: «а я ей не верю». Видимо, легче поверить своему личному «слепому» неконтро-лируемому «нерандомизированному» опыту в течение многих лет работы, когда основным аргументом эффективности метода является фраза «мы так всегда делаем», чем результату контролируемой, тщательно спланированной, хорошо отлаженной работы огромной группы специалистов.
Рациональная медицина – это медицина, когда не нужно ничего доказывать, когда и так всё вроде бы понятно. Например, назначение антибактериальной терапии при пневмонии или хирургической инфекции, ингибиторов АПФ при артериальной гипертензии. Однако и здесь при большом желании можно напартачить – превратить рациональную медицину в иррациональную. Например, назначение деэскалационой антибиотикотерапии (цефалоспоринов III поколения) с целью профилактики, видимо, гипостатической пневмонии у лежачих больных без признаков какой-либо инфекции или нейтропении повергнет в шок грамотного инфекциониста да и вообще любого врача, близко знакомого с принципами антибактериальной фармакотерапии. Сюда же так же относится и назначение ингибиторов АПФ больным артериальной гипертензией со стенозом почечных артерий.
Основным «злом» все же является традиционная медицина – это подход к лечению больного, обоснованный сугубо обычаями и традициями лечебного учреждения. И порой становится невозможным выяснить изначальный источник, прародитель догм, мифов и страшных сказок традиционной медицины, ибо эти принципы к моменту их выявления настолько въедаются в головы использующих их людей, что появляется слепая, подчас фанатичная вера в справедливость выбранного подхода. И если доказательную медицину можно доказать, рациональную оспорить (например, дозировка и кратность введения антибактериального препарата), то традиционную медицину изменить нельзя. Видимо, единственный выход из такой ситуации – оградить подрастающее поколение врачей от бредящих традиционной медициной старших коллег, всучить им в руки медицинские журналы и книги и заставить самостоятельно изучить интересующую проблему. К сожалению, по многим причинам сделать это невозможно, поэтому и в данный момент, и через год, и на сто лет в перспективе доказательный подход к медицине будет стоять в стороне от традиционного «дедовского» подхода местных «авторитетных» лиц, передающих свои традиции из поколения в поколение. В такой ситуации хочется пожелать всем коллегам сохранять в первую очередь интеллектуальную честность – готовность тщательно проверять правильность своих убеждений и в то же время иметь достаточно времени для выслушивания других имеющихся доказательств.
Должны быть в поиске подходящие альтернативы для реализации клинической модели, основанные не только на субъективном взгляде лечащего врача, обусловленном неким новомодным веянием, но и на реальной оценке состояния больного. «Запротоколированное» лечение не оставляет места для клинического мышления, сводя на нет все достижения доказательной медицины своим крайне редким обновлением, отстающим от современности порой на десятилетия.
Зачастую анализ КЩС и газового состава крови нужен врачам только для констатации самого факта наличия метаболических расстройств. «Ну ацидоз, ну алкалоз» - разводят руками многие клиницисты. Лечение таких нарушений часто проходит по принципу ацидоз-бикарбонат, алкалоз-соляная кислота. Необходимо заставить себя думать, что же стало причиной развития такого состояния и лечить патологию, а не следствие нарушения метаболизма. Когда отклонение КЩС является причиной, а не следствием нарушения витальных функций, только тогда, без сомнения, возможно применение «биохимических антидотов» - бикарбоната и соляной кислоты. Для того чтобы выяснить, что есть следствие, а что есть причина, и нужен весь арсенал знаний врача, пополнить и (или) если нужно, исправить которого, - основная цель данного руководства.
К традиционной медицине относится и применение бикарбоната при любом виде ацидоза, ориентируясь только на pH крови. Автор не является ярым противником щелочной терапии, но категорически против полипрагмазии, тем более, если в неё входит далеко не безобидный бикарбонат.
Не случайно послесловие заканчивается картинкой с символическим названием «Иван Грозный чуть не убил своего сына», чтобы каждый врач на секунду представил себя на месте царя, а вместо сына – пациента, которому был столь не опрометчиво введен бикарбонат натрия. Пусть выздоровление пациента будет заслугой именно лечащего врача, а не огромного резерва жизненных сил пациента, подорвать которых не в силах даже массивная щелочная терапия.

SUGGESTED READINGS
1. Marino, Paul L. ICU Book, The, 3rd Edition Lippincott Williams & Wilkins ©2007
2. Michael W. King, Ph.D. Hemoglobin and Myoglobin. Medical Biochemistry Terre Haute Center for Medical Education. 1997
3. Michael G. Levitzky, Ph.D Pulmonary Physiology 7th Edition by The McGraw-Hill Companies, Inc., 2007
4. West J. B. Respiratory physiology: the essentials, 8th edition Lippincott Williams & Wilkins ©2008
5. Brian K Genlbach, Gregory A Schmidt Treating acid-base abnormalities in the intensive care unit – the role of buffers BioMed Central Ltd, Critical Care 2004
6. Donall O’Croinin, Martina Ni Chonghaile, Brendan Higgins, John G Laffey Permissive hypercapnia Critical Care 2004, BioMed Central Ltd
7. Howard E Corey Fundamental principles of acid-base physiology Critical Care 2004, BioMed Central Ltd
8. Brandis Kerry Acid-base pHysiology www.qldanaesthesia.com, www.anaesthesiaMCQ.com
9. Arthur C. Guyton, M.D., John E. Hall, Ph.D. Textbook of Medical Physiology 11th ed. 2006, Elsevier Inc. Philadelphia
10. Pinsky Michael R., MD, Brochard L., MD, Mancebo J., MD Applied Physiology in Intensive Care Medicine, Springer-Verlag Berlin Heidelberg 2006
11. Irwin, Richard S.; Rippe, James M. Irwin and Rippe's Intensive Care Medicine, 6th Edition, Lippincott Williams & Wilkins Copyright В© 2008
12. Brenner Matthew, MD Critical Care Medcine, 2007 Michael Krutzik, M.D, Guy Foster, MD Endocrinologic and Nephrologic Disorders
13. Albert Clark, Jason O’Neale Roach CRASH COURSE: metabolism and nutrition Elsevier Inc. Copyright © 2007
14. Koolman J., Roehm K. H. Color Atlas of Biochemistry 2nd edition Thieme Stuttgart-New York 2005
15. Phillips Lynn D. IV therapy notes F. A. Davis Company, Philadelphia, 2005
16. Michael J. Apostolakos, M.D. Peter J. Papadakos, M.D. Intensive Care Manual McGRAW-HILL, Medical publishing division, 2001
17. Mary J. Mycek, Ph.D., Richard A. Harvey, Pamela C. Champe Lippincott’s illustrated reviews: pharmacology Lippincott Williams & Wilkins Copyright В© 2000
18. Hopkins B. Tracey, BSN, RN Lab Notes: Guide to Lab and Diagnostic Tests F. A. Davis Company, Philadelphia, 2005
19. Lewis J Kaplan and Spiros Frangos. Clinical review: Acid–base abnormalities in the intensive care unit – part II, New Haven, Connecticut, 2004 BioMed Central Ltd
20. Mazzagatti F.A, Lebovits L.C., Schluger N.W Respiratory care pearls, Hanley & Belfus, Philadelphia (пер. Бином, Санкт-Петербург), 2002 p.221-235
21. Margretta R Seashore The Organic Acidemias: An Overview, GeneReview – Last Revision 2006
22. Charles P Venditti, MD, PhD Methylmalonic Acidemia Genetic Disease Research, National Human Genome Research Institute, National Institutes of Health, 2005.
23. Kevin A Strauss, MD, Erik G Puffenberger, PhD, Holmes Morton, MD Maple Syrup Urine Disease (MSUD) Clinic for Special Children, University of Washington, Seattle Jan 30, 2006.
24. Milford Fulop, MD; Meggan Mackay, MD Renal Tubular Acidosis, Sjögren Syndrome, and Bone Disease Arch Intern Med. 2004.
25. Mahendra Agraharkar, MD, MBBS, FACP, Mark Fahlen, MD, Kanwarpreet Baweja, MD Hyperchloremic Acidosis www.eMedicine.com, Jul 25, 2006
26. Michele Azer, MD, Heatherlee Bailey, MD Toxicity, Salicylate www.eMedicine.com, Nov 8, 2007
27. Kreplick Lance W, MD, MMM, FAAEM, FACEP, Toxycity, Salicylate, www.eMedicine.com, Jul 11, 2008
28. Ann G Egland, MD, Douglas R Landry, MD Toxicity, Alcohols www.eMedicine.com, January 4, 2007
29. Christie P Thomas, MB, BS, Khaled Hamawi, MD Metabolic Acidosis www.eMedicine.com, Feb 1, 2007
30. Karen L Stavile, MD Metabolic Acidosis www.eMedicine.com September 22, 2005
31. Hipp Antonia, DO, Metabolic Acidosis, www.eMedicine.com, Sept 11, 2008
32. Andrade V. B., Flávio O. Ihara, Eduardo J. Troster Metabolic acidosis in childhood: why, when and how to treat J. Pediatr. (Rio J.) vol.83 no.2 suppl.0 Porto Alegre May 2007
33. Alper Brent A. Jr, MD, MPH, Uremia, www.eMedicine.com, Jun 6, 2008
34. Sameer Yaseen, MD, Christie Thomas, MD, FACP, FAHA, FASN Metabolic Alkalosis www.eMedicine.com, May 3, 2007
35. Huang H Lennox, MD, Alkalosis, Metabolic www.eMedicine.com, Aug 13, 2008
36. Frassetto Lynda A., MD, Bartter Syndrome, www.eMedicine.com, May 16, 2008
37. Devarajan Prasad, MD, Bartter Syndrome, www.eMedicine.com, Oct 1, 2008
38. Scofield R Hal, MD, Milk-alkali Syndrome, www.eMedicine.com, Jun 13, 2007
39. Gordon Michelle V, Hamblin P Shane, McMahon Lawrence P Life-threatening milk-alkali syndrome resulting from antacid ingestion during pregnancy eMJA 182 (7): 350-351, 2005
40. Ammonium chloride, reffered articles, University of Maryland Medical Center (UMMC) © 2008
41. Daniel C Keyes, MD, MPH Toxicity, Ethylene Glycol www.eMedicine.com, Dec 11, 2007
42. Osama Hamdy, MD, PhD Diabetic Ketoacidosis www.eMedicine.com, Sep 20, 2007
43. Donald W Rucker, MD, MBA, MS, Diabetic Ketoacidosis www.eMedicine.com Feb 12, 2008
44. David E. Trachtenbarg, MD, Diabetic Ketoacidosis, American Academy of Family Physicians Vol. 71/No. 9 May 1, 2005
45. George Ansstas, MD Irina Robinson, MD, Sofya M Rubinchik, MD, David S Schade, MD Alcoholic Ketoacidosis www.eMedicine.com, Jun 5, 2008
46. Mary Claire O'Brien, MD, Alcoholic Ketoacidosis www.eMedicine.com Jul 2, 2007
47. Bret A Nicks, MD, Lactic Acidosis www.eMedicine.com Apr 9, 2008
48. Sat Sharma, MD, FRCPC, FACP, FCCP, DABSM Lactic Acidosis Mar 27, www.eMedicine.com, 2007
49. Jackie A Hayes, MD, FCCP Respiratory Acidosis Jul 7, www.eMedicine.com, 2005
50. Jackie A Hayes, MD, FCCP Respiratory Alkalosis www.eMedicine.com, Jun 30, 2005
51. Goodman & Gilman’s the Pharmacological basis of Therapeutics - 11th Ed., McGraw-Hill, 2006
52. Capan L., Nahas G.G., Manne J. et etc. Guidelines for the Treatment of Acidaemia with THAM Drugs, Volume 55, Number 2, February, pp. 191-224(34), 1998
53. Jose A. Diaz-Buxo Bicarbonate solutions: update Advanced in peritoneal dyalisis, Vol. 21, 2005
54. Jens C. Rekling, Jack L. Feldman preBötzinger complex and pacemaker neurons: hypothesized site and kernel for respiratory rhythm generation, Los Angeles, California Annu. Rev. Physiol. 60:385–405, 1998
55. CW Oettinger and JC OliverNormalization of uremic acidosis in hemodialysis patients with a high bicarbonate dialysate, Journal of the American Society of the Nephrology, Vol. 3, 1804-1807, 1993
Merk Manual Professional Renal Tubular Acidosis (RTA): abnormal renal transport syndromes, the Merk Manual Medical Library, Nov, 2005
|
|
|

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни...

Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим...

Архитектура электронного правительства: Единая архитектура – это методологический подход при создании системы управления государства, который строится...

Индивидуальные и групповые автопоилки: для животных. Схемы и конструкции...
© cyberpedia.su 2017-2024 - Не является автором материалов. Исключительное право сохранено за автором текста.
Если вы не хотите, чтобы данный материал был у нас на сайте, перейдите по ссылке: Нарушение авторских прав. Мы поможем в написании вашей работы!