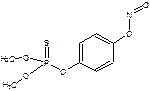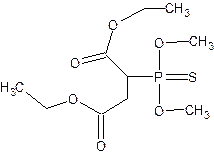В наружную камеру прибора для микродиффузии вносят 1 мл крови или мочи либо 1г гомогената ткани и 1 мл насыщенного раствора карбоната калия. Во внутреннюю камеру вносят 3 мл 10% -го раствора серной кислоты. Сосуд плотно закрывают крышкой и оставляют на 3 часа при комнатной температуре. При исследовании гомогената ткани время микродиффузии увеличивается до пяти часов.
К 1 мл раствора, взятого из внутренней камеры. Прибавляют 1 каплю 5%-го раствора перманганата калия и оставляют на 10мин, а затем прибавляют 1-2 капли насыщенного раствора гидросульфита или сульфита натрия. После исчезновения окраски перманганата калия к жидкости прибавляют 0,2 мл 0,5%-го раствора хромотроповой кислоты в концентрированной серной кислоте. Жидкость в пробирке охлаждают в ледяной воде, а затем прибавляют 4 мл концентрированной серной кислоты и нагревают пробирку на кипящей водяной бане в течение 15мин.
Появление красной или фиолетовой окраски жидкости указывает на наличие метилового спирта в исследуемой пробе.
ГЖХ определение спиртов алифатического ряда.
Условия хроматографирования:
хроматограф с детектором катарометром;
металлическая колонка спиральной формы размером 150х0,4; твердый носитель: диатомитовый кирпич ИНЗ 600, модифициро-ванный серебром;
неподвижная жидкая фаза: ПЭГ 2000/20%/;
температура термостатов колонок и детектора 60о С, температура дозатора –комнатная;
газ-носитель- гелий, скорость гелия 28мл/мин
ток катарометра 100 мА,
делитель 265;
скорость ленты самописца 0,6 см/мин.
3.1.Качественное определение.
В три пенициллиновые флакона помещают по 0,5мл 50% раствора трихлоруксусной кислоты. В первый добавляют контрольную смесь спиртов алифатического ряда, во второй – 0,5 мл крови, в третий –0,5 мл мочи. Флаконы закрывают фиксирующимися пробками и в каждый шприцем вводят по 0,3 мл 30% раствора нитрита натрия. Флаконы встряхивают в течение 1 минуты и шприцем из каждого отбирают по 1 мл парогазовой фазы, вводят в колонку хроматогра-фа. При введении пробы из контрольного флакона появляются пики по числу компонентов смеси.
Порядок выхода алкилнитритов из колонки хроматографа:
1. Несорбирующиеся газы
2. Метилнитрит.
3. Этилнитрит.
4. Изопропилнитрит.
5. Пропилнитрит.
6. Изобутилнитрит.
7. Бутилнитрит.
8. Изоамилнитрит.
9. Амилнитрит.
При введении проб из второго и третьего флаконов, в случае наличия в них «летучих» ядов, появляются соответствующие пики. Определяют время удерживания (абсолютное исправленное) спиртов в контрольной смеси и в пробах. Сравнивают их и делают вывод о наличии (или отсутствии) спиртов в пробах крови и мочи.
Количественный анализ спиртов алифатического ряда.
Готовят эталонные растворы определяемого спирта с концентрациями 0,3;1,2,4 и 6 промилле. В две серии по семь пенициллиновых флаконов помещают по 0,5 мл 50% раствора трихлоруксусной кислоты и по 1 мл смеси равных объёмов: №1 -0,3%о спирта и 4%о пропанола, №2 -1%о спирта и 4%о пропанола, №3 - 2%о спирта и 4%о пропанола, №4 – 4%о спирта и 4%о пропанола, №5 -6%о спирта и 4%о пропанола, №6 - крови и 4%о пропанола, №7 - мочи и 4%о пропанола.
Все флаконы закрывают фиксирующимися пробками, в каждый вводят по 0,3 мл 30% нитрита натрия и флаконы встряхивают в течение 1 минуты. Затем шприцем из каждого флакона отбирают по 1 мл парогазовой фазы и вводят в колонку хроматографа. Измеряют высоты пиков, определяют отношения высот пиков определяемого спирта к высотам пиков пропилнитрита. По полученным данным строят калибровочный график и рассчитывают концентрацию определяемого спирта в исследуемых объектах.
Степень алкогольного опьянения этиловым спиртом определяют по таблице в Приложении, вывод о фазе метаболизма делают по соотношению концентрации этанола в крови и в моче.
ЗАНЯТИЕ № 9
| ТЕМА:
| Решение экспертной задачи. Анализ дистиллята на неизвестный «летучий яд».
|
| ЦЕЛЬ:
| Сформировать целостную картину проведения анализа дистиллята на неизвестный «летучий яд».
|
САМОСТОЯТЕЛЬНАЯ ПОДГОТОВКА СТУДЕНТА К ЗАНЯТИЮ:
На основании полученных знаний и практических навыков на занятиях 6 - 10 составьте схему анализа дистиллята на неизвестный «летучий яд».
Литература для самоподготовки:
1. Вергейчик Т.Х. Токсикологическая химия [Текст] / Т.Х.Вергейчик-М.:МЕДпресс-информ,2009-с.100-105,262-305.
2. Швайкова М.Д. Токсикологическая химия: Учебник. - М.: Медицина, 1975, - с. 63 - 119
3. Крамаренко В.Ф. Токсикологическая химия: Учебник. - М.: Медицина, 1989, - с. 107 - 172.
4. Белова А.В. Руководство к практическим занятиям по токсикологической химии. - М.: Медицина, 1976, - с. 6 - 56.
СОДЕРЖАНИЕ АУДИТОРНОГО ЗАНЯТИЯ:
1. Проведение студентом анализа задачи - дистиллята на неизвестный «летучий яд».
2. Оформление протокола занятия. Интерпретация полученных результатов.
ЗАНЯТИЕ № 10
КОНТРОЛЬНАЯ РАБОТА № 2
(по итогам занятий 6- 8)
ВОПРОСЫ ДЛЯ ПОДГОТОВКИ К КОНТРОЛЬНОЙ РАБОТЕ
1. Метод изолирования ядовитых веществ перегонкой с водяным паром. Теория метода. Азеотропная и неазеотропная перегонка.
2. Влияние рН среды на перегонку ядовитых веществ с водяным паром. Особенности изолирования цианидов, уксусной кислоты и тетраэтилсвинца.
3. Метод, применяемый для изолирования этиленгликоля из биологического материала.
4. Микродиффузия. Применение в ХТА «летучих ядов».
5. Газовая хроматография. Теория метода. Использование газовой хроматографии в ХТА ядовитых веществ.
6. Процесс хроматографирования. Подвижная и неподвижная фаза. Колонки сорбенты, газ носитель.
7. Процесс детектирования. Детектор. Типы детекторов.
8. Хроматограмма как источник информации о качественном и количественном содержании веществ. Качественные и количественные характеристики хроматограммы. Методы количественного ГХ анализа применяемые в токсикологической химии.
9. ГЖХ метод определения спиртов алифатического ряда.
10. Токсикологическое значение, особенности изолирования, ХТА синильной кислоты.
11. Токсикологическое значение, особенности изолирования, ХТА формальдегида.
12. Токсикологическое значение, особенности изолирования, ХТА алифатических спиртов. Алкогольное опьянение. Методы экспресс диагностики.
13. Токсикологическое значение, особенности изолирования, ХТА этиленгликоля.
14. Токсикологическое значение, особенности изолирования, ХТА ацетона.
15. Токсикологическое значение, особенности изолирования, ХТА фенолов.
16. Токсикологическое значение, особенности изолирования, ХТА галогенуглеводородов.
17. Токсикологическое значение, особенности изолирования, ХТА уксусной кислоты.
18. Токсикологическое значение, особенности изолирования, ХТА анилина и нитробензола.
19. Токсикологическое значение, особенности изолирования, ХТА тетраэтилсвинца.
20. Общая схема анализа дистиллята на неизвестный «летучий яд».
Литература для подготовки к контрольной работе:
1.Лужников Е.А. Клиническая токсикология: Учебник. - М.: Медицина, 1994, - с. 145 - 168.
2.Швайкова М.Д. Токсикологическая химия: Учебник. - М.: Медицина, 1975, - с. 63 – 119
3.Токсикологическая химия (под ред.Т.В.Плетенёвой).М.: ГЭОТАР –Медия,2005,с.314-340.
4.Крамаренко В.Ф. Токсикологическая химия: Учебник. - М.: Медицина, 1989, - с. 107 - 172.
5.Белова А.В. Руководство к практическим занятиям по токсикологической химии. - М.: Медицина, 1976, - с. 6 –54.
СОДЕРЖАНИЕ АУДИТОРНОГО ЗАНЯТИЯ:
1. Проведение рубежного тестового контроля.
2. Контрольная работа №3.
3. Написание акта судебно - химической экспертизы на основании данных полученных на занятии №9.
ЗАНЯТИЕ № 11
| ТЕМА:
| Экология Проблема химической безопасности окружающей среды. Ядохимикаты. Методы изолирования ядохимикатов. ХТА галогенпроизводных ядохимикатов.
|
| ЦЕЛЬ:
| Охарактеризовать основные проблемы химической безопасности окружающей среды. Сформировать знания и практические навыки по методам изолирования ядохимикатов, химико - токсикологическому анализу хлорорганических ядохимикатов.
|
САМОСТОЯТЕЛЬНАЯ ПОДГОТОВКА СТУДЕНТА К ЗАНЯТИЮ
Основные термины и понятия:
Экология. Промышленно - санитарное и судебно - химическое значение ядохимикатов. Классификация ядохимикатов. Акарициды. Антисептики. Бактерициды. Гербициды. Зооциды. Инсектициды. Фунгициды. Дефолианты. Десиканты. Репелленты. Остаточные количества ядохимикатов. Методы изолирования ядохимикатов. Гексахлорциклогексан (гексахлоран), гептахлор, ДДТ, метоксихлор, пертан, ДДД.
Логическая структура темы:
| ЯДОХИМИКАТЫ
|
| Классификации ядохимикатов
|
| Химическая
классификация
| Неорганические-
соли меди,ртути, цинка, мышьяка
|
| Органические
хлорорганические (ХОС)
фосфорорганические (ФОС) фенолы
производные карбаминовой кислоты
Синтетические пиретроиды
|
| Элементорганические
Ртутьорганические
Оловоорганические
|
| Практическая
классификация
| акарициды, инсектициды, антисептики, фунгициды, бактерициды, дефолианты гербициды, десиканты, зооциды, репелленты
|
| Классификация гигиеническая
| высокотоксичные, умереннотоксичные, малотоксичные
|
| Классификация инсектицидов по характеру проникновения
| контактные, кишечные,
системные, фунгициды
|
| Токсические свойства
|
| ХОС
| - кожнорезорбтивное действие
- поражают печень, почки
- яд ЦНС
- кумулируются,
вызывая остаточную токсичность
|
| ФОС
| - ингибирование холинэстеразы
- высокая инсектицидная активность
- отсутствует способность к кумулированию
- метаболизируются в печени
|
| Производные карбаминовой кислоты
Севин
| - ингибитор холинэстеразы
- гепатояд
|
| Фенолы
| - мембранотоксины
- кожнорезорбтивное (прижигающее) действие
|
| Пиретроиды
| - кумулируются
- вызывают возбуждение
- нарушение координации
- клонико-тонические судороги
- поражение ЖКТ
- парезы, параличи.
|
| Гранозан
| - кумулируется
- поражение жкт
- энцефалопатия
- психозы, паралич
- гематурия
|
| Методы изолирования ядохимикатов
|
| Экстракция неполярными растворителями
| Перегонка с водяным паром
|
| ХЛОРОРГАНИЧЕСКИЕ ЯДОХИМИКАТЫ
|
| Токсические свойства, Токсикокинетика, Токсикодинамика
|
| ХИМИКО - ТОКСИКОЛОГИЧЕСКИЙ АНАЛИЗ
|
| Группа ДДТ
|
| Изолирование
| Из твердого Б/м
-экстракция водой с серной кислотой и н-гексаном
Из биожидкостей
- экстракция диэтиловым эфиром
|
| Качественный анализ
| Определение органически связанного хлора
Нитрование с последующим
переводом в псевдоацисоль
ТСХ
ГЖХ
|
| Количественный анализ
| Аргентометрия
ФЭК метод Шахтера – Галлера
ГЖХ
|
| Группа ГХЦГ
|
| Изолирование
| Перегонка с водяным паром
|
| Качественный анализ
| Определение органически
связанного хлора
Нитрование -образование псевдо- ацисоли
Янтарная кислота и Fe2(SO4)3
ТСХ
ГЖХ
|
| Количественный анализ
| Аргентометрия
ФЭК
ГЖХ
|
| Группа гептахлора
|
| Изолирование
| Экстракция н-гексаном и диэтиловым эфиром
|
| Качественный анализ
| Диэтиламин в р-ре NaOH Диэтаноламин в р-ре NaOH
Анилин в пиридине
ТСХ и ГЖХ
|
| Количественный анализ
| ФЭК
ГЖХ
|
|
| |
| | | |
Литература для самоподготовки:
1. Швайкова М.Д. Токсикологическая химия: Учебник. - М.: Медицина, 1975, - с. 246 - 278
2. Крамаренко В.Ф. Токсикологическая химия: Учебник. - М.: Медицина, 1989, - с. 393 - 415.
3. Белова А.В. Руководство к практическим занятиям по токсикологической химии. - М.: Медицина, 1976, - с. 190 - 221.
4. Лужников Е.А. Клиническая токсикология: Учебник. - М.: Медицина, 1994, - с. 168 - 189.
5.Токсикологическая химия (под ред.Т.В.Плетенёвой).-М.: ГЭОТАР –Медия,2005,с.340-350,357-358.
6.Лекции по токсикологической химии.
Вопросы для самоподготовки:
1. Какие основные источники отравления ядохимикатами?
2. Перечислите виды классификаций ядохимикатов.
3. Какие ядохимикаты изолируются методом перегонки с водяным паром? В чем заключается особенность их изолирования?
4. Как осуществляется изолирование этилмеркурхлорида, который входит в состав ядохимиката «Гранозан», из внутренних органов трупа?
5. Охарактеризуйте основные токсические свойства хлороргани-ческих ядохимикатов.
6. Объясните термин «персистентность».
7. Что является основным метаболитом ядохимикатов группы ДДТ?
8. Какой ядохимикат группы ХОС подвергается метаболизму по «летальному» синтезу?
9. Какой детектор используется для ГЖХ анализа на ядохимикаты группы ХОС?
10. В чем заключается метод ФЭК определения пестицидов группы ДДТ и гексахлорциклогексана?
11. Что является проявителем в методе ТСХ определения ХОС?
Тестовый контроль по теме:
ТЗ 1-2.Установите соответствие
Ядохимикат Группа ядохимикатов
| 1. Карбарил
2. Метафос
| А. Ртутьорганические
Б. ФОС
В. ХОС
Г. Производные карбаминовой кислоты
Д. Фенолы
|
ТЗ 3.Вещества, применяемые для борьбы с болезнями растений называются........
ТЗ 4. Метод, используемый для изолирования гексахлорцикло-гексана из внутренних органов трупа
1. Экстракция гексаном. 2. Перегонка с водяным паром. 3. Минерализация. 4. Микродиффузия. 5. Экстракция спиртовым раствором серной кислоты.
ТЗ 5 –6. Установите соответствие
Объект исследования Метод изолирования из биоматериала
| 1. ДДТ
2. Гранозан
| А. Экстракция полярными растворителями
Б. Экстракция неполярными растворителями
В. Перегонка с водяным паром
Г. Прямая перегонка
Д. Минерализация
|
ТЗ 7. Название группы ядохимикатов, используемой для борьбы с сорными растениями.........
ТЗ 8 -9. Установите соответствие
Вещество Структурная формула
| 1. ДДТ
2. Гепта-хлор
| А. 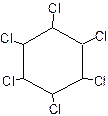
| Б. 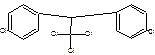
| В. 
|
|
|
Г.

|
Д.
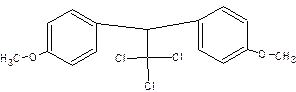
|
ТЗ 10. Хлорорганические ядохимикаты в организме человека накапливаются в....... ткани.
ТЗ 11. Реактив- проявитель в ТСХ определении ХОС.
1. Диэтаноламин в растворе NaOH. 2. Водно-ацетоновый раствор аммиаката серебра. 3. Янтарная кислота, сульфат железа (III). 4. Анилин. 5. Хлоруксусная кислота.
ТЗ 12. Метаболитом гептахлора является соединение........
ТЗ 13-14. Установите соответствие
Ядохимикат Реактив обнаружения
| 1. ГХЦГ
2. Гептахлор
| А. Диэтаноламин в растворе NaOH
Б. Хлорид железа (III)
В. Пикриновая кислота
Г. 4-аминоантипирин
Д. Янтарная кислота и сульфат железа (III)
|
ТЗ 15. Детектор, используемый для определения ХОС ГЖХ методом.
1. Пламенно - фотометрический. 2. Масс - детектор. 3. Катарометр.4.Электрон захватный. 5. ИК - спектрофотометрический.
СОДЕРЖАНИЕ АУДИТОРНОГО ЗАНЯТИЯ
1. Контроль выполнения домашнего задания.
2. Семинар по теме занятия.
3. Оформление протокола практического занятия.
4. Тестовый контроль усвоения темы.
ЗАНЯТИЕ № 12
| ТЕМА:
| Химико - токсикологический анализ ядохимикатов производных ФОС, карбаминовой кислоты, ртутьорганических пестицидов и синтетических пиретроидов. ГЖХ –анализ пестицидов.
|
| ЦЕЛЬ:
| Сформировать знания в области химико - токсикологического анализа ядохимикатов производных ФОС, карбаминовой кислоты, синтетических пиретроидов.
|
САМОСТОЯТЕЛЬНАЯ ПОДГОТОВКА СТУДЕНТА К ЗАНЯТИЮ
Основные термины и понятия, ключевые соединения:
Инсектицид, холинэстеразная проба. Хлорофос, метафос, карбофос, трихлорметафос, дихлофос, карбарил (севин). Пиретрины и синтетические пиретроиды. Перметрин, циперметрин, дельтаметрин.
Логическая структура темы:
 ЯДОХИМИКАТЫ ПРОИЗВОДНЫЕ ФОС ЯДОХИМИКАТЫ ПРОИЗВОДНЫЕ ФОС
|
| Токсические свойства, Токсикокинетика, Токсикодинамика
|
| ХИМИКО - ТОКСИКОЛОГИЧЕСКИЙ АНАЛИЗ
|
| Изолирование
|
| Качественное обнаружение
|
| Общегрупповые тесты
|
| Холинэстеразная проба
| Обнаружение фосфора
| о - толидин и Н2О2
|
| Частные реакции
|
| Хлорофос, Дихлофос
| реакция Фудживара
резорцин
образование изонитрила
2,4 -динитрофенилгидразин ацетон в спиртовом растворе NaOH
|
| Карбофос
| диазотированная
сульфаниловая кислота
реактив Марки
|
| Метафос
| о - дианизидин и NaBO4
после гидролиза:
образование индофенолового красителя
восстановление и реакция образования азокрасителя
с FeCI3
|
| Количественное определение
|
| ФЭК, ГЖХ
|
| ЯДОХИМИКАТЫ ПРОИЗВОДНЫЕ КАРБАМИНОВОЙ КИСЛОТЫ
|
| Карбарил
|
| Качественное обнаружение
пикриновая
кислота
CuCl2 и KBr
4 – аминоантипирин
и K4[Fe(CN)6]
ТСХ, ГЖХ
| Количественное определение ФЭК по реакции с CuCl2 и KBr; ГЖХ
|
| ПИРЕТРИНЫ И ПИРЕТРОИДЫ
|
| Качественное обнаружение Реактив Дениже,
Реактив Драгендорфа
ТСХ, ГЖХ, ВЭЖХ
| Количественное определение ГЖХ, ВЭЖХ.
|
| РТУТЬСОДЕРЖАЩИЕ ЯДОХИМИКАТЫ
|
| Гранозан
|
| Качественное обнаружение Дитизон
Медная проволока, реакция Полежаева
ТСХ, ГЖХ
| Количественное определение ФЭК
ГЖХ
|
| | | | |
Литература для самоподготовки:
1.Швайкова М.Д. Токсикологическая химия: Учебник. - М.: Медицина, 1975, - с. 262 - 278
2.Крамаренко В.Ф. Токсикологическая химия: Учебник. - М.: Медицина, 1989, - с. 399 - 415.
3.Белова А.В. Руководство к практическим занятиям по токсикологической химии. - М.: Медицина, 1976, - с. 207 - 221.
4.Лужников Е.А. Клиническая токсикология: Учебник. - М.: Медицина, 1994, - с. 168 - 189.
5.Токсикологическая химия (под ред.Т.В.Плетенёвой).М.: ГЭОТАР –Медия,2005,с.348-358.
6.Лекции по токсикологической химии.
Вопросы для самоподготовки:
1. Какие преимущества и недостатки фосфорорганических ядохимикатов?
2. Как выполняется холинэстеразная проба на фосфорорганические ядохимикаты?
3. Какой реактив используется в качестве проявителя в ТСХ анализе ФОС?
4. Как выделяется карбарил из биологического материала и с помощью, каких реакций его можно обнаружить в вытяжках?
5. На каких реакциях основано ФЭК определение ФОС и карбарила?
6. Что такое пиретроиды? Чем они отличаются от пиретринов?
7. Какие методы применяют для изолирования пиретроидов из биоматериала?
Тестовый контроль по теме:
ТЗ.1-2.Установите соответствие
Ядохимикат Структурная формула
| 1. Карбарил
2. Метафос
| 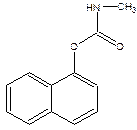 А.
А.
| Б.
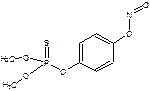
| В.

|
|
| Г.
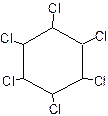
| Д.
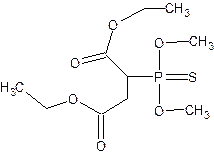
|
ТЗ.3. Название энзиматического метода определения ФОС в биологических жидкостях........
ТЗ.4.Растворитель, используемый для изолирования хлорофоса из твердого биологического материала
1. Водный раствор серной кислоты. 2. Спиртовой раствор серной кислоты. 3. Гексан. 4. Эфир. 5. Хлороформ.
ТЗ.5.Реактив- проявитель при ТСХ скрининге ФОС
1. Марки. 2. Фреде. 3. О - толидин и H2O2. 4. Фелинга. 5. Серебра нитрат.
ТЗ. 6-7.Установите соответствие
Ядохимикат Метаболит
| 1. Дихлофос
2. Карбарил
| А. Ацетальдегид
Б. Бета - нафтол
В. Нафталин
Г. Альфа - нафтол
Д. Дихлорацетальдегид
|
ТЗ. 8. Ядохимикат, обладающий метгемоглобинобразующим действием.
1. ДДТ.2. Метафос.3. Гексахлоран.4. Карбарил. 5. Гептахлор
ТЗ. 9. Реакция,используемая для ФЭК определения Севина
1. С хлоридом железа (III). 2.С бромидокупратом калия. 3. С аминопиридином. 4.С нитритом натрия. 5. С диазотированной сульфаниловой кислотой.
ТЗ.10. Общегрупповой качественный тест на ФОС
1. Холинэстеразная проба. 2. Реакция Фудживара. 3. С реактивом Марки. 4. С 2.4-динитрофенилгидразином. 5. С о - дианизидином и NaBO4.
СОДЕРЖАНИЕ АУДИТОРНОГО ЗАНЯТИЯ
1. Контроль выполнения домашнего задания.
2. Практикум по теме занятия.
3. Оформление протокола практического занятия.
4. Тестовый контроль усвоения темы.
ПРАКТИКУМ
1.Качественные реакции на хлорофос.
1.1.Реакция Фудживара.
В пробирку вносят 1 мл исследуемого раствора, 1 мл пиридина и 1 мл 30% раствора гидроксида натрия. Смесь нагревают на кипящей водяной бане 5 мин. При наличии хлорофоса в пробе появляется красная или розовая окраска.
1.2. Реакция с резорцином.
В пробирку вносят 1 мл исследуемого раствора, 2 капли 1% раствора резорцина в 20% растворе карбоната натрия или 15% растворе гидроксида натрия. Через 10 мин появляется розовая окраска, а через 15-30 мин наблюдается жёлто-зелёная флуоресценция раствора. Окраска и флуоресценция раствора достигают максимума через 1-2 ч после прибавления реактивов к исследуемому раствору. Через 4-6 часов розовая окраска переходит в оранжевую, а затем в жёлтую. Флуоресценция раствора сохраняется в течение нескольких суток.
1.3. Реакция с ацетоном.
В пробирку вносят 0,1-0,5 мл раствора исследуемого вещества в этиловом спирте, прибавляют 1 мл ацетона и 0,5 мл 0,5 н спиртового раствора гидроксида натрия. При наличии хлорофоса в пробе через 5-15 мин появляется розовая окраска. Переходящая в оранжевую.
2.Реакции на карбофос.
2.1. Реакция с диазотированной сульфаниловой кислотой.
0,5 мл исследуемого раствора вносят в пробирку и выпаривают досуха. К сухому остатку прибавляют 2 мл воды, 0,5 мл 5% раствора гидроксида натрия и реактива Паули (диазотированной сульфаниловой кислоты). Появление вишнево-красной окраски указывает на наличие карбофоса в исследуемом растворе.
2.2. Реакция с реактивом Марки.
В фарфоровую чашку вносят 0,5мл исследуемого раствора и выпаривают досуха. К сухому остатку прибавляют 5-10 капель реактива Марки. Появление оранжевой окраски, которая через некоторое время переходит в тёмно-коричневую, указывает на наличие карбофоса в исследуемом растворе.
3.Обнаружение фосфат-ионов.
В пробирку вносят 3-5 капель минерализата и прибавляют 5 капель раствора молибдата аммония. Смесь подкисляют 10% раствором азотной кислоты. При наличии фосфат ионов появляется жёлтая окраска. К этому раствору прибавляют 3-5 капель насыщенного водного раствора гидрохлорида бензидина. Затем прибавляют 10% раствор аммиака до щелочной реакции. При наличии фосфат-ионов в минерализате появляется синяя окраска.
ЗАНЯТИЕ № 13
ЗАЧЕТНОЕ ЗАНЯТИЕ
СОДЕРЖАНИЕ АУДИТОРНОГО ЗАНЯТИЯ
1. Написание семестрового и итогового тестового контроля.
2. Подведение итогов семестра.
3. Зачет по практическим навыкам.
Перечень вопросов для зачёта по практическим навыкам
1. ГЖХ анализ спиртов алифатического ряда.
2. Минерализация по методу Равданикиса.
3.Холинэстеразная проба.
4.Изолирование ядовитых, наркотических и сильнодействующих веществ методом Васильевой.
5.Изолирование ядовитых, наркотических и сильнодействующих веществ из биожидкостей.
6.ТСХ-скрининг ядовитых, наркотических и сильнодействующих веществ.
ПРИЛОЖЕНИЕ
Таблица I



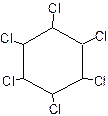
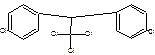


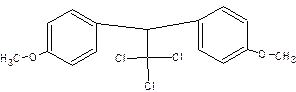
 ЯДОХИМИКАТЫ ПРОИЗВОДНЫЕ ФОС
ЯДОХИМИКАТЫ ПРОИЗВОДНЫЕ ФОС
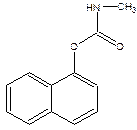 А.
А.