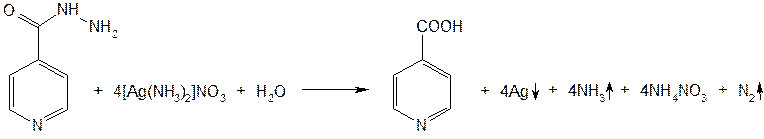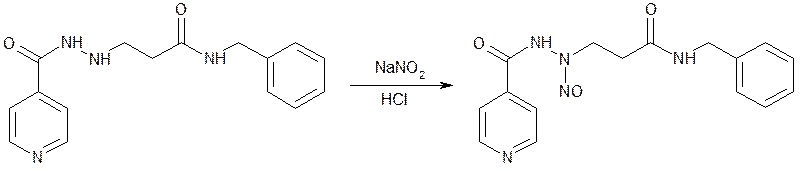Статистика по развивающимся странам утверждает, что туберкулез ответствен за одну из четырех смертей. Во всем мире ежегодно умирает от туберкулеза около трех миллионов человек (данные на начало 90-х годов). К настоящему времени многие разновидности туберкулезных микобактерий (Micobacterium tuberculosis), селящиеся в легких человека, выработали резистентность к действию большой части когда-то эффективных противотуберкулезных препаратов.
В настоящее время приходится применять комбинации из нескольких лекарств для более успешной борьбы с возбудителями туберкулеза. Однако уже стали известны случаи устойчивости некоторых мутантных микобактерий и к комплексным средствам, в которые могут входить до семи различных препаратов. В самое последнее время появилось сообщение, что найден способ блокирования биосистем, используемых патогенными бактериями для быстрой выработки ими резистентности к антибактериальным лекарственным веществам, что дает надежду на возвращение к многим старым препаратам (особенно пенициллинам). Одним из наиболее широко используемых с 1952 г. антитуберкулезных средств является и малотоксичный гидразид 4-пиридинкарбоновой кислоты - изониазид. Он является антагонистом никотинамида, контролирующего внутриклеточные редокс-процессы. Точный механизм его действия на микобактерии пока неизвестен, хотя предполагают, что он может блокировать фермент, ответственный за биосинтез высших жирных кислот, участвующих в формировании стенок микобактериальных клеток.
Изониазид синтезируют по следующей схеме:
· Методом Чичибабина получают 4-пиколин и окисляют его в изоникотиновую кислоту или в ее нитрил.
· Затем действием гидразина превращают ее эфир или нитрил в целевой гидразид.
· Конденсацией ванилина с изониазидом получают еще один противотуберкулезный препарат - фтивазид, обладающий меньшей токсичностью, чем его предшественник:

Высокой способностью подавлять развитие микобактерий обладают также тиоамиды - этионамид и протионамид, введенные в практику 45 лет назад. Эти производные имеют строение амидов тиоизоникотиновой кислоты. Их синтезируют на основе пиколина. Сначала действием фениллития и соответствующего алкилгалогенида наращивают метильную группу до этильной или пропильной, а затем оба гомолога окисляют в N-оксиды и хлорируют их трихлороксидом фосфора до 4-хлорпиридинов. В последних нуклеофильно замещают хлор на циангруппу и затем в соединении (35) действием сероводорода превращают циангруппу в тиоамидную, получая искомые противотуберкулезные тиоамиды (36) и (37):

Гидразидными производными пиридинкарбоновой кислоты являются также ипразид и ниаламид, которые, однако, используются в качестве антидепрессантов, а не бактерицидов:

Считается, что механизм их действия заключается в ингибировании фермента моноаминооксидазы (МАО), который отвечает за дезактивацию в организме медиаторов нервного возбуждения.
Эти препараты необратимо связывают МАО, что приводит к прекращению окислительного дезаминирования норадреналина, дофамина и серотонина, к их накоплению в участках мозга и, таким образом, к улучшению передачи нервных импульсов и снятию тяжелых депрессий у психически больных.
Метод синтеза фтивазида.
Работы в области синтеза и исследования гидразидов и гидразонов как противотуберкулезных средств были начаты в 1951 г. во ВНИХФИ под руководством М.Н.Щукиной. Синтезировано около 100 различных соединений, из которых применяют изониазид, фтивазид, метазид и др.
Изониазид (гидразид изоникотиновой кислоты) — исходный продукт для получения других производных изоникотиновой кислоты. Синтез фтивазида осуществляют из гидразида изоникотиновой кислоты и ванилина (3-метокси-4-оксибензальдегида):

Гидразид изоникотиновой кислоты явился источником синтеза его карбамоилпроизводных, в частности отечественного лекарственного вещества ниаламида (табл. 7), представляющего собой 2-[2-(бензилкарбамоил)-этил] гидразид изоникотиновой кислоты.
Синтезируют ниаламид по схеме:

Ниаламид в отличие от рассмотренных производных изоникотиновой кислоты не обладает противотуберкулезным действием. Присоединение к гидразиновой части молекулы радикала, включающего карбамоильную группу, привело к созданию антидепрессанта — ингибитора моноаминоксидазы. По физическим свойствам (табл. 7) производные изоникотиновой кислоты представляют собой кристаллические порошки белого, светло-желтого или желтого цвета. Фтивазид отличается выраженной желтой окраской и запахом ванилина.
Табл. №7. Свойства производных изоникотиновой кислоты.
| Лекарственное вещество
| Химическая структура
| Описание
|
| Isoniazid— изониазид
|  гидразид изоникотиновой кислоты гидразид изоникотиновой кислоты
| Белый кристаллический порошок без запаха. Т. пл. 170–174 °C
|
| Ftivazide— фтивазид
|  3-метокси-4-оксибензилиденгидразид изоникотиновой кислоты, моногидрат 3-метокси-4-оксибензилиденгидразид изоникотиновой кислоты, моногидрат
| Светло-желтый или желтый мелкокристаллический порошок со слабым запахом ванилина
|
| Nialamide— ниаламид
|  2-[2-(бензилкарбамоил)-этил] гидразид изоникотиновой кислоты 2-[2-(бензилкарбамоил)-этил] гидразид изоникотиновой кислоты
| Белый мелкокристаллический порошок без запаха. Т.пл. 151-153 °C
|
Изониазид легко растворим в воде, умеренно растворим в этаноле; ниаламид мало растворим, фтивазид практически не растворим в воде. В этаноле фтивазид очень мало растворим, а ниаламид — умеренно растворим. В хлороформе ниаламид мало растворим, изониазид очень мало растворим. Ниаламид и фтивазид легко растворимы в минеральных кислотах. Фтивазид растворим в растворах едких щелочей.
Лекарственные вещества, производные изоникотиновой кислоты, обладают способностью к таутомерным превращениям:

При этом они могут проявлять в растворах как кислотные, так и основные свойства, которые характеризуются константами ионизации. Так, например, изониазид при pH ниже 1,6 проявляет себя в растворе как основание, а при pH 13,15 и выше как кислота. В области значений pH от 6,6 до 8,1 на 99% изониазид будет находиться в неионизированной форме. Исходя из этого, подбирают индикаторы для кислотно-основного титрования, а затем условия определения производных изоникотиновой кислоты спектрофотометрическим методом.
Подлинность изониазида и фтивазида устанавливают по ИК-спектрам, снятым в вазелиновом масле в области 3700-400 см–1. Они должны полностью совпадать с полосами поглощения прилагаемого к распечатке спектра по положениям и интенсивностям полос.
В федеральный стандарт (ФС) включены способы идентификации производных изоникотиновой кислоты по УФ-спектрам поглощения. Раствор изониазида в 0,1 М растворе хлороводородной кислоты в области 220-350 нм имеет максимум поглощения при 266 нм и минимум поглощения при 234 нм, ниаламида в том же растворителе — максимум поглощения при 267 нм и минимум поглощения при 236 нм. Удельный показатель поглощения 0,002%-ного раствора ниаламида в хлороводородной кислоте равен 185-195. УФ-спектр раствора фтивазида в хлороводородной кислоте в области 215-400 нм имеет максимумы поглощения при 229, 274, 309 нм и минимумы поглощения при 247 и 298 нм.
Испытания на подлинность и количественное определение производных изоникотиновой кислоты основаны на химических реакциях, обусловленных наличием в их молекулах цикла пиридина и гидразина, а также реакциях гидролиза, кислотно-основных и восстановительных свойствах.
Подлинность производных изоникотиновой кислоты устанавливают, используя в качестве реактива 2,4-динитрохлорбензол. После кипячения лекарственного вещества и реактива в этаноле, охлаждения и добавления раствора гидроксида натрия появляется буро-красное (изониазид) или желто-бурое (фтивазид) окрашивание, усиливающееся или изменяющееся при стоянии. Это общая реакция на пиридиновый цикл. Пиридиновый цикл в молекуле ниаламида обнаруживают, нагревая на кипящей водяной бане с уксусным ангидридом в присутствии лимонной кислоты; смесь приобретает вишневое окрашивание.
Известны и другие цветные реакции на производные изоникотиновой кислоты. В качестве реактивов используются нингидрин в присутствии гидроксида натрия, разведенная серная или хлороводородная кислота, концентрированная серная кислота, смесь камфоры или тимола с концентрированной серной кислотой, раствор дихромата калия в разведенной серной кислоте. Как и другие соединения третичного азота, производные изоникотиновой кислоты образуют окрашенные осадки с раствором фосфорномолибденовой кислоты и некоторыми другими осадительными (общеалкалоидными) реактивами.
Для испытания подлинности изониазида и ниаламида используют восстановительные свойства, обусловленные наличием остатка гидразина в их молекулах. При взаимодействии изониазида с аммиачным раствором нитрата серебра выделяется серого цвета осадок, а при нагревании на стенках сосуда осаждается серебро, т.е. происходит реакция «серебряного зеркала»:
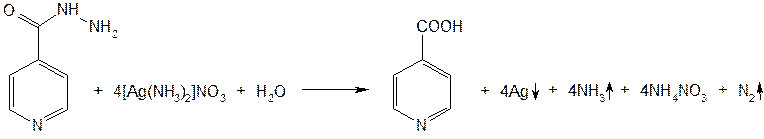
Идентифицировать изониазид можно также по характерной цветной реакции с раствором сульфата меди (II). Вначале образуется медная комплексная соль изониазида (голубого цвета), а затем происходит гидролиз и окисление гидразида солью меди (II), что сопровождается изменением окраски раствора от голубой до изумрудно-зеленой и грязно-желтой. Наблюдается выделение пузырьков газа (азота), а ион меди (II) восстанавливается до оксида меди (I):

Изониазид дает цветную реакцию со щелочным раствором нитропруссида натрия. Появляется оранжевое окрашивание, которое после добавления хлороводородной кислоты переходит в вишневое.
Гидразин, образующийся при щелочном гидролизе изониазида, обнаруживают цветной реакцией с n -диметиламинобензальдегидом в кислой среде. Возникает желто-оранжевая окраска, обусловленная конденсацией альдегида и гидразина с образованием хиноидного катиона:

Изониазид идентифицируют по образованию фтивазида при добавлении горячего раствора ванилина (см. схему синтеза фтивазида). Образующийся при стоянии желтый осадок после перекристаллизации из этанола и высушивания должен иметь температуру плавления около 227°C.
Фтивазид, обладая амфотерными свойствами, растворяется как в растворах гидроксидов (за счет наличия в молекуле фенольного гидроксила), так и в кислотах (за счет третичного азота). При этом образуются феноксиды или соли, имеющие различную окраску. Это свойство используют для испытания его подлинности. Так, спиртовой раствор фтивазида от добавления раствора щелочи приобретает оранжево-желтое окрашивание. Последующее постепенное прибавление раствора хлороводородной кислоты приводит вначале к ослаблению, а затем к усилению окраски до оранжево-желтой (за счет образования четвертичной соли с атомом азота в пиридиновом цикле):

При нагревании раствора фтивазида в разведенной хлороводородной кислоте происходит его гидролиз с образованием гидразина, изоникотиновой кислоты и ванилина. Ванилин легко обнаружить по характерному запаху:

Ванилин можно идентифицировать с помощью химических реакций на альдегиды с использованием в качестве реактивов первичных ароматических аминов.
При испытании на чистоту устанавливают допустимые пределы примесей исходных продуктов синтеза и гидролиза. В изониазиде методом ТСХ на пластинках Силуфол или Сорбфил УФ-254 обнаруживают примесь свободного гидразина (не более 0,02%). Тем же методом определяют посторонние примеси (не более 1%) в ниаламиде, сравнивая с СОВС. Во фтивазиде обнаруживают присутствие примесей гидразида изоникотиновой кислоты (нитритометрическим методом) и ванилина (нейтрализацией 0,05 М раствором гидроксида натрия водного извлечения по фенолфталеину).
Количественное определение изониазида и фтивазида выполняют методом неводного титрования 0,1 М раствором хлорной кислоты (индикатор кристаллический фиолетовый). Изониазид предварительно растворяют в смеси ледяной уксусной кислоты и уксусного ангидрида, а фтивазид — в смеси муравьиной кислоты и уксусного ангидрида (2:30). В случае фтивазида процесс идет по схеме:

Ряд методик количественного определения изониазида и фтивазида основан на окислении продуктов гидролиза, например, при использовании иодометрии. Окисление ведут иодом в слабощелочной среде:

Изониазид определяют также броматометрическим методом в солянокислой среде:
KBrO3 + 5KBr + 6HCl ¾® 3Br2 + 6KCl + 3H2O

Избыток брома устанавливают иодометрическим методом.
К этой же группе относятся способы определения, основанные на применении ванадатометрического и цериметрического методов. Оксидиметрические методы определения изониазида основаны также на действии дихроматом калия, избыток которого титруют раствором соли Мора, или хлорамином Т с иодометрическим титрованием избытка окислителя.
Фтивазид количественно определяют иодатометрическим методом после предварительного гидролиза в солянокислой среде. Выделяющийся при гидролизе гидразин окисляют иодатом калия в присутствии хлороформа. Образующийся иод извлекают реакционной массы хлороформом. При последующем титровании иод превращается в бесцветный иода хлорид (слой хлороформа обесцвечивается):

5H2N–NH2 + 4KIO3 + 4HCl ¾® 5N2 + 2I2 + 4KCl + 12H2O
KIO3 + 2I2 + 6HCl ¾® 5ICl + KCl + 3H2O
Из других химических методов для количественного определения изониазида используют нитритометрию. Разработан унифицированный способ количественного определения изониазида, фтивазида и других производных изоникотиновой кислоты, основанный на применении нитритометрии с внутренними индикаторами (Л.Н.Гусева). Можно предположить, что при воздействии на изониазид нитритом натрия происходит образование азида изоникотиновой кислоты:

Количественное определение ниаламида выполняют нитритометрическим методом, используя внутренний индикатор — смесь тропеолина 00 и метиленового синего. Определение основано на образовании нитрозопроизводного ниаламида:
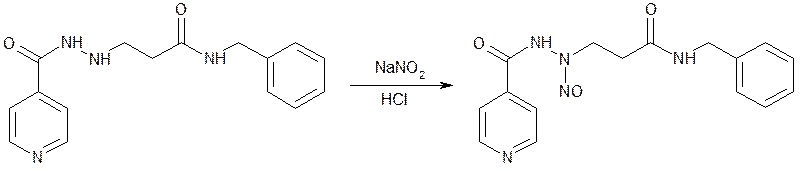
Обратное аргентометрическое определение изониазида основано на образовании комплексов с солями меди и кадмия. Изониазид можно определить косвенным комплексонометрическим методом с помощью иодвисмутата калия.
Фотометрические методы определения производных изоникотиновой кислоты основаны на образовании окрашенных продуктов с ванадатом аммония, 2,3-дихлор-1,4-нафтохиноном, 1,2-нафтохинон-4-сульфонатом натрия. В качестве реактивов для фотометрического определения изониазида используют также реакции с n-диметиламинобензальдегидом, пирокатехином в щелочной среде, 9-хлоракридином, фторборатом n -нитрофенилдиазония, глутаконовым альдегидом, хлоридом трифенилтетразолия и другими реактивами. Спектрофотометрическое определение можно выполнить и по собственному поглощению в 0,1 М растворе хлороводородной кислоты при 267 нм (изониазид, ниаламид), 274 нм (фтивазид).
Производные изоникотиновой кислоты хранят по списку Б в хорошо укупоренной таре, в прохладном, защищенном от света сухом месте.








 гидразид изоникотиновой кислоты
гидразид изоникотиновой кислоты
 3-метокси-4-оксибензилиденгидразид изоникотиновой кислоты, моногидрат
3-метокси-4-оксибензилиденгидразид изоникотиновой кислоты, моногидрат
 2-[2-(бензилкарбамоил)-этил] гидразид изоникотиновой кислоты
2-[2-(бензилкарбамоил)-этил] гидразид изоникотиновой кислоты