Физиология иммунной системы
1.1. Понятие об иммунитете и иммунной системе
Иммунитет – это защита организма от любых агрессивных факторов: физических, химических или биологических. В более узком смысле, иммунитет (лат. immunities – освобождение от чего-то) – способность организма распознавать и уничтожать любые субстанции, несущие чуждую генетическую информацию. Таковыми могут быть другие организмы (паразиты, микробы, вирусы), трансплантаты, чужеродные сложные органические вещества, а также собственные измененные клетки, подвергающиеся регенерации или ставшие излишними.
В иммунитете участвуют две системы:
1. Неспецифические факторы защиты от любого патогенного или чужеродного начала – врождённые, имеют видовые особенности, передаются по наследству.
Животные с пониженной резистентностью плохо адаптируются к любым изменениям окружающей среды и подвержены как инфекционным, так и неинфекционным болезням.
2. Высокоспециализированная иммунная система, реагирующая на конкретный антиген клеточными и гуморальными реакциями, направленными на его обезвреживание и выведение из организма.
Иммунная система сохраняет генетический гомеостаз организма, его индивидуальность, защищает от конкретных возбудителей болезней. В этом смысле иммунитет индивидуален и по наследству не передается.
Органы иммунной системы
Органы иммунной системы подразделяют на центральные и периферические. Связь между ними обеспечивается нервной, эндокринной, кровеносной и лимфатической системами. Важной особенностью иммунной системы является непрерывная циркуляция лимфоцитов между центральными и периферическими органами.
К центральным органам иммунной системы относятся красный костный мозг и тимус, а у птиц, кроме того, Фабрициева сумка (бурса). В центральных органах происходит первая фаза дифференцировки лимфоцитов, независимая от присутствия антигенов. Здесь образуются достаточно зрелые лимфоциты, имеющие ряд рецепторов и маркеров на мембране, но еще физиологически неактивные, неспособные выполнять свои специфические функции.
В красном костном мозге из полипотентных стволовых клеток начинают развиваться все форменные элементы крови. На ранней стадии развития лимфоциты дифференцируются на предшественников Т и В-клеток, они ещё незрелые и морфологически неотличимые, но снабжены соответствующими маркерами.
Будущие, или пре-Т-лимфоциты выходят из красного костного мозга и через кровь попадают в тимус – вилочковую железу. Здесь они заселяют корковую зону, где активно размножаются и созревают, обучаются распознавать свои клетки, приобретают различные рецепторы и маркеры на мембранах. В этих процессах участвуют гормоны тимуса. Постепенно зрелые Т-лимфоциты переходят в мозговую зону тимуса, а оттуда – в кровеносные сосуды. Т-лимфоциты, не обладающие свойством распознавать свои и чужие клетки, подлежат уничтожению макрофагами до выхода их из тимуса в кровоток. Поэтому около 95 % Т-лимфоцитов погибают в тимусе, и только малая их часть попадает в кровоток. Этим предотвращается развёртывание иммунной реакции против собственных клеток и тканей.
Характерной особенностью тимуса является его возрастная инволюция. Уже после подсосного периода тимус начинает уменьшаться в размерах, особенно значительная атрофия наступает в период полового созревания. Хотя полностью тимус не исчезает, его значение теряется. К этому времени в организме накопилось уже достаточное количество долгоживущих клеток памяти, а регуляторные и эффекторные Т-лимфоциты пролиферируют (размножаются) в периферических иммунных органах.
У птиц пре-В-лимфоциты после выхода из красного костного мозга заселяют фабрициеву сумку, где превращаются в В-лимфоциты. У млекопитающих В-лимфоциты все стадии антигеннезависимой дифференцировки проходят в красном костном мозге. Отсюда они выходят в кровоток, имея на поверхности антитела класса IgM, и заселяют периферические иммунные органы.
Периферическими органами иммунной системы являются селезёнка, лимфатические узлы, лимфатические фолликулы, кожа. Здесь происходит активация и пролиферация лимфоцитов в результате встречи с антигенами, здесь вырабатываются и накапливаются антитела, и здесь разыгрываются иммунные реакции.
Лимфатические узлы. В корковой части лимфатических узлов находятся первичные фолликулы, содержащие центры размножения лимфоцитов и ретикулярных клеток. Корковый слой лимфатических узлов называется тимуснезависимым, так как активация и пролиферация В-лимфоцитов при введении антигена происходит здесь без участия Т-лимфоцитов.
Ниже кортикального (коркового) слоя расположен паракортикальный слой, или глубокая кора. Это – тимусзависимая зона, она атрофируется после удаления тимуса и значительно увеличивается в размере во время иммунного ответа по клеточному типу, то есть с участием Т-лимфоцитов.
В мозговой зоне лимфоузлов в процессе иммунного ответа накапливаются плазматические клетки.
Селезёнка. Лимфоидная ткань селезёнки участвует преимущественно в иммунных реакциях гуморального типа. В ней происходит обмен лимфоцитами между кровью и лимфоидной тканью, а во время иммунного ответа накапливаются плазматические клетки. Поскольку в селезёнке нет лимфатической системы, циркуляция лимфоцитов осуществляется только через кровеносные сосуды и красную пульпу.
Селезёнка осуществляет контроль за цитологическим составом крови, в ней разрушаются и удаляются из крови утратившие функциональную активность эритроциты и лейкоциты («кладбище эритроцитов»).
Лимфоидная ткань расположена вдоль пищеварительного тракта, дыхательных и мочеполовых путей, то есть в местах проникновения антигенов из внешней среды. По своим функциям она сходна с лимфатическими узлами и селезёнкой.
Кожа не является лимфоидным органом, но в коже имеется много лимфоидной ткани, скопления лимфоцитов, макрофаги – клетки Лангерганса и дендритные (ретикулярные) клетки. Указанные структуры обеспечивают защиту организма от патогенных микробов, проникших через кожный барьер, от опухолей, кожного трансплантата.
При внутрикожном введении антигена вначале развивается местная иммунная реакция. Такую местную иммунизацию в медицине и ветеринарии применяют для прижизненной диагностики ряда болезней – например, туберкулеза, а сама процедура называется туберкулинизацией. Если животное не заражено туберкулезом, в крови его отсутствуют специфические антитела и реакция на туберкулин не дает клинических признаков (отрицательная проба). Если животное больное, и в крови имеется высокий уровень антител, появляется ограниченный отёк кожи, покраснение, местное повышение температуры и болезненность, а иногда развивается и общая реакция организма (положительная проба).
Миграция (рециркуляция) лимфоцитов. В организме происходит постоянная рециркуляция лимфоцитов между центральными и периферическими органами. Из костного мозга пре-Т-лимфоциты переходят по кровеносным сосудам в тимус, затем мигрируют в лимфатические узлы и селезёнку, где заселяют тимусзависимые зоны. Оттуда они поступают в кровь или лимфу. В области капилляров и венул Т-лимфоциты проходят по межклеточным щелям через эпителиальный барьер, проникают в ткани, а затем – в лимфатические капилляры, и с током периферической лимфы заносятся в лимфатические узлы. Выйдя из лимфоузлов, лимфоциты через грудной лимфатический проток снова оказываются в крови.
Пре-В-лимфоциты из красного костного мозга через кровеносную систему переходят в селезёнку, групповые лимфатические фолликулы и лимфатические узлы, где заселяют тимуснезависимые зоны. Эти клетки мигрируют значительно в меньшей степени, чем Т-лимфоциты, но при антигенной стимуляции их подвижность усиливается в тысячи раз.
Выйдя в кровоток, часть В-лимфоцитов мигрирует в красный костный мозг, где участвует в дифференцировке стволовых клеток и отбору тех клонов, которые будут синтезировать специфические антитела.
Миграция лимфоцитов по кровеносным и лимфатическим сосудам позволяет осуществлять иммунный надзор над всеми регионами организма, его органами и тканями, создает возможность генерализации иммунного ответа и обеспечивает функционирование иммунной системы как единого целого.
Механизмы иммунного ответа
Иммунный ответ включает в себя распознавание антигена, активацию лимфоцитов и выполнение ими клеточных и гуморальных реакций, направленных на обезвреживание или уничтожение чужеродного материала.
Распознавание антигена осуществляют Т-лимфоциты, причём только на поверхностях клеток – или «чужих» клеток, в том числе микробных, или фагоцитов. Более эффективно для последующей активации лимфоцитов представление (презентация) антигена на поверхности макрофагов.
Под антигенпрезентацией понимают процесс поглощения антигена особыми клетками (их называют антигенпрезентирующие, А-презентирующие клетки, или А-клетки), переработку антигена и выведение наиболее значимой части антигена в соединении с ГКГС на поверхность мембраны. Только в таком виде антиген может быть распознан лимфоцитами. Одновременно А-презентирующая клетка секретирует интерлейкин-1. Эти процессы в макрофагах начинаются в месте встречи их с антигеном, и продолжаются по пути миграции макрофага к ближайшему региональному лимфатическому узлу.
Активация лимфоцитов. Т-лимфоциты распознают на мембране А-клетки измененный антигеном участок ГКГС, признают его чужеродным, в присутствии ИЛ1 сближаются с А-клеткой.
В результате Т-лимфоцит приобретает новое качество – он становится активным киллером, хелпером, супрессором или клеткой памяти. Активированные Тh секретируют ряд лимфокинов, активирующих В-лимфоциты и вызывающих пролиферацию определенного клона В-лимфоцитов. Кроме того, лимфокины стимулируют секрецию В-лимфоцитами IgM, а затем переключение синтеза на IgG.
Активированные Тs угнетают превращение В-лимфоцитов в плазматические клетки, синтез ими антител. В результате иммунный ответ прекращается или снижается его интенсивность, тем самым регулируется адекватность иммунной реактивности.
Для активации В-лимфоцитов также необходимы кооперативные отношения с А-презентирующей клеткой, несущей антигенную детерминанту, контакт с Тh и интерлейкином.
Клеточные реакции иммунитета. Тk реагируют на клеточные рецепторы главного комплекса гистосовместимости, изменённые мутацией, химическими веществами, старением или присоединением к ним чужеродного антигена. Таким образом, даже небольшие изменения ГКГС могут быть причиной превращения собственных клеток в мишени для Т-лимфоцитов. Получив помощь от Тh, активированные Т-лимфоциты превращаются в клетки-убийцы.
Способов уничтожения мишеней у Тk много, они весьма изощрённые. В одних случаях необходимо межклеточное взаимодействие: Т-киллер сближается с клеткой-мишенью, межклеточные щели сужаются, в это пространство Тk выделяет лизины, проделывающие в мембране отверстия. Через бреши в мембране в клетку поступает вода и клетка разрушается.
В других случаях Т-лимфоцит выпускает отростки, образующие высокопроницаемые контакты с мембраной изменённой клетки – «поцелуй смерти». Через них в жертву вводятся лимфотоксины – вещества, повреждающие внутриклеточные компоненты клетки: монооксид азота, активный кислород, перекись водорода, свободные галогены, различные ферменты. Ещё один способ уничтожения чужой клетки – введение в неё веществ, включающих апоптоз – запрограммированную в геноме клетки программу её гибели.
После такой атаки Тk не погибает, он может поразить несколько клеток.
Гуморальные механизмы иммунной реакции осуществляются антителами, продуцируемыми плазматическими клетками. В результате межклеточного взаимодействия и участия интерлейкинов происходит отбор тех В-клеток, которые несут на мембране иммуноглобулиновые рецепторы того же строения, что и антигенная детерминанта. Далее происходит размножение (пролиферация) клона В-лимфоцитов, трансформация их в плазматические клетки (последняя фаза клеточного цикла) и нарастание скорости секреции антител.
Если неактивированный В-лимфоцит синтезирует за час до 500 молекул иммуноглобулинов, причем, только класса М, то одна плазматическая клетка образует за такое же время более 10 миллионов молекул иммуноглобулинов, причём, различных классов, больше всего – IgG.
Уникальной особенностью антителогенеза является выработка именного того единственного типа иммуноглобулина, одного из многих миллионов вариантов, который может образовать комплекс с данным антигеном. Поскольку чужеродные клетки (например, бактериальные) несут на своей поверхности не одну, а множество антигенных детерминант, то в иммунный ответ вовлекаются многие клоны лимфоцитов и синтезируется не один вариант иммуноглобулина, а столько, сколько имелось антигенов.
Синтезированные в результате гуморального иммунного ответа антитела (иммуноглобулины) образуют комплексы с антигенами, их называют иммунными комплексами. Дальнейшая судьба иммунных комплексов различна, она зависит от вида антител, размера и количества. Иммунные комплексы могут присоединять к себе компоненты комплемента и растворяться, могут выпадать в осадок (преципитация), они могут быть захвачены фагоцитами и подвергнуться полному уничтожению. В любом случае антиген в комплексе с антителом должен быть уничтожен и элиминирован (выведен) из организма.
Таким образом, в организме возможен синтез многих миллиардов разновидностей антител, то есть человек или животные хорошо подготовлены к встрече с любым возможным антигеном. Такое разнообразие достигается многими, еще недостаточно изученными механизмами – например, путем рекомбинации генов, а также их наследственной неоднородностью в хромосомах. Антитела вырабатываются даже к таким антигенам, которые никогда ещё не существовали в природе.
В течение индивидуальной жизни используется очень небольшая часть антител. В организме образуется большое число клонов лимфоцитов, и только некоторые из них будут когда-либо участвовать в иммунной защите. Однако такая «расточительность» позволяет сохранять высокую степень готовности к возможному появлению новых инфекционных болезней, мутировавшим микроорганизмам и вирусам и новым (искусственным) антигенам.
Иммунологическая память
Иммунологическая память – это способность лимфоидных клеток сохранять информацию об антигене и отвечать ускоренной и усиленной реакцией на повторную встречу с тем же антигеном. Это явление основано на том, что при первой встрече с антигеном (в процессе болезни или иммунизации) в ходе иммунного ответа образуются Т- и В-клетки памяти.
Низкие дозы антигена обычно не вызывают гуморального иммунного ответа, то есть не сопровождаются выработкой антител, но приводят к образованию Т-клеток памяти. Большие дозы антигена формируют В-клетки памяти. По сравнению с пре-В-лимфоцитами, эти клетки имеют бóльшую плотность иммуноглобулиновых рецепторов на мембране.
Клетки памяти могут сохраняться в организме достаточно длительное время в покоящемся (неактивном) состоянии. Приобретенный иммунитет сохраняется от нескольких месяцев до многих лет, а при некоторых болезнях – на всю жизнь.
При повторной встрече с антигеном клетки иммунологической памяти активируются, пролиферируют и образуют множество лимфоцитов одного клона, превращающихся в плазматические клетки. В таком случае повторное заболевание протекает легче, быстрее, с меньшими клиническими признаками, или вообще не развивается. Это объясняется достаточной выработкой иммуноглобулинов, связывающих антигены в иммунные комплексы с последующим выведением (элиминацией) их из организма.
Физиология сердца
Свойства сердечной мышцы
Основными физиологическими свойствами сердца являются: автоматия, возбудимость, сократимость и проводимость.
Автоматия сердца. Под автоматией понимают спосособность сердца ритмически сокращаться и расслабляться без каких-либо внешних по отношению к сердцу воздействий, то есть без участия нервной системы или гуморальных (химических) раздражителей, приносимых к сердцу кровью
У позвоночных животных автоматия сердца объясняется наличием в сердце специализированных атипических мышечных клеток – пейсмекеров, составляющих проводящую систему сердца. Эти мышечные волокна не способны к сокращению, их функция – генерация потенциала действия (ПД) и передача его на сократительные мышечные волокна. Проводящая система сердца включает в себя синусный узел, атриовентрикулярный узел, пучок Гиса, ножки пучка Гиса и тончайшие разветвления – волокна Пуркинье.
Ведущую роль в автоматии играет синусный, или атриальный узел, или узел Кейт-Флака. Его называют водителем ритма сердца первого порядка. В клетках этого узла спонтанно, ритмически возникает ПД, он распространяется на предсердия, атриовентрикулярный узел, пучок Гиса и далее – до сократительных волокон сердца. Та частота сокращения сердца, которая обусловлена возбуждением синусного узла, называется синусным ритмом.
Если синусный узел оказывается изолированным от сердца, тогда водителем ритма становится атриовентрикулярный узел (узел Ашоф-Тавара), но его возбудимость меньше и он задаёт более редкий ритм сердечных сокращений. Этот узел называют водителем ритма сердца второго порядка.

Пучок Гиса – водитель ритма сердца третьего порядка, так как он обладает ещё меньшей возбудимостью и задаёт свой ритм только в тех случаях, когда первые два узла бездействуют. Атриовентрикулярный узел и пучок Гиса называют скрытыми, или латентными пейсмекерами, они становятся водителями сердца только в условиях патологии.
Волокна Пуркинье не обладают автоматией, их значение заключается в передаче ПД на сократительные волокна миокарда.
Рис. 4. Проводящая система сердца:
1 – синусный узел;
2 – атриовентрикулярный узел;
3 – пучок Гиса; 4 – ножки пучка Гиса.
Возбудимость – свойство сердечной мышцы переходить в состояние возбуждения под влиянием различных раздражителей. В естественных условиях этим раздражителем является ПД, возникающий в синусном узле и распространяющийся по проводящей системе до сократительных мышечных волокон.
Во время возбуждения в сердечной мышце происходят физико-химические, биохимические и морфологические изменения, которые завершаются сокращением. Наиболее ранним признаком возбуждения является генерация потенциала действия.
Потенциал покоя в миокардиоцитах имеет величину 80 – 90 мВ, наружная поверхность мембран миокардиоцитов имеет положительный заряд. Под влиянием электрического импульса, поступающего от проводящей системы сердца, начинается активация натриевых и кальциевых каналов. Входящие через мембрану ионы Na+ и Ca+2 снижают мембранный потенциал до критического уровня, и возникает ПД; его величина 110 – 120 мВ, причём теперь снаружи мембрана заряжена отрицательно, а внутри – положительно (фаза деполяризации). Затем начинаются восстановительные процессы: открываются калиевые каналы и увеличивается ток К+ из клеток; одновременно кальциевые и натриевые каналы закрываются, ионные насосы выкачивают Na+ и Ca+2 из клетки и закачивают в клетку К+ (фаза реполяризации). В результате мембранный потенциал возвращается к уровню покоя.
ПД в пейсмекерах имеет важную особенность: здесь почти не бывает потенциала покоя, а после окончания ПД сразу спонтанно начинается медленная деполяризация мембраны, приводящая к новому ПД. В этом механизме и заключается уникальное свойство сердца – автоматия.
Изменения возбудимости сердца во время возбуждения. Во время фазы деполяризации сердце находится в состоянии абсолютной рефрактерности, или невозбудимости. Это объясняется тем, что все натриевые и кальциевые каналы «заняты» проведением ионов, поэтому на любое раздражение в данное время сердце не ответит. В отличие от других возбудимых тканей, фаза абсолютной рефрактерности в сердце очень продолжительная, по времени она совпадает с периодом систолы (предсердий или желудочков). Благодаря этому сердце не способно к непрерывному, или тетаническому сокращению.
Во время реполяризации, которая совпадает с началом диастолы, возбудимость сердца постепенно восстанавливается; хотя натриевые и кальциевые каналы инактивированы, но часть их уже способна пропустить новый поток ионов. Это – фаза относительной рефрактерности. Если в этот момент на сердце будет действовать новый раздражитель, то в сердце возникает внеочередное возбуждение и сокращение, которое называется экстрасистолой (рис. 5).
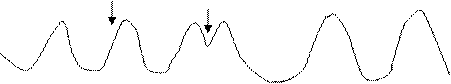
Рис. 5. Запись сокращений желудочков сердца.
Восходящая часть – систола желудочков, нисходящая – диастола. Стрелками показано нанесение раздражения. Если раздражение совпадает с систолой, то сердечный цикл не меняется, а с началом диастолы – возникает экстрасистола
После желудочковой экстрасистолы, то есть возникшей при нанесении внеочередного раздражения на желудочек, имеет место более длительная пауза, она называется компенсаторной. Экстрасистолы рассматриваются как нарушения сердечного ритма, но у молодых животных вследствие несовершенства регуляторной системы возможны редкие единичные экстрасистолы, не требующие лечения.
В конце диастолы имеется очень кратковременный период экзальтации, или повышенной возбудимости.
Проводимость – свойство сердечной мышцы проводить возбуждение, то есть передавать ПД на соседние участки. Зарождаясь в синусном узле, ПД распространяется вначале по предсердиям. Здесь очень мало волокон проводящей системы, поэтому возбуждение распространяется и по ним, и по поверхности сократительных волокон – с одного мышечного волокна на другое. В предсердиях скорость передачи возбуждения невелика – до 1 м/сек.
Когда возбуждение распространится по предсердиям, они сокращаются, а желудочки находятся еще в диастоле. Это объясняется задержкой возбуждения в атриовентрикулярном узле, где скорость возбуждения самая маленькая в сердце – 2 – 4 см/сек.
По проводящей системе желудочков возбуждение передается с очень большой скоростью – до 4 – 5 м/сек, поэтому, несмотря на большую массу желудочков, возбуждение охватывает их практически мгновенно, что вызывает синхронное сокращение миокардиоцитов желудочков.
Сократимость. Под сократимостью понимают способность миокардиоцитов сокращаться под воздействием потенциала действия. Это – функция миофибрилл. Как и в мышцах других типов – гладких, поперечно-полосатых, сокращение миофибрилл происходит за счет скольжения актиновых протофибрилл между миозиновыми. Большое значение в процессе мышечного сокращения имеет Ca+2, помимо участия в генерации потенциала действия, он регулирует положение молекул тропомиозина. Это – белок, расположенный между актиновыми и миозиновыми нитями, от его конформации зависит возможность взаимодействия между актином и миозином.
Сердечная мышца – функциональный синцитий, и сокращается как единое целое. Поэтому сердце на раздражение реагирует так же, как одиночное мышечное волокно, по закону «всё или ничего». Этот закон называется законом Боудича: на подпороговое раздражение сердце не реагирует («ничего»), а на раздражение пороговой силы отвечает максимальным сокращением («всё»).
Закон Франка-Старлинга: сила сокращения сердца зависит от первоначальной длины мышечных волокон, то есть от их растяжения кровью во время диастолы. Чем больше крови попадает в сердце во время расслабления, тем с большей силой оно сокращается. Этим объясняется, что при физической нагрузке увеличивается кровенаполнение сердца и возрастает сила его сокращения.
Круги кровообращения
Кровь движется в замкнутой сосудистой сети по двум кругам кровообращения – большому и малому.
Большой круг кровообращения: левый желудочек – аорта, артерии, артериолы, капилляры, венулы, вены; две крупные вены – краниальная и каудальная впадают в правое предсердие. Значение большого круга кровообращения – доставка кислорода и питательных веществ к тканям и перенос от них продуктов обмена.
Малый, или лёгочной круг: правый желудочек, лёгочная артерия, артериолы, капилляры, вены; несколько крупных лёгочных вен впадают в левое предсердие. Значение малого круга кровообращения – оксигенация венозной крови.
К большому кругу кровообращения относятся несколько добавочных кругов, отражающих особенности сосудистой системы в печени, почках и сердце.
Система воротной вены: в печень поступает артериальная кровь по печеночной артерии и венозная кровь – по воротной вене от органов брюшной полости, главным образом – от желудка и кишечника. В печени эти крупные сосуды разветвляются на капилляры, затем из капилляров венозная кровь собирается в печёночные вены, которые впадают в каудальную полую вену.
В почках кровь дважды проходит через капилляры. В первый раз – через капилляры мальпигиева тельца в капсуле Шумлянского-Боумена, это – артериальные капилляры («чудесная сеть»). Из капсулы Шумлянского-Боумена отводящая артериола вдоль канальцев нефрона, где снова разветвляется на капилляры, и образовавшаяся венозная кровь оттекает в почечные вены.
В сердце артериальная кровь поступает по двум коронарным артериям – правой и левой. Во время систолы эти артерии почти полностью пережимаются, кровь к миокарду практически не поступает, и в сердце происходят анаэробные процессы. Во время диастолы приток крови к сердечной мышце увеличивается и начинается аэробный гликолиз. Венозная кровь от сердца оттекает в венозный синус в правом предсердии и через сосуды Тибезия – непосредственно в полость предсердий.
Сосудосуживающие вещества
Катехоламины (адреналин, норадреналин, допамин) имеют различное происхождение. Они являются медиаторами адренергических нервов, медиаторами в ЦНС, а также гормонами мозгового слоя надпочечников. Влияние катехоламинов на кровеносные сосуды в разных органах различно и по направленности, и по величине. Это зависит от наличия на мембранах гладкомышечных клеток двух типов адренорецепторов – α и β. При взаимодействии катехоламинов с α-адренорецепторами сосуды сужаются, с β-адренорецепторами – расширяются.
Норадреналин действует преимущественно на α-адренорецепторы, то есть сужает сосуды, а адреналин – на оба типа рецепторов. В большинстве кровеносных сосудов имеются и те, и другие рецепторы, но их количество и соотношение может быть различным. Если в сосудах больше α-адренорецепторов, то адреналин вызывает их сужение, а если больше β-адренорецепторов, то их расширение.
Порог возбудимости β-адренорецепторов ниже, чем α-адренорецепторов. Поэтому в малых дозах адреналин вызывает расширение сосудов, а в больших – сужение.
При высоком уровне адреналина в крови артериальное давление в крупных сосудах увеличивается. При этом усиливается работа сердца, и повышаются систолический и минутный объём крови, сужаются сосуды кожи и органов брюшной полости (но одновременно расширяются сосуды сердца, скелетных мышц и мозга), и увеличивается объём циркулирующей крови за счёт кровяных депо.
Норадреналин сужает артерии и немного повышает артериальное давление, но также он уменьшает работу сердца путём воздействия на сосудистые рефлексогенные зоны.
Ренин-ангиотензин-альдостероновая система. Ренин – гормон, синтезирующийся постоянно в юкстагломерулярном аппарате почек, но его уровень увеличивается при снижении кровотока или кислородном голодании почек. Поэтому первичное значение ренина – усиление кровообращения в самой почке. Однако через кровь он действует и на сосуды других органов.
По механизму действия ренин является ферментом, он активизирует сосудосуживающее вещество, находящееся в плазме крови – ангиотензиноген и превращает его ангиотензин-1. В лёгких ангиотензин-1 превращается в ангиотензин-2, и его активность увеличивается в 50 раз. Ангиотензин-2, во-первых, сам является мощным сосудосуживающим веществом в отношении артериол и венул, а во-вторых, он вызывает выделение из надпочечников альдостерона. Альдостерон повышает уровень натрия в крови и увеличивает объём крови, что также способствует увеличению кровяного давления.
Вазопрессин, или антидиуретический гормон – гормон задней доли гипофиза. В небольшой концентрации вазопрессин стимулирует обратное всасывание воды в почечных канальцах, тем самым повышает объём крови. В более высоких концентрациях вазопрессин сужает артериолы, капилляры и венулы, и не только в почках, но и в других органах.
Серотонин образуется в различных органах – в слизистой кишечника, в головном мозге, при разрушении тромбоцитов. Важное значение имеет местный сосудосуживающий эффект серотонина при травмах и кровотечениях. Однако при высоком тонусе гладких мышц сосудов серотонин является дилятатором.
Сосудорасширяющие вещества
Ацетилхолин – медиатор парасимпатических нервов. Выделяясь из окончаний парасимпатических нервов, ацетилхолин взаимодействует с М-холинорецепторами (мускариновые холинорецепторы), в результате чего происходит расслабление гладких мышц сосудов. Ацетилхолин быстро разрушается ферментом ацетилхолинэстеразой, поэтому он обладает местным и кратковременным эффектом.
Кинины (калликреин, каллидин, брадикинин) – образуются в различных тканях и вызывают местную дилятацию. Так, они увеличивают приток крови к пищеварительным железам, к потовым железам при потоотделении, расширяют кожные сосуды при повышении температуры.
Гистамин секретируется базофилами и тучными клетками. Он вызывает местное сосудорасширяющее действие на артериолы, капилляры и венулы, увеличивает тем самым приток крови к участку ткани. Гистамин повышает проницаемость капилляров, увеличивает образование тканевой жидкости. В большой концентрации гистамин может вызвать перераспределение крови в организме, тогда за счёт переполнения капиллярного русла снижается артериальное давление.
Медуллин – тканевой гормон почек, в небольших дозах расширяет сосуды почек, при более высокой концентрации – и в других органах.
Простагландины – тканевые гормоны – производные арахидоновой кислоты, действуют на многие функции организма; некоторые простагландины являются сосудосуживающими веществами.
Вазодилятаторами являются также кислые продукты обмена веществ (молочная, фосфорная, угольная кислоты и др. и их соли), АТФ, ионы натрия, магния, ртути, кадмия.
Тонус сосудов зависит от газового состава крови: снижение концентрации О2 и увеличение СО2 вызывают расширение сосудов.
Физиология дыхания
Внешнее дыхание
Внешнее дыхание, или вентиляция лёгких – это газообмен между альвеолами лёгких и окружающим воздухом. Оно складывается из вдоха и выдоха. Лёгкие расширяются при вдохе и спадаются при выдохе в результате изменения давления в грудной полости.
Грудная полость – это узкая капиллярная щель между париетальным и висцеральным листками плевры, заполненная серозной жидкостью. До рождения головки рёбер зафиксированы у тел позвонков – в одной точке. Рёбра опущены, грудная клетка сжата, давление в грудной полости равно атмосферному. В момент первого вдоха новорожденного рёбра приподнимаются, и рёберные бугорки фиксируется на поперечно-остистом отростке позвонков – во второй точке фиксации. В результате объём грудной полости увеличивается, а давление в ней снижается, и становится ниже атмосферного, или отрицательным. Во время выдоха рёбра сохраняют новое положение, грудная полость остается несколько растянутой и давление в ней остается отрицательным.
Вдох
Последовательностьпроцессов при вдохе следующая:
1. Сокращается группа вдыхательных (инспираторных) мышц, основными из которых являются наружные межреберные мышцы и диафрагма. При этом органы брюшной полости, сдавленные диафрагмой, оттесняются в каудальном направлении, рёбра описывают дугу кверху, а грудная кость немного опускается.
2. Изменения положения рёберной клетки и диафрагмы приводит к увеличению объёма грудной полости.
3. Увеличение объёма грудной полости приводит к снижению в ней давления, в результате лёгкие растягиваются, пассивно следуя за изменениями объёма грудной полости
4. В альвеолах давление снижается и в них засасывается воздух.
При усиленном дыхании участвуют дополнительные респираторные мышцы, которые при сокращении ещё больше увеличивают объём грудной полости и снижают в ней давление. Поэтому вдох оказывается более глубоким, и в лёгкие входит больше воздуха.
Выдох
Выдох начинается с расслабления мышц-инспираторов, вследствие чего грудная клетка возвращается в исходное положение. Давление в грудной полости при этом повышается, не достигая, однако, атмосферного. В лёгких, однако, давление становится выше атмосферного, что приводит к вытеснению воздуха и уменьшению их объёма. Сжатию лёгких во время выдоха способствует эластическая тяга паренхимы. Включение в работу мышц-экспираторов (в основном, внутренних межреберных мышц и мышц живота) необходимо только при усиленном, форсированном дыхании.
Изменения давления в грудной (то есть плевральной) полости во время дыхания следующие:
1. При спокойном вдохе оно меньше атмосферного (то есть отрицательное) на 30 мм рт. ст., при спокойном выдохе – на 5 – 8. При очень глубоком вдохе (например, перед чиханием, или при мышечной нагрузке) – становится на 60-65 мм рт.ст.ниже атмосферного, а при полном, максимальном выдохе (в конце чихания, например), – оно на 1,5 – 2 мм ниже атмосферного.
2. При изменениях атмосферного давления в окружающей среде давление в грудной полости также изменяется, но всё равно остается отрицательным на указанные величины.
Таким образом, давление в плевральной полости всегда отрицательное. При нарушении целостности грудной полости (проникающее ранение или разрыв поверхностных альвеол) атмосферный воздух засасывается в плевральную полость. Такое состояние называется пневмотораксом. Давление в грудной полости выравнивается с атмосферным, лёгкие спадаются за счёт эластичной тяги, и дыхание становится невозможным.
Количество дыхательных движений у животных в 1 минуту – видовой признак. У лошадей в состоянии покоя оно составляет 8 – 16, у коров – 10 – 30, у свиней – 8 – 18, у собак –10 – 30, у кошек 10 – 25, у морских свинок – 100 – 150.
Вентиляция лёгких
При спокойном дыхании животные вдыхают и выдыхают сравнительно небольшое количество воздуха, именуемое дыхательным (респираторным) объёмом: у лошади и коровы он составляет – 5 – 6, у крупных собак – около 0,5 литра.
При максимальном вдохе животное может вдохнуть больше – это дополнительный объём вдоха (у крупных животных он колеблется от 10 до 12, у крупных собак – равняется 1 литру), а после спокойного выдоха – дополнительно столько же выдохнуть (резервный объём выдоха). Сумма дыхательного, дополнительного объёма вдоха и дополнительного объёма выдоха составляет жизненную ёмкость лёгких. Дополнительные объёмы используются при усилении дыхания – например, во время физической работы.
После спокойного выдоха в